⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
El mecanismo de fármaco comprende la interacción específica del fármaco con dianas biológicas, regulada por farmacocinética y farmacodinamia, que determina el efecto terapéutico y la variabilidad en la respuesta clínica.
🧬 Concepto base
Es la secuencia de procesos moleculares y celulares que produce efectos del fármaco en el organismo. Define cómo el fármaco se absorbe, distribuye, metaboliza, elimina y actúa en su blanco específico.
⚙️ Mecanismo clave
El fármaco une dianas (receptores, enzimas, canales, transportadores), modula funciones celulares y genera señalización que provoca respuestas biológicas con potenciales efectos beneficiosos o adversos.
🔗 Por qué es importante
Permite entender la variabilidad interindividual, predecir efectos adversos y optimizar el uso terapéutico mediante ajustes basados en genética y estado fisiopatológico.
🎯 Puntos que suelen preguntarse en examen
- Diferencia entre farmacocinética y farmacodinamia en el mecanismo de fármaco
- Rol de receptores y enzimas en la acción farmacológica
- Influencia de variabilidad genética en metabolismo y respuesta
- Efecto de la unión a proteínas plasmáticas sobre la biodisponibilidad
- Concepto y consecuencias del efecto de primer paso
- Clasificación básica de reacciones adversas tipo A y B
Palabras clave: mecanismo de fármaco, farmacocinética, farmacodinamia, receptores, metabolismo, transportadores, índice terapéutico, reacciones adversas
El mecanismo de fármaco se refiere al conjunto encadenado de procesos moleculares, celulares y tisulares por los cuales una sustancia produce efectos en el organismo humano.
Analizar estos pasos intermedios permite comprender la variabilidad en la respuesta farmacológica, la relación entre dosis y efecto, y los riesgos y beneficios de la intervención con fármacos en seres humanos.
🧠 Idea central
El mecanismo de fármaco integra una secuencia de interacciones específicas entre una molécula exógena—el fármaco—y dianas biológicas, así como los procesos de transporte, metabolismo y eliminación que determinan su concentración, distribución y acción final.
Este concepto es fundamental porque explica cómo una sustancia es capaz de modular procesos fisiológicos, desencadenar efectos adversos o producir beneficios terapéuticos a distintos niveles organizativos del cuerpo humano.
Para comprender el mecanismo de un fármaco, es necesario considerar dos dimensiones complementarias: la farmacocinética (cómo el organismo maneja el fármaco: absorción, distribución, metabolismo y excreción) y la farmacodinamia (cómo el fármaco modifica funciones biológicas tras alcanzar su sitio de acción).
Variaciones a nivel genético, enfermedad concomitante y otras variables personales influyen en ambos aspectos y, por tanto, en la respuesta al fármaco.
🌍 Contexto y alcance
El estudio del mecanismo de fármaco abarca distintas escalas biológicas:
- Nivel molecular: Interacciones entre el fármaco y proteínas específicas (receptores, enzimas, transportadores).
- Nivel celular: Modulación de actividades intracelulares, señalización y modificaciones específicas en células blanco.
- Nivel tisular y sistémico: Cambios en el funcionamiento de órganos o sistemas corporales, resultado acumulativo de efectos celulares.
La farmacología clínica analiza cómo la administración del fármaco resulta en efectos observables, identificando factores que modulan el mecanismo, como la variabilidad genética, interacciones medicamentosas, estado fisiopatológico del paciente y características socioambientales, incluyendo adherencia al tratamiento.
No todo mecanismo de acción es constante entre individuos: alteraciones en la expresión génica, presencia de enfermedades o coadministración de otros compuestos pueden modificar tanto las concentraciones efectivas del fármaco (farmacocinética) como la respuesta del sistema efector (farmacodinamia).
Estas consideraciones fundamentan la farmacogenómica y la individualización terapéutica.
🧬 Estructuras clave
Las interacciones biológicas de los fármacos dependen de estructuras específicas que median su acción. Cada una desempeña roles y mecanismos distintivos:
- Receptores:
- ¿Qué son?: Proteínas especializadas, transmembrana o intracelulares, capaces de unirse selectivamente a ligandos exógenos (fármacos) para iniciar señalización.
- ¿Dónde actúan?: Membranas celulares, citoplasma o núcleos celulares de células blanco.
- ¿Qué producen?: Transducción de señales químicas en respuestas celulares (modificación de segundos mensajeros, fosforilación, regulación génica).
- ¿Cómo funcionan?: El fármaco se une al sitio activo, alterando la conformación del receptor y desencadenando cascadas intracelulares.
- ¿Qué ocurre si se altera?: Mutaciones o regulación anómala pueden modificar sensibilidad o resistencia farmacológica.
- Enzimas:
- ¿Qué son?: Catalizadores biológicos que aceleran reacciones específicas y pueden ser blancos farmacológicos de inhibición o activación.
- ¿Dónde actúan?: Principalmente en citoplasma, membrana y ocasionalmente en plasma.
- ¿Qué producen?: Modifican rutas metabólicas, alterando concentración de sustratos o productos fisiológicos.
- ¿Cómo funcionan?: El fármaco puede unirse al sitio catalítico o alostérico, modulando la actividad enzimática.
- ¿Qué ocurre si se altera?: Cambios en función enzimática afectan flujos metabólicos, pudiendo causar desequilibrios o potenciar efectos terapéuticos.
- Canales iónicos:
- ¿Qué son?: Complejos transmembrana que permiten el paso selectivo de iones según gradientes electroquímicos.
- ¿Dónde actúan?: Membranas plasmáticas de células excitables (neuronas, músculo cardíaco y esquelético).
- ¿Qué producen?: Regulan potencial de membrana, propagación eléctrica y liberación de neurotransmisores.
- ¿Cómo funcionan?: El fármaco puede bloquear, abrir o modular estos canales, alterando excitabilidad celular.
- ¿Qué ocurre si se altera?: Disfunciones pueden causar hipo- o hiperexcitabilidad, o alteraciones en ritmos biológicos.
- Transportadores y bombas:
- ¿Qué son?: Proteínas que median el paso activo o facilitado de sustancias (iones, moléculas pequeñas) a través de membranas.
- ¿Dónde actúan?: Enterocitos, hepatocitos, barrera hematoencefálica y otros epitelios.
- ¿Qué producen?: Controlan distribución y eliminación de fármacos, nutrientes o metabolitos.
- ¿Cómo funcionan?: El fármaco puede inhibir o potenciar transportadores, afectando absorción, distribución y barreras biológicas.
- ¿Qué ocurre si se altera?: Variabilidad genética o inhibición modifican biodisponibilidad y penetración tisular.
Estas estructuras fundamentan la especificidad y selectividad farmacológica. Su distribución y expresión varían entre tejidos, explicando efectos localizados o sistémicos.
⚙️ Funciones y procesos
El mecanismo de fármaco se descompone en etapas secuenciales desde la administración hasta la respuesta biológica observable. Cada paso puede describirse así:
-
Absorción
- ¿Qué es?: Ingreso del fármaco a la circulación sistémica desde el sitio de administración.
- ¿Dónde ocurre?: Mucosa intestinal (vía oral), tejidos subcutáneos o musculares (vía parenteral), mucosa oral (sublingual), entre otros.
- ¿Qué permite?: Determina velocidad y extensión del acceso sistémico (biodisponibilidad).
- ¿Cómo funciona?:
- Difusión pasiva, transporte activo o endocitosis atraviesan membranas celulares.
- Factores como pH, solubilidad y transportadores influyen en la absorción.
- ¿Qué ocurre si se altera?: Baja absorción o metabolismo presistémico reducen eficacia.
-
Distribución
- ¿Qué es?: Movimiento del fármaco desde sangre hacia tejidos y órganos.
- ¿Dónde ocurre?: Por todo el organismo, regulado por flujo sanguíneo, permeabilidad capilar y unión a proteínas plasmáticas.
- ¿Qué permite?: Alcance y concentración en sitio diana.
- ¿Cómo funciona?:
- Se distribuye según gradientes de concentración y barreras físicas; unión proteica afecta fracción libre activa.
- Presencia de barreras restrictivas limita acceso a algunos órganos.
- ¿Qué ocurre si se altera?: Cambios en perfusión, proteínas o integridad de barreras modifican respuesta clínica.
-
Metabolismo
- ¿Qué es?: Transformación química del fármaco para facilitar eliminación.
- ¿Dónde ocurre?: Principalmente hígado, también riñón, intestino, pulmón y plasma.
- ¿Qué produce?: Metabolitos más polares, usualmente menos activos; algunos mantienen o adquieren actividad farmacológica.
- ¿Cómo funciona?:
- Fase I: modificaciones químicas (oxidación, reducción, hidrólisis) mediadas por citocromo P450.
- Fase II: conjugación con compuestos endógenos para facilitar excreción.
- Pro-fármacos requieren metabolismo para activación.
- ¿Qué ocurre si se altera?: Polimorfismos, inhibidores/inductores enzimáticos o enfermedades afectan metabolismo y acción.
-
Eliminación
- ¿Qué es?: Retiro del fármaco o metabolitos del organismo.
- ¿Dónde ocurre?: Principalmente riñón (excreción urinaria), también hígado (bilis), pulmón (aire exhalado) y piel (sudoración).
- ¿Qué permite?: Limita duración y magnitud del efecto farmacológico.
- ¿Cómo funciona?:
- Filtración glomerular, secreción y reabsorción tubular determinan excreción en orina.
- El metabolismo genera compuestos más eliminables.
- Patologías renales o hepáticas disminuyen depuración y prolongan vida media.
-
Unión y acción en blanco molecular
- ¿Qué es?: Interacción física y química específica entre fármaco y diana (receptor, enzima, canal, transportador).
- ¿Dónde ocurre?: Depende de la diana, puede ser membrana, citosol o compartimentos extracelulares.
- ¿Qué permite?: Desencadena respuesta funcional que conduce al efecto farmacodinámico.
- ¿Cómo funciona?:
- Puede resultar en activación, inhibición, bloqueo o modulación alostérica.
- Afinidad y selectividad determinan potencia y especificidad.
-
Transducción de señal y respuesta biológica
- ¿Qué es?: Cambios celulares internos tras unión fármaco-diana.
- ¿Dónde ocurre?: Citoplasma, núcleo, membrana o compartimentos subcelulares según diana.
- ¿Qué produce?: Cambios en expresión génica, síntesis proteica, regulación metabólica y funciones celulares.
- ¿Cómo funciona?:
- Señales se amplifican mediante segundos mensajeros, cascadas enzimáticas y modificaciones postraduccionales.
- Magnitud, duración y naturaleza de la respuesta dependen de cantidad de diana, persistencia del fármaco y regulación interna.
Cada paso puede estar influido por variantes genéticas, enfermedades, interacciones con otros fármacos y factores ambientales.
La alteración en una etapa puede modificar la respuesta, amplificándola, reduciéndola o anulándola.
🔗 Integración funcional del mecanismo de fármaco
La eficacia y seguridad de un fármaco dependen de la integración funcional de su mecanismo a lo largo de todas las fases mencionadas.
Diversos factores biológicos y clínicos pueden afectar cada etapa y el resultado clínico final:
- Variabilidad genética: Polimorfismos en enzimas metabolizadoras (como citocromo P450), transportadores o dianas moleculares modulan magnitud y duración del efecto.
- Interacciones medicamentosas: Coadministración puede inhibir o inducir rutas metabólicas, alterar unión proteica o compartir blancos, cambiando acción terapéutica o tóxica.
- Estado fisiopatológico: Enfermedad renal, hepática, insuficiencia cardíaca o cambios en desarrollo (pediatría, envejecimiento) modifican absorción, distribución, metabolismo y excreción, afectando dosis y respuesta.
- Factores poblacionales y adherencia: Varianza interindividual y cultural influye en cumplimiento terapéutico, afectando eficacia y riesgo.
Alteraciones en estos elementos pueden impactar la función celular y sistémica, modificando la homeostasis y la susceptibilidad a reacciones adversas o fracaso terapéutico.
🔬 Métodos y evidencias en el estudio del mecanismo de fármaco
La elucidación de mecanismos farmacológicos utiliza enfoques experimentales y analíticos para definir la interacción del fármaco con sus blancos:
- Análisis bioquímico: Identificación de interacciones enzimáticas y velocidad de transformación de fármacos y metabolitos.
- Electrofisiología: Estudio de modulación de canales iónicos y función eléctrica celular.
- Biología molecular: Técnicas como PCR, secuenciación y edición génica para manipular expresión de blancos o rutas metabólicas.
- Medición de concentraciones plasmáticas: Caracterización farmacocinética mediante niveles séricos y parámetros como vida media y clearance.
- Modelos celulares y animales: Aislamiento y validación de mecanismos antes de extrapolación a humanos.
- Análisis ómicos y de sistemas: Integración de transcriptómica, metabolómica y proteómica para comprender variabilidad interindividual y nuevas dianas terapéuticas.
Estas herramientas sustentan la predicción, identificación y explicación de variabilidad, efectos adversos y optimización terapéutica.
🩺 Puente clínico: relación entre el mecanismo de fármaco y su aplicación biomédica
Comprender los mecanismos de fármaco es esencial para predecir y explicar la variabilidad en la respuesta, efectos adversos tanto esperados como inesperados y diferencias interindividuales.
La relación dosis–respuesta refleja cómo los efectos beneficiosos y tóxicos dependen de la concentración en el sitio de acción.
El índice terapéutico representa el margen de seguridad entre dosis eficaces y tóxicas, siendo crucial para fármacos con ventana terapéutica estrecha y monitoreo riguroso.
Alteraciones en absorción, distribución, metabolismo o eliminación pueden incrementar la concentración plasmática, elevando riesgo de toxicidad si no se ajustan las dosis.
Enfermedades que afectan órganos o sistemas de transporte modifican significativamente la respuesta clínica.
Las reacciones adversas a medicamentos (RAM) se clasifican en:
- Tipo A (dependientes de mecanismo farmacológico y dosis): Exageración de efecto deseado o secundario (ejemplo, hemorragia con anticoagulantes).
- Tipo B (impredecibles y no dosis-dependientes): Incluyen mecanismos inmunológicos, idiosincráticos y estructurales.
Este análisis mecanicista facilita interpretar efectos adversos, falta de respuesta y consecuencias clínicas de interacciones o enfermedades concomitantes, apoyando el uso racional y la personalización terapéutica basada en mecanismos.
💎 Perlas de alto rendimiento
- Integración farmacocinética y farmacodinamia: El mecanismo de fármaco integra farmacocinética y farmacodinamia como dimensiones inseparables.
- Metabolismo presistémico y barreras biológicas: El metabolismo presistémico y barreras biológicas limitan la biodisponibilidad de fármacos administrados oralmente.
- Enzimas citocromo P450: Las enzimas citocromo P450 medían la mayoría de las transformaciones hepáticas; inhibidores o inductores modifican la respuesta clínica.
- Fracción libre de fármaco: La fracción libre de fármaco determina acceso y acción; cambios en proteínas plasmáticas pueden alterar significativamente su actividad.
- Alteración genética en enzimas: La alteración genética en enzimas metabolizadoras afecta la activación de profármacos, modificando el efecto terapéutico esperado.
- Índice terapéutico estrecho: Fármacos con índice terapéutico estrecho requieren monitoreo cuidadoso para evitar toxicidad o subdosificación.
- Insuficiencia renal o hepática: En insuficiencia renal o hepática, la reducción en eliminación prolonga la vida media y exige ajustes dosis/intervalo.
- Monitoreo plasmático: El monitoreo plasmático es útil solo cuando existe una correlación clara entre concentración y efecto; no siempre refleja concentración en sitios específicos.
🧠 Puntos clave
- Composición del mecanismo: El mecanismo de fármaco comprende todas las etapas desde la administración hasta el efecto final, incluyendo absorción, distribución, metabolismo, eliminación y acción en su blanco molecular.
- Especificidad y función: La especificidad y efecto funcional dependen de la estructura del fármaco y su interacción precisa con dianas biológicas.
- Variabilidad en la respuesta: La variabilidad en la respuesta emerge de modificaciones en cualquier fase del mecanismo debido a genética, enfermedad, interacciones o estado fisiológico.
- Índice terapéutico y seguridad: El índice terapéutico define la seguridad: a menor margen, mayor necesidad de monitoreo y ajuste de dosis.
- Reacciones adversas: Las reacciones adversas reflejan excesos o fallas en los mecanismos o procesos inmunológicos asociados.
- Personalización terapéutica: La personalización terapéutica se sustenta en el conocimiento preciso de los mecanismos farmacológicos y su variabilidad.
❓ Preguntas frecuentes
¿Cómo se diferencian farmacocinética y farmacodinamia en el mecanismo de fármaco?
La farmacocinética describe cómo el organismo maneja el fármaco (absorción, distribución, metabolismo, excreción), determinando la concentración disponible; la farmacodinamia explica cómo el fármaco produce efectos específicos al interactuar con sus blancos moleculares.
¿Por qué un mismo fármaco puede ser efectivo en algunos pacientes y tóxico o ineficaz en otros?
Debido a variabilidad genética, enfermedades concomitantes, interacciones medicamentosas y diferencias en adherencia que modulan metabolismo, transporte y sensibilidad del organismo al fármaco.
¿Qué efecto tiene la unión intensa del fármaco a proteínas plasmáticas?
Solo la fracción libre está disponible para difundir a tejidos y ejercer acción; cambios en la unión pueden alterar significativamente la eficacia y el riesgo de toxicidad.
¿Qué es el “efecto de primer paso” y cómo afecta al mecanismo?
Es la reducción de fármaco activo que alcanza la circulación sistémica tras administración oral, por metabolismo intestinal y hepático previo al acceso vascular, limitando la biodisponibilidad y efecto.
¿Por qué algunas reacciones adversas pueden ocurrir a dosis bajas o en la primera exposición?
Muchas reacciones tipo B son independientes de la dosis y mediadas por mecanismos inmunológicos o idiosincráticos, difíciles de predecir con base en el mecanismo principal del fármaco.
¿Cómo influye una enfermedad renal en la respuesta a un fármaco?
La disfunción renal limita la excreción, elevando concentraciones de fármaco o metabolitos y aumentando el riesgo de toxicidad, especialmente para compuestos excretados por el riñón.
¿El sitio de acción determina el efecto clínico del fármaco?
Sí; la localización y expresión de dianas moleculares condicionan la magnitud, especificidad y naturaleza del efecto farmacológico.
¿Monitorear la concentración plasmática garantiza un efecto adecuado?
No siempre; es útil solo cuando existe correlación directa entre concentración plasmática y efecto. En tejidos protegidos por barreras o con transportadores específicos, puede no reflejar la concentración efectiva.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico y conceptual del mecanismo de fármaco presentado.
Nivel 1 – Básico
¿Cuál es el principal enfoque de la farmacocinética dentro del mecanismo de fármaco?
¿Qué papel cumplen los receptores en el mecanismo de fármaco?
¿Dónde ocurre principalmente el metabolismo de un fármaco dentro del organismo?
Nivel 2 – Intermedio
¿Cuál es la relación correcta entre estructuras farmacológicas y su función según el texto?
¿Qué diferencia hay entre farmacocinética y farmacodinamia dentro del mecanismo de fármaco?
Según el artículo, ¿cuál relación correcta resume cómo la variabilidad genética puede alterar la respuesta al fármaco?
Nivel 3 – Avanzado
Si un paciente presenta insuficiencia renal, ¿qué consecuencia directa sobre el mecanismo de fármaco se prevé según el artículo?
¿Qué efecto tendría una mutación que altera la función de un receptor específico en el mecanismo de fármaco?
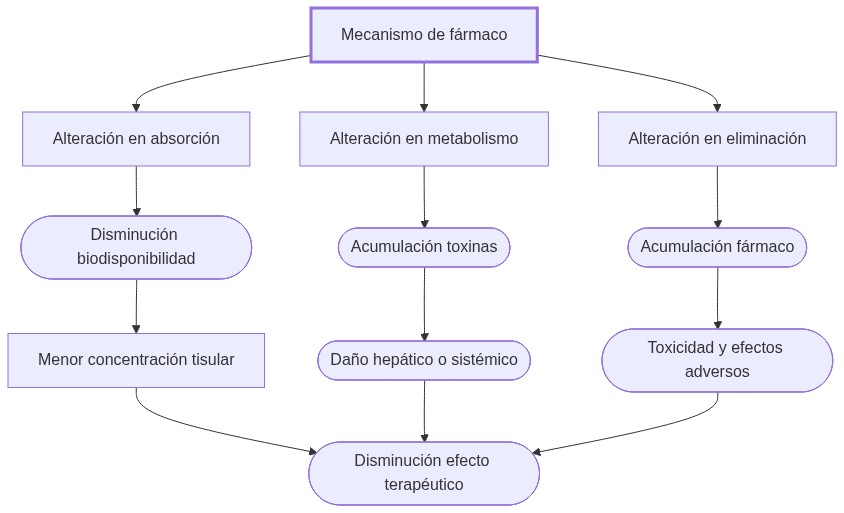
En la secuencia del mecanismo de fármaco, ¿qué consecuencias tiene una disminución en la absorción oral?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.