⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
Los principios de farmacogenómica explican cómo variantes genéticas afectan enzimas, transportadores y receptores modulando la farmacocinética y farmacodinámica, lo que condiciona la respuesta individual a medicamentos y su toxicidad. Estas diferencias moleculares ilustran la base biológica de la variabilidad fenotípica en la eficacia y reacciones adversas farmacológicas.
🧬 Concepto base
La farmacogenómica estudia variantes genéticas que alteran proteínas involucradas en el metabolismo y acción de fármacos, modificando concentración, efecto y seguridad. Afecta genes codificantes para enzimas, transportadores y dianas celulares en tejidos clave como hígado y membranas celulares.
⚙️ Mecanismo clave
Las variantes genéticas causan cambios en la síntesis, estructura o función proteica, afectando la velocidad metabólica y la respuesta celular al fármaco, lo que genera fenotipos de metabolizadores lentos, ultrarrápidos o con reacciones inmunológicas adversas específicas.
🔗 Por qué es importante
Permite predecir y explicar la heterogeneidad en eficacia y toxicidad medicamentosa, optimizando el uso seguro y personalizado de fármacos y apoyando el diseño racional de terapias.
🎯 Puntos que suelen preguntarse en examen
- Definición y impacto de polimorfismos en genes metabolizadores (CYP450)
- Relación entre variantes en transportadores y biodisponibilidad del fármaco
- Efecto de alelos HLA en reacciones inmunomediadas adversas
- Diferencias funcionales entre metabolizadores lentos y ultrarrápidos
- Mecanismos moleculares que modifican la farmacocinética y farmacodinámica
- Importancia del contexto poblacional en la frecuencia de variantes
Palabras clave: principios de farmacogenómica, polimorfismos, metabolizadores, enzimas CYP450, transportadores, dianas farmacológicas, farmacocinética, farmacodinámica
La farmacogenómica investiga cómo las variaciones genéticas individuales modulan la respuesta a los fármacos, mediante alteraciones en rutas farmacocinéticas y farmacodinámicas. Este campo permite comprender el fundamento biológico detrás de la eficacia, toxicidad y variabilidad de los efectos medicamentosos, abriendo el camino hacia la individualización de la terapéutica.
🧠 Idea central
La farmacogenómica analiza cómo los distintos tipos de variantes genéticas —principalmente polimorfismos de un solo nucleótido (SNP), inserciones, deleciones, duplicaciones y variantes en regiones regulatorias— afectan moléculas involucradas en el destino y la acción de los fármacos. Este análisis conecta la secuencia molecular al fenotipo farmacológico, explicando por qué individuos o poblaciones con genotipos diferentes pueden experimentar beneficios terapéuticos, reacciones adversas graves o nula respuesta bajo el mismo tratamiento.
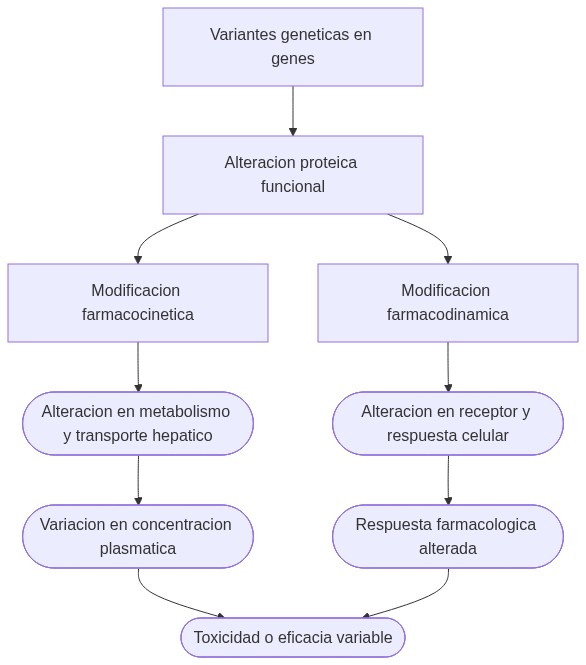
En concreto, la farmacogenómica descompone la modulación genética de dos componentes principales:
- Farmacocinética: Procesos que determinan las concentraciones plasmáticas del fármaco según su absorción, distribución, metabolismo y eliminación, que dependen en gran parte de enzimas y transportadores codificados por genes altamente polimórficos.
- Farmacodinámica: Respuestas celulares y tisulares inducidas por la interacción del fármaco con sus dianas (proteínas receptoras, canales, enzimas); influida por variantes génicas que modifican la estructura, abundancia o función de esos blancos moleculares.
🌍 Contexto y alcance
El ámbito de la farmacogenómica abarca desde el estudio molecular de variantes genéticas en genes humanos hasta la evaluación de su repercusión a nivel poblacional. A diferencia de la farmacogenética, la farmacogenómica incorpora el análisis de múltiples variantes distribuidas a lo largo del genoma y su efecto colectivo sobre la respuesta a los medicamentos en grandes grupos humanos. La variabilidad genética esclarecida por este campo no solo se aplica a la predicción de efectos adversos o eficacias individuales, sino también a estrategias de desarrollo de nuevos fármacos y a la comprensión de la fisiopatología subyacente a ciertas enfermedades.
La frecuencia de variantes relevantes para la farmacogenómica varía considerablemente según el origen ancestral, lo que resulta en riesgos o respuestas diferenciales entre poblaciones. Muchas variantes consideradas críticas en la respuesta farmacológica han sido identificadas mediante estudios en genes candidatos y enfoques de análisis genómico de asociación amplia (genome-wide association studies, GWAS).
Además, el alcance contemporáneo de la farmacogenómica incluye la consideración de variantes en genomas de agentes infecciosos o tumores cuando estos modifican la eficacia o toxicidad de agentes terapéuticos dirigidos.
🧬 Estructuras clave
Las estructuras moleculares implicadas en farmacogenómica pueden agruparse en categorías funcionales, cada una asociada con mecanismos precisos de acción o modulación farmacológica:
-
Enzimas metabolizadoras: Suelen ser miembros de las familias del citocromo P450 (como CYP2D6, CYP2C9, CYP2C19 y CYP3A5), que catalizan reacciones de biotransformación (oxidación, reducción, conjugación) de medicamentos. Estas enzimas residen principalmente en el retículo endoplásmico hepático y en otros tejidos.
Definición: proteínas codificadas por genes con polimorfismos que modifican la velocidad o ruta del metabolismo de fármacos.
Dónde actúan: hepatocitos, citoplasma y membranas celulares.
Qué producen: variaciones en la concentración, semivida y biodisponibilidad del fármaco. -
Transportadores de membrana: Familias como ATP-binding cassette (ABC) (p. ej., ABCB1) y solute carrier organic anion transporter family (SLCO) (p. ej., SLCO1B1) median la entrada o salida de fármacos entre compartimentos celulares y tisulares.
Definición: proteínas transmembranales cuyos polimorfismos alteran la afinidad o el flujo de sustancias.
Dónde actúan: membranas de enterocitos, hepatocitos, túbulos renales, barreras tisulares.
Qué producen: modulación de la cantidad de fármaco que llega a su diana o es eliminado. -
Proteínas receptoras y dianas celulares: Incluyen receptores de superficie o intracelulares, canales, enzimas blanco y proteínas del complejo mayor de histocompatibilidad (como alelos HLA).
Definición: moléculas estructurales con capacidad de unión al fármaco que traducen la señal a una respuesta biológica.
Dónde actúan: neuronas, miocitos, células inmunes y otros tejidos.
Qué producen: iniciación de efectos farmacológicos o desencadenamiento de reacciones inmunomediadas cuando están alteradas.
Las variantes pueden ser SNP sinónimos (modifican el ARN mensajero o el plegamiento proteico sin alterar el codón), SNP no sinónimos (cambian un aminoácido), variantes en regiones promotoras (regulan la cantidad de ARN y proteína generada) o alteraciones en el número de copias (deleciones/duplicaciones).
| Estructura | Función | Ejemplo genético |
|---|---|---|
| Enzimas metabolizadoras (CYP2D6, CYP2C9, CYP2C19, CYP3A5, TPMT) | Oxidan, reducen o inactivan fármacos, regulando su actividad y eliminación | Polimorfismos en CYP2D6 (metabolizadores pobres y ultrarrápidos), variantes inactivas de TPMT |
| Transportadores (ABCB1, SLCO1B1) | Controlan el paso de fármacos entre tejidos (absorción, distribución, excreción) | SLCO1B1*5 aumenta riesgo de miopatía por estatinas; ABCB1 rs1045642 modula estabilidad del ARN mensajero |
| Dianas farmacológicas (receptores β-adrenérgicos, HLA, VKORC1) | Mediadores de la acción directa del fármaco o desencadenantes de reacciones inmunológicas | Polimorfismos en VKORC1 alteran requerimientos de dosis de anticoagulante; HLA-B*57:01 predispone a reacción de hipersensibilidad |
| Enzimas transferasas (NAT2, UGT1A1) | Conjugan fármacos facilitando su eliminación | UGT1A1*28 se asocia a hiperbilirrubinemia e incrementa toxicidad de irinotecán |
⚙️ Funciones y procesos
La farmacogenómica clarifica mecanismos diferenciales de respuesta a los fármacos mediante el análisis secuencial de los siguientes procesos:
-
Modificación genética:
Qué es: presencia de una variante genética (SNP, deleción, duplicación o variante en promotor).
Dónde actúa: locus génico correspondiente en el genoma de cada célula.
Qué produce: codificación de proteínas con función, cantidad o estructura alteradas, como proteínas no funcionales por cambios en el codón.
Caso específico: la duplicación del gen CYP2D6 origina metabolizadores ultrarrápidos; dos alelos no funcionales en CYP2C19 generan metabolizadores lentos.
-
Alteración en síntesis, estructura o función proteica:
Qué es: resultado directo de la variante.
Dónde actúa: ARN mensajero y proteína generados en las células correspondientes.
Qué produce: enzimas, transportadores o receptores con función incrementada, normal, reducida o perdida.
Cómo funciona: las variantes pueden causar proteínas truncadas por codón de parada prematuro, mal plegadas o modificar la transcripción por mutaciones en promotor.
-
Impacto sobre farmacocinética y farmacodinámica:
Farmacocinética:
- Enzimas metabolizadoras alteradas modifican la velocidad de activación o inactivación de fármacos. Ejemplo: CYP2C9 con actividad reducida requiere ajustes en dosis de anticoagulantes.
- Transportadores con mutaciones pueden aumentar concentración intracelular o favorecer eliminación excesiva. Ejemplo: variantes en SLCO1B1 incrementan riesgo de toxicidad muscular con estatinas.
Farmacodinámica:
- Receptores con cambios estructurales presentan diferente afinidad por el fármaco, modificando la respuesta biológica. Polimorfismos en receptor β₂ adrenérgico afectan eficacia de agonistas en asma.
- Variantes HLA pueden desencadenar reacciones inmunomediadas graves como síndrome de Stevens-Johnson.
-
Consecuencia fenotípica:
Qué es: expresión clínica o biológica resultante.
Qué produce: desde alteraciones sutiles en eficacia hasta reacciones potencialmente letales.
Ejemplos notables:
- Portadores de dos alelos inactivos de TPMT presentan toxicidad hematopoyética grave con tiopurinas.
- Metabolizadores ultrarrápidos de CYP2D6 convierten pro-fármacos demasiado rápido, aumentando riesgo de toxicidad aguda.
- Variantes en VKORC1 reducen producción de la proteína diana de warfarina, requiriendo dosis menores para evitar sangrado excesivo.
🔗 Integración funcional
La integración funcional articula los elementos estructurales, vías moleculares y las consecuencias biológicas en la respuesta individual al fármaco. El siguiente ejemplo ilustra este proceso:
-
Variantes de CYP2D6:
Qué es: múltiples SNP, deleciones y duplicaciones afectan este gen que codifica una enzima clave del metabolismo de medicamentos.
Cómo funciona:
- Dos alelos no funcionales generan metabolizadores lentos (PM).
- Duplicaciones de alelos funcionales originan metabolizadores ultrarrápidos (UM), resultando en fenotipos definidos en la población.
Consecuencias:
- PM acumulan fármacos y tienen mayor riesgo de toxicidad.
- UM eliminan rápido y pueden requerir dosis mayores o presentan riesgo si el fármaco es pro-fármaco.
-
Variantes en receptores HLA:
Qué es: alelos del complejo mayor de histocompatibilidad que permiten la presentación de fármacos o metabolitos como neoantígenos.
Qué producen: predisposición a reacciones de hipersensibilidad graves, como síndrome de Stevens-Johnson.
Cómo funciona: solo la combinación de fármaco y alelo de riesgo desencadena activación inmunológica anómala. La frecuencia varía según la ascendencia genética.
-
Modulación colectiva por variantes múltiples:
Qué es: combinación de variantes en transportadores, enzimas y dianas que actúan aditiva o sinérgicamente.
Cómo funciona: por ejemplo, variantes en CYP2C9 y promotor de VKORC1 explican gran parte de la variabilidad en dosis estable de anticoagulante.
🔬 Métodos y evidencias
La identificación y validación de variantes farmacogenómicas requiere múltiples enfoques complementarios:
-
Genotipificación directa:
Identificación de variantes en genes candidatos mediante técnicas como PCR, secuenciación Sanger y secuenciación masiva (NGS). Útil para detectar SNP y variantes en genes relacionados con metabolismo o acción farmacológica.
-
Estudios de asociación genómica amplia (GWAS):
Análisis no dirigido que correlaciona numerosas variantes genéticas con fenotipos de respuesta o toxicidad; identifica variantes que incrementan riesgo poblacional, como alelos HLA asociados a reacciones cutáneas graves.
-
Análisis funcional:
Experimentos en modelos celulares que expresan la variante para cuantificar su impacto en función enzimática o transporte de fármacos, comparando actividad con la variante de referencia.
-
Estudios bioinformáticos:
Herramientas computacionales predicen el efecto de variantes en base a secuencia, estructura o datos poblacionales.
-
Correlación clínica y fenotípica:
Integración de datos farmacocinéticos y farmacodinámicos en individuos con genotipos conocidos para vincular variantes con eficacia, toxicidad o requerimiento de dosis ajustada.
La validez de los hallazgos se fortalece con su repetición en múltiples cohortes y evidencia fisiopatológica coherente.
🩺 Puente clínico
La aplicación clínica de la farmacogenómica se basa en dos ejes principales:
- Predicción y prevención de efectos adversos: Identificando variantes con impacto en farmacocinética o farmacodinámica, se anticipan riesgos de toxicidad o falta de respuesta, integrando esta información en sistemas de apoyo a la prescripción.
- Optimización del desarrollo farmacológico: El conocimiento de distribución de variantes guía el diseño de ensayos clínicos y selección de dianas genéticamente validadas, disminuyendo riesgos de toxicidad inesperada.
Existen dos enfoques para incorporar la información farmacogenómica en la práctica:
-
Testing en el punto de atención:
Prueba genética solicitada al momento de prescribir para obtener resultado inmediato que guíe la decisión.
-
Testing preemptivo:
Perfil farmacogenético determinado antes de la indicación, disponible en la historia clínica electrónica para futuras prescripciones.
El beneficio clínico depende de:
- El tamaño del efecto de la variante genética sobre la respuesta farmacológica.
- Robustez de la evidencia que vincula genotipo con fenotipo.
- Disponibilidad de terapias alternativas y estrategias de monitorización.
Ejemplos destacados incluyen la reducción de efectos adversos graves evitando fármacos en portadores de alelos HLA de riesgo y personalización de dosis para medicamentos con margen terapéutico estrecho.
💎 Perlas de alto rendimiento
- Distribución multimodal: Los fenotipos de respuesta a fármacos suelen mostrar distribución multimodal debida a variantes específicas de gran efecto en genes claves.
- Polimorfismos en metabolizadores: Polimorfismos en genes metabolizadores influyen directamente en velocidad de activación o eliminación de múltiples fármacos.
- Variaciones en número de copias: Variaciones en número de copias génicas pueden generar fenotipos extremos, como metabolizadores ultrarrápidos.
- Variantes en transportadores: Variantes en transportadores modifican biodisponibilidad y riesgo de toxicidad al alterar flujo celular de fármacos.
- Alelos HLA específicos: Alelos HLA específicos determinan susceptibilidad genética a reacciones inmunomediadas, con prevalencias variables entre poblaciones.
- Variabilidad en dosis: La farmacogenómica explica una parte importante de la variabilidad en requerimientos de dosis mediante análisis de variantes combinadas.
- Variantes en regiones no codificantes: Variantes en regiones no codificantes afectan expresión proteica y fenotipos sin alterar secuencia aminoacídica.
- Contexto ancestral: Interpretar farmacogenómica requiere considerar el contexto ancestral por variación en frecuencias alélicas.
🧠 Puntos clave
- Variantes genéticas: Las variantes genéticas influyen en metabolismo y acción farmacológica con consecuencias funcionales relevantes.
- Variabilidad poblacional: Frecuencia e impacto de esas variantes varían entre poblaciones, condicionando la respuesta individual a medicamentos.
- Principales estructuras moduladas: Enzimas metabolizadoras, transportadores y receptores son principalmente modulados por farmacogenómica.
- Integración de datos: Integrar datos genéticos y funcionales explica gran parte de la variabilidad en eficacia y toxicidad de fármacos.
- Herramientas genómicas: Herramientas genómicas modernas apoyan predicción de riesgos y desarrollo racional de terapias con dianas funcionalmente validadas.
- Modalidades de análisis: Análisis farmacogenético puede ser puntual o preemptivo, según contexto clínico y recursos disponibles.
❓ Preguntas frecuentes
¿Cómo una variante genética puede alterar la función de una enzima metabolizadora de fármacos?
Una variante puede modificar aminoácidos críticos, generando enzimas con actividad disminuida, ausente o aumentada. La pérdida de función aumenta la concentración del fármaco y riesgo de toxicidad, mientras que duplicaciones pueden causar eliminación rápida y respuesta clínica subóptima.
¿Por qué algunas reacciones adversas sólo ocurren en ciertos grupos poblacionales?
La frecuencia de variantes de riesgo, como alelos HLA o polimorfismos en transportadores, varía según el origen ancestral, lo que modula la probabilidad de respuestas inmunológicas adversas en diferentes poblaciones.
¿Qué diferencia a un metabolizador lento de un metabolizador ultrarrápido para un mismo fármaco?
El metabolizador lento posee variantes que reducen o eliminan la actividad enzimática, acumulando fármaco; el ultrarrápido elimina o activa el fármaco rápidamente, requiriendo a veces ajustes de dosis.
¿Cómo se demuestra que una variante genética es la causa de una respuesta atípica a un fármaco?
Se requiere correlacionar la variante con alteraciones funcionales en la proteína, demostrar el efecto fenotípico en modelos celulares o animales y confirmar la asociación en estudios clínicos y poblacionales robustos.
¿Cuál es la relevancia de analizar variantes en transportadores de membrana?
Los transportadores determinan la cantidad de fármaco que alcanza la diana o es eliminado; variantes pueden modificar la exposición tisular, afectando eficacia y riesgo de toxicidad en órganos específicos.
¿Por qué la farmacogenómica considera variantes en genes del sistema inmunológico?
Algunas reacciones adversas graves se deben al reconocimiento inmunológico anómalo de fármacos o metabolitos, proceso dependiente de variantes en genes HLA que afectan la presentación antigénica y activación inmune.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión biológica de conceptos clave de farmacogenómica presentados en el artículo.
Nivel 1 – Básico
¿Qué define la farmacodinámica según el artículo?
¿Dónde actúan principalmente las enzimas metabolizadoras mencionadas en el texto?
¿Cuál es la función principal de los transportadores de membrana en farmacogenómica?
Nivel 2 – Intermedio
¿Cuál es la relación correcta según el artículo entre variantes en CYP2D6 y fenotipos de metabolizadores?
Según el texto, ¿cómo afecta una variante en el gen SLCO1B1 al riesgo asociado a ciertos fármacos?
¿Cuál de las siguientes afirmaciones sobre variantes en genes HLA es correcta según el artículo?
Nivel 3 – Avanzado
Según la secuencia mecanística descrita, ¿qué consecuencia fenotípica tiene un portador de dos alelos inactivos de TPMT al recibir tiopurinas?
¿Cómo se explica la variabilidad en requerimientos de dosis estable de anticoagulantes según la integración funcional del artículo?
Según los pasos del proceso farmacogenómico, ¿qué ocurre después de la presencia de una variante genética en un locus génico?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.