⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
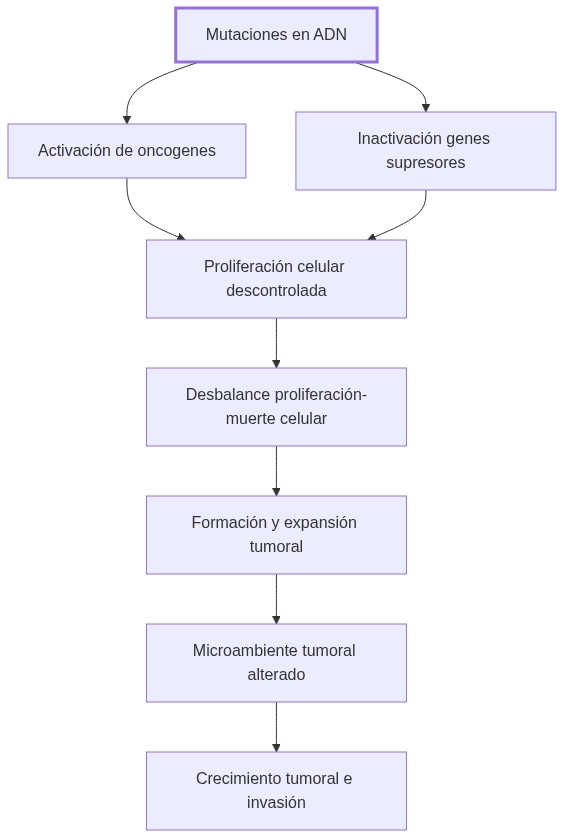
El mecanismo de cáncer consiste en la acumulación secuencial de mutaciones somáticas que alteran oncogenes y genes supresores, generando proliferación celular descontrolada y escape a mecanismos de control. Este proceso multietápico produce la transformación de células normales en malignas con capacidad invasiva y heterogeneidad genética.
🧬 Concepto base
El cáncer es una enfermedad genética causada por mutaciones que otorgan ventajas proliferativas a células clonales. Se caracteriza por la desregulación del ciclo celular, escape a apoptosis y alteraciones en el ADN, dando lugar a la formación de tumores.
⚙️ Mecanismo clave
Mutaciones activan oncogenes o inactivan genes supresores, desbalanceando proliferación y muerte celular. Este descontrol favorece expansión clonal, inestabilidad genómica y evasión inmunitaria, conduciendo a la progresión tumoral.
🔗 Por qué es importante
Explica la base molecular de la tumorigenesis, la heterogeneidad tumoral y el impacto de factores genéticos y ambientales en la formación y agresividad del cáncer.
🎯 Puntos que suelen preguntarse en examen
- ¿Qué roles tienen oncogenes y genes supresores en el cáncer?
- ¿Por qué la inactivación de ambos alelos es necesaria en genes supresores?
- ¿Cómo contribuye la acumulación secuencial de mutaciones a la tumorigenesis?
- ¿Qué es la inestabilidad cromosómica y su efecto en el cáncer?
- ¿Cuál es la importancia del origen clonal en los tumores?
- ¿Cómo influye la predisposición germinal en la aparición del cáncer?
Palabras clave: mecanismo de cáncer, oncogenes, genes supresores de tumores, acumulación mutacional, inestabilidad genómica, proliferación celular, apoptosis, heterogeneidad tumoral
El mecanismo de cáncer describe cómo alteraciones somáticas en el ADN de células normales conducen a una proliferación descontrolada, generando una ventaja selectiva en clones celulares y la eventual adquisición de un fenotipo maligno responsable de la tumorigenesis.
Comprender estos procesos, que involucran diversas escalas biológicas desde el gen hasta el organismo, es esencial para entender la base molecular de la neoplasia y situar la enfermedad en el contexto de la biología celular, la genética y la fisiopatología.
🧠 Idea central
El cáncer es una enfermedad que surge principalmente por alteraciones somáticas en el ADN de una única célula, otorgándole a esta y a sus descendientes una ventaja proliferativa.
Estas alteraciones incluyen mutaciones en genes que regulan el destino y la supervivencia celular. Existen dos grandes grupos de genes implicados: los oncogenes (genes que, al activarse por mutación, promueven el crecimiento celular) y los genes supresores de tumores (genes que normalmente restringen la proliferación y cuya inactivación elimina estos controles).
La progresión tumoral no depende de un solo cambio, sino de la acumulación secuencial de varias mutaciones clave.
Este proceso, similar a una microevolución darwiniana, conduce inicialmente a proliferación celular desorganizada y luego a la adquisición de capacidades invasivas características del cáncer maligno.
Generalmente, la transformación de una célula normal a maligna requiere al menos tres mutaciones en genes impulsores (“driver genes”).
🌍 Contexto y alcance
El mecanismo de cáncer actúa en varios niveles de organización biológica:
- Nivel molecular: El ADN sufre mutaciones puntuales, amplificaciones, deleciones y reordenamientos cromosómicos. En algunos casos, la inestabilidad genética facilita la acumulación acelerada de nuevas alteraciones.
- Nivel celular: Cambios en la maquinaria intracelular afectan la detección de daño, la regulación del ciclo celular, la apoptosis y el mantenimiento genómico. Las células con ventajas proliferativas forman clones que desplazan a las células normales.
- Nivel tisular y orgánico: La expansión clonal genera masas celulares (tumores), que pueden invadir y metastatizar según el tipo y número de mutaciones acumuladas.
- Nivel poblacional: Factores como la exposición a carcinógenos (tabaco, radiación), errores de replicación y predisposición genética afectan la frecuencia y tipo de mutaciones en distintos grupos humanos, relacionando la epidemiología con la biología molecular.
El estudio de estas interacciones permite distinguir neoplasias benignas, que requieren menos eventos genéticos y carecen de invasividad, de tumores malignos que superan los controles fisiológicos y alteran la homeostasis sistémica.
🧬 Estructuras clave
-
ADN (ácido desoxirribonucleico):
¿Qué es?: Material genético celular formado por secuencias de nucleótidos.
¿Dónde actúa?: Núcleo celular.
¿Qué permite?: Conserva y transmite la información genética para el control celular.
¿Cómo funciona?: Una replicación fiel es clave para la herencia; errores espontáneos o inducidos pueden originar mutaciones oncogénicas.
-
Protooncogenes:
¿Qué son?: Genes normales que regulan proliferación y diferenciación cell.
¿Dónde actúan?: Expresados en diversos tipos celulares.
¿Qué producen?: Promueven crecimiento celular bajo control fisiológico.
¿Cómo funcionan?: Codifican proteínas señalizadoras y factores de transcripción. Mutaciones activadoras en una sola copia los convierten en oncogenes con función desregulada.
-
Genes supresores de tumores:
¿Qué son?: Genes que limitan la proliferación y mantienen la homeostasis tisular.
¿Dónde actúan?: Presentes en la mayoría de tejidos.
¿Qué producen?: Codifican proteínas que frenan el ciclo celular, promueven reparación del ADN o inducen apoptosis.
¿Cómo funcionan?: Requieren la inactivación de ambas copias génicas para perder su función supresora.
-
Ciclo celular y puntos de control:
¿Qué son?: Secuencia de fases que culminan en división celular, regulada para asegurar fidelidad genómica.
¿Dónde actúan?: Células en proliferación.
¿Qué producen?: Evitan replicación o mitosis de células dañadas.
¿Cómo funcionan?: Proteínas como p53 y retinoblastoma (Rb) detienen el ciclo ante daño genético. Su pérdida favorece inestabilidad cromosómica y aneuploidía.
-
Apoptosis:
¿Qué es?: Muerte celular programada fisiológica.
¿Dónde actúa?: Células con daño genotóxico severo.
¿Qué produce?: Elimina células anómalas para proteger tejidos.
¿Cómo funciona?: Cascadas enzimáticas fragmentan la célula. Alteraciones favorecen supervivencia celular mutada.
-
Telómeros y telomerasa:
¿Qué son?: Secuencias repetitivas terminales y enzima que las mantiene.
¿Dónde actúan?: Células normales y tumorales.
¿Qué producen?: Previenen acortamiento límite que restringe replicación.
¿Cómo funcionan?: Activación aberrante en tumores permite replicación ilimitada, contribuyendo a la inmortalidad celular.
-
Inestabilidad genómica y cromosómica:
¿Qué es?: Mayor propensión a mutaciones y alteraciones cromosómicas.
¿Dónde actúa?: Tumores sólidos y síndromes hereditarios.
¿Qué produce?: Acelera progresión tumoral y aparición de subclonas.
¿Cómo funciona?: Defectos en reparación del ADN o puntos de control provocan fenotipo mutador.
-
Microambiente tumoral:
¿Qué es?: Células normales, matriz extracelular y moléculas cerca del tumor.
¿Dónde actúa?: Entorno tisular inmediato al tumor.
¿Qué produce?: Modula angiogénesis, invasión y respuesta inmune.
¿Cómo funciona?: Señales y moléculas de adhesión modifican comportamiento tumoral.
⚙️ Funciones y procesos
El mecanismo de cáncer involucra diversos procesos biológicos dependientes de cambios moleculares:
-
Inducción de mutaciones genéticas:
¿Qué es?: Cambios en la secuencia de ADN por errores replicativos, carcinógenos o defectos de reparación.
¿Cómo funciona?: Afectan genes reguladores del crecimiento y muerte celular, activando oncogenes o inactivando genes supresores.
-
Acumulación secuencial de mutaciones – multietapicidad:
¿Qué es?: Serie progresiva de mutaciones no simultáneas durante la vida.
¿Cómo funciona?: Cada mutación otorga ventaja proliferativa, expandiendo clones y aumentando probabilidad de mutaciones adicionales.
Consecuencia: Se requieren usualmente tres mutaciones “driver” para tumores sólidos; menos para tumores líquidos o pediátricos.
-
Activación de oncogenes:
¿Qué es?: Mutación puntual, amplificación o reordenamiento convierte un protooncogén en oncogén.
¿Cómo funciona?: Ejemplo: mutaciones en codones específicos de KRAS activan RAS constitutivamente, promoviendo proliferación independiente.
Consecuencia: Una sola alteración puede hiperactivar la función génica.
-
Inactivación de genes supresores de tumores:
¿Qué es?: Pérdida funcional de ambos alelos de genes como TP53, RB1 o APC.
¿Cómo funciona?: Mutaciones, deleciones o epigenéticas silencias eliminan sus frenos regulatorios.
Consecuencia: Células proliferan aún con daño genómico.
-
Desbalance entre proliferación y muerte celular:
¿Qué es?: Más células nacen que mueren.
¿Cómo funciona?: Mutaciones rompen el equilibrio que mantiene el número celular estable.
Consecuencia: Tumorigenesis ocurre con un pequeño desbalance acumulado en décadas.
-
Formación y expansión clonal:
¿Qué es?: Origen a partir de una célula mutada progenitora.
¿Cómo funciona?: Descendientes comparten mutaciones fundadoras, adquiriendo alteraciones adicionales.
Consecuencia: Permite identificación molecular y perfilado genómico del tumor.
-
Genómica tumoral y heterogeneidad:
¿Qué es?: Diversidad genética entre células de un tumor y entre pacientes.
¿Cómo funciona?: Mutaciones driver fundadoras son universales; pasajeras contribuyen a variabilidad.
Consecuencia: Influye en evolución tumoral y resistencia.
-
Inestabilidad cromosómica y aneuploidía:
¿Qué es?: Alteración en número y estructura cromosómica.
¿Cómo funciona?: Defectos en puntos de control, como regulación por p53 y mitosis, causan segregación errónea.
Consecuencia: Favorece pérdida de supresores y ganancia de oncogenes.
-
Contribución del microambiente y evasión inmunitaria:
¿Qué es?: Interacción entre células tumorales e inmunitarias.
¿Cómo funciona?: Tumores expresan neoantígenos pero bloquean activación inmunitaria local mediante mecanismos de puntos de control.
Consecuencia: Permite crecimiento sin eliminación inmune.
-
Predisposición germinal y síndromes familiares:
¿Qué es?: Mutaciones heredadas en genes supresores o raramente protooncogenes.
¿Cómo funciona?: Portadores requieren solo una mutación somática adicional para iniciar tumores (“doble golpe”).
Consecuencia: Aparición temprana y frecuente de cáncer en familias.
🔗 Integración funcional
Relacionar estructuras y funciones alteradas explica el inicio y progreso tumoral desde una perspectiva sistémica:
- Secuencia causal: Mutación activa oncogén que impulsa proliferación autónoma; inactivación de gen supresor elimina capacidad de control y apoptosis.
- Desregulación progresiva: Alteraciones sucesivas eliminan barreras fisiológicas claves: control del ciclo, detección de daño, limitación replicativa y muerte celular.
- Contexto tisular y sistémico: Microambiente favorece angiogénesis, evasión inmune y remodelado tisular que facilitan invasión y crecimiento tumoral.
- Evolución clonal: Proceso dinámico con expansión y fijación de nuevas mutaciones, generando heterogeneidad subclonal en tumores avanzados.
El mecanismo de cáncer describe una cascada multietápica donde la interacción de eventos genéticos, celulares, microambientales y hereditarios determina la progresión desde la célula normal a neoplasia maligna.
🔬 Métodos y evidencias
El estudio del mecanismo tumoral se basa en diversas metodologías:
-
Secuenciación del ADN y perfilamiento genómico:
Permite detectar mutaciones puntuales, translocaciones, amplificaciones y deleciones relevantes para el cáncer. El análisis genómico integral identifica mutaciones driver y pasajeras.
-
Estudios de clonogenicidad celular:
Evalúan la expansión clonal desde una célula mutada y la heterogeneidad resultante, confirmando el origen monoclonal de la mayoría de tumores.
-
Análisis citogenéticos y FISH:
Detectan aneuploidía y reordenamientos cromosómicos recurrentes, facilitando la correlación de alteraciones estructurales con mecanismos moleculares.
-
Modelos in vitro e in vivo:
Sistemas celulares y animales con mutaciones definidas han confirmado las secuencias causales y efecto de mutaciones combinadas.
-
Bases de datos genéticos y consorcios internacionales:
Proyectos como The Cancer Genome Atlas sistematizan información sobre mutaciones, vías alteradas y heterogeneidad tumoral en pacientes.
La convergencia de estas evidencias respalda el modelo multietápico y clonal del cáncer, aplicable a tumores esporádicos y hereditarios.
🩺 Puente clínico
El conocimiento del mecanismo molecular y celular del cáncer fundamenta la interpretación clínica en varios niveles:
- Diferencia tumores benignos y malignos según número y tipo de alteraciones genéticas y capacidad invasiva.
- Relaciona cáncer familiar con mutaciones germinales, explicando aparición precoz y multifocal en síndromes de predisposición.
- Justifica diversidad fenotípica y biológica mediante heterogeneidad genética entre pacientes.
- Explica el aumento del riesgo con la edad por acumulación progresiva de mutaciones (“multi-hit”).
- Fundamenta bases para estratificación molecular y la medicina de precisión, sin abordar terapéutica específica.
Así, el mecanismo de cáncer conecta la biología molecular con la complejidad clínica y evolutiva de las neoplasias.
💎 Perlas de alto rendimiento
- Concepto clave: enfermedad genética. El cáncer es esencialmente una enfermedad genética originada por mutaciones somáticas acumuladas.
- Concepto clave: activación e inactivación génica. Los oncogenes se activan con una sola mutación, mientras los genes supresores requieren inactivación bialélica.
- Concepto clave: mutaciones acumuladas. La transformación maligna de tumores sólidos generalmente implica al menos tres mutaciones driver acumuladas.
- Concepto clave: origen clonal. El origen clonal es un rasgo distintivo que diferencia neoplasias de procesos hiperplásicos.
- Concepto clave: inestabilidad cromosómica. La inestabilidad cromosómica contribuye a la aneuploidía y acelera el desarrollo tumoral.
- Concepto clave: microambiente tumoral. El microambiente tumoral modula la angiogénesis y evasión inmune, influyendo en el comportamiento neoplásico.
- Concepto clave: predisposición germinal. Mutaciones germinales predisponen al cáncer mediante un “doble golpe” somático adicional.
- Concepto clave: heterogeneidad genética. La heterogeneidad genética es clave en la resistencia tumoral y evolución clínica.
🧠 Puntos clave
- Idea central: acumulación de mutaciones. El mecanismo de cáncer se basa en la sucesiva acumulación de mutaciones genéticas que generan crecimiento descontrolado.
- Idea central: alteraciones combinadas. La transformación maligna requiere la alteración combinada de oncogenes y genes supresores de tumores.
- Idea central: equilibrio celular alterado. El equilibrio entre proliferación y muerte celular es alterado, favoreciendo la expansión clonal.
- Idea central: roles opuestos complementarios. Protooncogenes y genes supresores tienen roles opuestos pero complementarios en la tumorigenesis.
- Idea central: inestabilidad genética aceleradora. La inestabilidad genética y cromosómica acelera la evolución tumoral, especialmente en síndromes hereditarios.
- Idea central: participación del microambiente. El microambiente y la respuesta inmune participan activamente en la regulación y evasión tumoral.
❓ Preguntas frecuentes
¿Cómo se activa un oncogén y en qué etapa del mecanismo de cáncer ocurre?
Un oncogén se activa por mutación puntual, amplificación o reordenamiento cromosómico, habitualmente en etapas iniciales de la tumorigenesis, proporcionando señales proliferativas independientes.
¿Por qué es necesario inactivar ambos alelos de un gen supresor de tumores para perder su función?
Porque en células diploides la función supresora puede mantenerse con un alelo intacto; sólo la inactivación bialélica elimina completamente su acción reguladora.
¿Cómo contribuye la inestabilidad cromosómica a la progresión tumoral?
Facilita ganancias, pérdidas y reorganizaciones cromosómicas que promueven la pérdida de genes supresores y la duplicación de oncogenes, acelerando la acumulación de mutaciones driver.
¿Qué distingue a una mutación driver de una pasajera en el contexto tumoral?
Las mutaciones driver confieren ventaja selectiva y promueven la tumorigénesis; las pasajeras no aportan beneficio proliferativo y coexisten sin efecto funcional.
¿Cómo influye la herencia germinal en la aparición del cáncer?
Una mutación germinal predispone al cáncer al otorgar una ventaja inicial; sólo se requiere una segunda mutación somática para iniciar la neoplasia, acelerando y aumentando la frecuencia de aparición.
¿Por qué los tumores sólidos suelen requerir al menos tres mutaciones driver para su formación?
Por la necesidad de alterar múltiples rutas independientes vinculadas a proliferación, apoptosis y reparación, la transformación maligna resulta de mutaciones acumuladas que afectan esos procesos.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico del artículo sobre el mecanismo de cáncer.
Nivel 1 – Básico
¿Qué tipo de alteraciones en las células normales conducen a la tumorigenesis según el artículo?
¿Dónde se encuentra el ADN en la célula según el texto?
¿Qué función tiene la proteína p53 en el ciclo celular según el artículo?
Nivel 2 – Intermedio
¿Cuál de las siguientes relaciones estructura-función es correcta según el artículo?
¿Cómo se describe la progresión tumoral en relación con las mutaciones acumuladas?
Según el artículo, ¿Qué diferencia al microambiente tumoral en la regulación tumoral?
Nivel 3 – Avanzado
Según la integración funcional descrita, ¿qué ocurre si se inactiva un gen supresor de tumores en una célula con un oncogén activo?
¿Cuál es la consecuencia funcional de la inestabilidad cromosómica según el artículo?
En un individuo con predisposición germinal, ¿qué implica el “doble golpe” somático para iniciar el cáncer según el texto?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.