⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
El tratamiento del cáncer requiere comprender alteraciones celulares y moleculares que rompen la homeostasis, permitiendo proliferación incontrolada, evasión de apoptosis y modificación del microambiente. Estas disfunciones integradas favorecen la persistencia y diseminación tumoral mediante mecanismos de comunicación celular alterada y escape inmunológico.
🧬 Concepto base
El cáncer es una patología caracterizada por la proliferación desregulada de células que modifican estructuras como el núcleo, membrana plasmática y organelos para evadir controles celulares y resistir muerte programada.
⚙️ Mecanismo clave
Mutaciones en genes supresores y protooncogenes alteran el ciclo celular y apoptosis, mientras que la secreción de factores como VEGF induce angiogénesis y la degradación de matriz extracelular permite invasión y metastatización.
🔗 Por qué es importante
Estas alteraciones facilitan el crecimiento tumoral autónomo y su resistencia a la eliminación inmunitaria, asegurando persistencia y progresión dentro del huésped.
🎯 Puntos que suelen preguntarse en examen
- Mutaciones que permiten proliferación celular descontrolada.
- Mecanismos de evasión de apoptosis en células tumorales.
- Rol de la angiogénesis en suministro tumoral de nutrientes.
- Procesos de invasión y pérdida de adhesión intercelular.
- Modificación del microambiente para escape inmunitario.
- Interacción entre núcleo y membrana plasmática en señalización aberrante.
Palabras clave: tratamiento del cáncer, ciclo celular, apoptosis, angiogénesis, microambiente tumoral, metástasis, mutaciones genéticas, evasión inmunológica
El estudio del tratamiento del cáncer requiere entender en detalle los procesos celulares y moleculares que subyacen a la transformación maligna. Para analizar el comportamiento patológico de las células cancerosas y su persistencia en el huésped, es esencial comprender cómo diversas interacciones moleculares y estructurales a nivel tisular y celular alteran la homeostasis normal, permitiendo el desarrollo, mantenimiento y expansión de la enfermedad.
El análisis debe centrarse en cómo las alteraciones en la comunicación celular, la modulación de la respuesta inmunológica y los cambios en el microambiente condicionan los procesos biológicos implicados en la patogénesis tumoral.
🧠 Idea central
Comprender los mecanismos biológicos que determinan el cáncer es fundamental para interpretar cómo las células tumorales logran expandirse, evadir los sistemas de control fisiológico y establecerse en el organismo.
Esto ocurre gracias a interacciones reguladas entre estructuras celulares—entre ellas el núcleo, la membrana plasmática y organelos—y señales moleculares que coordinan la función y supervivencia celular.
En el cáncer, se observa una alteración profunda de estos procesos: las células adquieren capacidad para proliferar sin control, resistir señales de muerte programada (apoptosis) y comunicarse con su entorno para colonizar nichos específicos, escapando a la respuesta defensiva del huésped.
Estos mecanismos modifican la fisiopatología tisular, facilitando el desarrollo, progresión y daño asociado a la enfermedad.
🌍 Contexto y alcance
La base molecular y celular del cáncer se estudia a partir de las interacciones entre las células tumorales y su microambiente.
Esto implica analizar modificaciones en vías de comunicación celular, expresión génica y organización tisular tridimensional.
En particular:
- Interacción célula-célula: La comunicación mediante uniones celulares y señales paracrinas se altera, facilitando que las células tumorales evadan mecanismos regulatorios normales.
- Microambiente tisular: El entorno cercano a la célula tumoral, formado por otros tipos celulares, matriz extracelular y señales solubles, sufre cambios que favorecen la supervivencia tumoral y la invasión de tejidos vecinos.
Estas alteraciones ocurren desde la escala molecular hasta la orgánica, mostrando cómo disfunciones celulares se traducen en manifestaciones complejas.
La capacidad tumoral para establecerse en nichos tisulares depende de su adaptación y manipulación del metabolismo propio y la respuesta inmunitaria del huésped.
🧬 Estructuras clave
Las estructuras biológicas que intervienen en la fisiopatología del cáncer comprenden elementos subcelulares y tisulares relevantes para la interacción molecular en la tumorogénesis:
| Estructura | Definición y localización | Implicancia en cáncer (Mecanismo funcional) |
|---|---|---|
| Núcleo celular | Organelo central de células eucariotas, contiene ADN y proteínas asociadas. |
|
| Membrana plasmática | Delimita la célula, formada por bicapa lipídica y proteínas de superficie. |
|
| Organelos (mitocondria, retículo endoplasmático) | Regulan metabolismo energético (mitocondria) y síntesis/procesamiento proteico (retículo endoplasmático). |
|
| Moléculas señalizadoras | Factores solubles (citoquinas, factores de crecimiento) y segundos mensajeros presentes intracelular y extracelularmente. |
|
La función de cada estructura depende de su localización, composición y dinámica de interacción intracelular y con tejido circundante.
⚙️ Funciones y procesos
El cáncer surge por acumulación progresiva de alteraciones en funciones celulares que generan un comportamiento patológico sostenido.
Los procesos clave incluyen:
-
Desregulación del ciclo celular
- Definición: El ciclo celular comprende fases G1, S, G2 y M, reguladas por quinasas dependientes de ciclinas.
- Mecanismo: Mutaciones en protooncogenes (ejemplo: Ras, Myc) y genes supresores (ejemplo: p53, Rb) interrumpen puntos de control, permitiendo replicación incontrolada.
- Consecuencia: Aumento de proliferación y riesgo de variabilidad genética tumoral.
-
Evasión de la apoptosis
- Definición: Muerte celular programada mediada por caspasas y vías mitocondriales.
- Mecanismo: Sobreexpresión de proteínas antiapoptóticas (ejemplo: Bcl-2) bloquea activación de caspasas, impidiendo eliminación celular.
- Consecuencia: Acumulación de células anómalas y heterogeneidad tumoral.
-
Inducción de angiogénesis
- Definición: Formación de nuevos vasos sanguíneos en respuesta a demandas nutricionales tumorales.
- Mecanismo: Secreción de VEGF y otros factores estimula migración y proliferación endotelial.
- Consecuencia: Suministro de nutrientes y oxígeno para crecimiento tumoral y acceso vascular para diseminación.
-
Invasión tisular y metastatización
- Definición: Células tumorales atraviesan barreras tisulares y colonizan sitios distantes.
- Mecanismo: Disminuye adhesión (ejemplo: E-cadherina), secreción de enzimas degradantes (metaloproteinasas) y migración celular.
- Consecuencia: Formación de metástasis y diseminación sistémica.
-
Escape a la respuesta inmunológica
- Definición: Elusión de reconocimiento y destrucción por células inmunitarias.
- Mecanismo: Modificación antigénica y secreción de moléculas inmunomoduladoras que inhiben linfocitos y células presentadoras de antígenos.
- Consecuencia: Persistencia tumoral y progresión de la enfermedad.
🔗 Integración funcional
La comprensión de la fisiopatología tumoral requiere analizar cómo las alteraciones estructurales y funcionales se integran y potencian en el tiempo, otorgando adaptabilidad y persistencia al cáncer frente a controles homeostáticos.
-
Relación núcleo-membrana plasmática:
- Mutaciones nucleares pueden modificar expresión y afinidad de receptores de membrana, amplificando la respuesta a factores de crecimiento y señalización proliferativa.
-
Interacción organelos-moléculas señalizadoras:
- Alteraciones metabólicas en mitocondrias y retículo endoplasmático afectan producción de factores angiogénicos e inmunomoduladores, favoreciendo supervivencia tumoral.
-
Microambiente y evasión inmune:
- El microambiente tumoral crea un nicho protectivo mediante secreción de citoquinas y reclutamiento o inhibición de células inmunes.
-
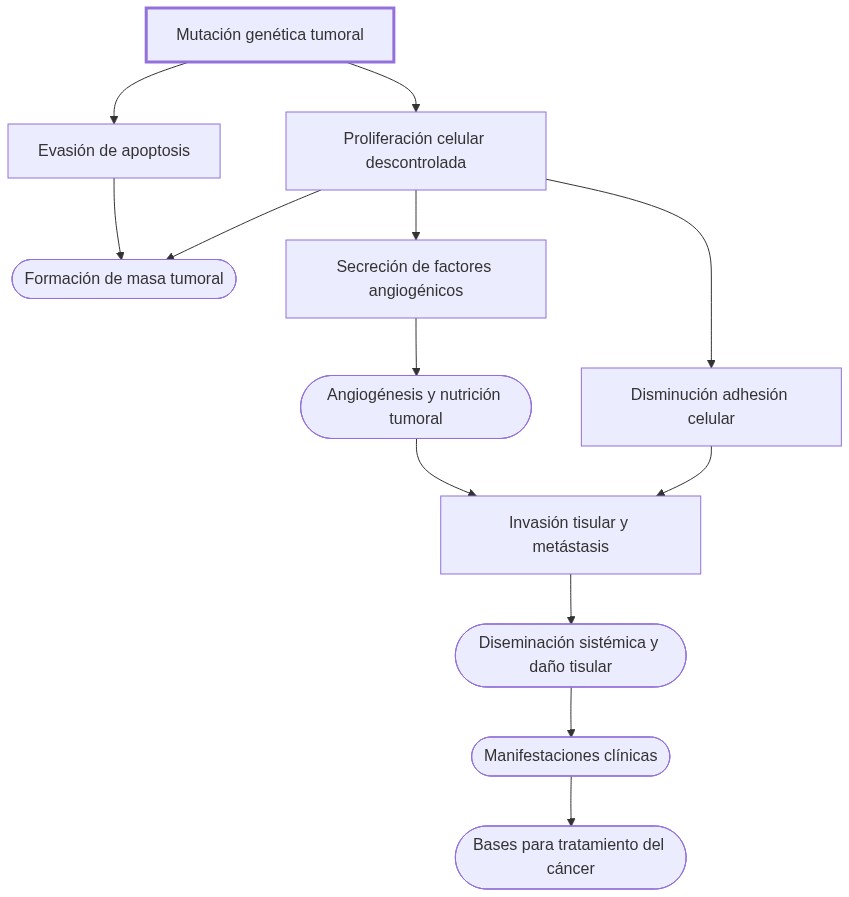
Secuencia progresiva de alteraciones:
- Mutación genética con proliferación descontrolada.
- Evasión de apoptosis.
- Activación de angiogénesis y pérdida de adhesión para invasión.
- Manipulación del microambiente e inhibición inmunológica para persistencia.
Así, la biología tumoral es una red dinámica que determina la heterogeneidad y capacidad de persistencia del cáncer.
🔬 Métodos y evidencias
La elucidación de procesos moleculares y celulares en cáncer utiliza herramientas que permiten visualizar, cuantificar y caracterizar alteraciones propias de células tumorales:
-
Microscopía óptica y electrónica:
- Permite observar morfología y ultraestructura celular, identificando anomalías nucleares, variaciones en organelos y cambios en membranas.
-
Métodos moleculares:
- Diagnóstico y análisis de mutaciones y expresión génica mediante PCR, hibridación y secuenciación.
-
Ensayos funcionales:
- Evaluación de proliferación, apoptosis e invasión celular in vitro bajo condiciones controladas.
-
Análisis del microambiente:
- Detección de expresión molecular y composición celular mediante citometría de flujo e inmunohistoquímica, caracterizando nichos tumorales.
La combinación de estos métodos permite caracterizar la biología tumoral multidimensionalmente, reflejando su heterogeneidad e interacción con el huésped.
🩺 Puente clínico
El conocimiento de las bases celulares y moleculares clarifica cómo las alteraciones biológicas desencadenan manifestaciones fisiopatológicas a nivel orgánico.
La proliferación tumoral genera masas celulares que comprimen o invaden tejidos normales, mientras la inflamación asociada produce daño y disfunción.
La persistencia tumoral y la evasión inmunitaria, junto con la inducción de angiogénesis, explican la progresión y síntomas relacionados con invasión local y diseminación.
Por ello, el análisis fisiopatológico debe vincular evidencias moleculares con fenómenos clínicos, interpretando la progresión tumoral como resultado de la integración celular, molecular y de la respuesta del huésped.
💎 Perlas de alto rendimiento
- Transformación tumoral: La transformación tumoral requiere mutaciones acumulativas en genes reguladores del ciclo celular y apoptosis.
- Pérdida de puntos de control: La pérdida de puntos de control permite proliferación incluso con daño genético.
- Resistencia a apoptosis: La resistencia a apoptosis se asocia con proteínas antiapoptóticas y alteraciones mitocondriales.
- Angiogénesis tumoral: La angiogénesis depende de factores secretados por células malignas para nutrir el tumor.
- Invasión tumoral: La invasión tumoral implica reducción de adhesión celular y secreción de metaloproteinasas.
- Microambiente tumoral: El microambiente tumoral interactúa con células inmunes para favorecer la evasión y supervivencia.
- Patogénesis tumoral: La patogénesis tumoral es una secuencia ordenada y dinámica de alteraciones moleculares y celulares.
- Integración mecanicista: La integración de múltiples mecanismos explica la heterogeneidad y persistencia del cáncer.
🧠 Puntos clave
- Alteraciones moleculares: El cáncer se basa en alteraciones moleculares y celulares que rompen la homeostasis tisular.
- Mutaciones genéticas: Mutaciones genéticas facilitan proliferación descontrolada y evasión de apoptosis.
- Angiogénesis y microambiente: La angiogénesis y remodelación del microambiente son esenciales para crecimiento tumoral.
- Invasión tisular: La invasión tisular requiere pérdida de adhesión y degradación de matriz extracelular.
- Escape inmunológico: El escape inmunológico se debe a modificaciones antigenicas y supresión de la respuesta inmune.
- Técnicas combinadas: La combinación de técnicas estructurales y funcionales es clave para entender la fisiopatología tumoral.
❓ Preguntas frecuentes
¿Cómo desregula el cáncer el ciclo celular?
Por mutaciones en genes que controlan puntos de control, permitiendo divisiones celulares sin restricciones.
¿Por qué la apoptosis suele estar ausente en células malignas?
Debido a la sobreexpresión de proteínas inhibitorias y bloqueo de vías proapoptóticas que impiden la muerte programada.
¿En qué consiste el escape inmune del cáncer?
Las células tumorales modifican sus antígenos o secretan moléculas que inhiben la función de células inmunitarias para evitar su eliminación.
¿Cómo contribuye la angiogénesis a la progresión tumoral?
Genera nuevos vasos sanguíneos que proporcionan oxígeno y nutrientes, favoreciendo el crecimiento y viabilidad tumoral.
¿Cómo inicia y progresa la invasión y metastatización?
Por pérdida de adhesión celular y producción de enzimas que degradan la matriz extracelular, permitiendo migración y colonización de órganos distantes.
¿Qué papel tienen las moléculas señalizadoras en la biología tumoral?
Regulan la comunicación intercelular y con el microambiente, promoviendo proliferación, migración, invasión y evasión inmune.
¿Por qué es fundamental el microambiente tumoral para la persistencia del cáncer?
Porque modula la interacción con células inmunes y moléculas que pueden favorecer o inhibir la supervivencia tumoral.
¿Cómo ayudan las técnicas moleculares al entendimiento del cáncer?
Permiten detectar mutaciones y cambios en expresión génica, ayudando a comprender mecanismos de transformación y progresión tumoral.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico sobre la fisiopatología tumoral presentado en el artículo.
Nivel 1 – Básico
¿Cuál es la función principal del núcleo celular en la fisiopatología del cáncer según el artículo?
¿Qué rol tiene la mitocondria en el cáncer según el texto?
¿Cuál es una de las funciones de las moléculas señalizadoras en el microambiente tumoral?
Nivel 2 – Intermedio
¿Cuál es la relación correcta entre mutaciones en el núcleo y la alteración en la membrana plasmática en células tumorales?
Según el artículo, ¿qué diferencia funcional existe entre las proteínas Bcl-2 y las caspasas en el contexto del cáncer?
¿Cuál de las siguientes afirmaciones describe adecuadamente el proceso de invasión tisular en el cáncer?
Nivel 3 – Avanzado
Si una célula tumoral aumenta la secreción de VEGF y disminuye la expresión de E-cadherina, ¿qué consecuencia fisiopatológica se espera según el artículo?
¿Cómo contribuye la disfunción mitocondrial a la resistencia tumoral a la apoptosis y proliferación según el texto?
Según la secuencia progresiva de alteraciones en la tumorogénesis, ¿qué ocurre después de la pérdida de adhesión celular y activación de angiogénesis?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.