⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
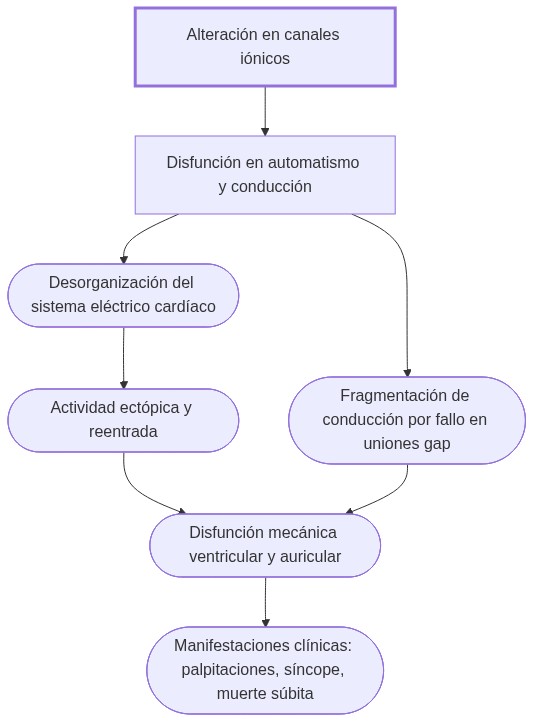
El mecanismo de arritmias es la alteración en la generación o propagación del impulso eléctrico cardíaco causada por disfunciones en canales iónicos, células marcapasos y conexiones intercelulares que resultan en ritmos cardíacos irregulares y descoordinados.
🧬 Concepto base
Las arritmias son trastornos eléctricos del corazón donde la coordinación celular falla. Involucran células especializadas, canales iónicos y vías de conducción que regulan el ciclo cardíaco.
⚙️ Mecanismo clave
Alteraciones en canales de Na⁺, K⁺ y Ca²⁺ o en uniones gap modifican la despolarización, repolarización y conducción, generando automatismo anormal, actividad desencadenada o reentrada que producen ritmos irregulares.
🔗 Por qué es importante
Estas disfunciones afectan la sincronía eléctrica y contráctil del corazón, provocando compromiso en la eficiencia cardíaca y base fisiopatológica de trastornos arrítmicos.
🎯 Puntos que suelen preguntarse en examen
- Definición y función del nodo sinoauricular en el automatismo cardíaco
- Rol de canales iónicos en fases del potencial de acción
- Importancia de uniones gap en la transmisión eléctrica rápida
- Mecanismos celulares que conducen a reentrada y arritmia
- Diferencias regionales en canales iónicos y su relación con la susceptibilidad a arritmias
- Impacto de la isquemia en la función iónica y generación de ritmos ectópicos
Palabras clave: mecanismo de arritmias, canales iónicos, nodo sinoauricular, uniones gap, potencial de acción, automatismo, reentrada, fibras de Purkinje
El mecanismo de arritmias describe cómo los procesos celulares y fisiológicos coordinan la actividad eléctrica del corazón y cómo las alteraciones en estos procesos originan anomalías en el ritmo cardíaco.
Comprender profundamente estos mecanismos es vital para interpretar la función eléctrica cardiaca en estado normal y patológico, pues el ritmo cardíaco se sustenta en la actividad de canales iónicos, la comunicación entre células especializadas y la organización del sistema de conducción.
🧠 Idea central
Las arritmias cardíacas surgen cuando hay alteraciones en la generación o la propagación del impulso eléctrico en el corazón.
A nivel celular, estos ritmos irregulares reflejan cambios en la función de canales iónicos responsables del flujo de sodio (Na+), potasio (K+) y calcio (Ca2+) a través de las membranas de las células cardíacas.
Normalmente, la función de estos canales iónicos y las conexiones intercelulares aseguran una activación eléctrica sincrónica, lo que permite una contracción cardíaca eficiente.
Si alguno de estos mecanismos falla por alteraciones estructurales o funcionales, el corazón puede desarrollar ritmos irregulares de variada severidad.
Estudiar el mecanismo de arritmias implica analizar cómo el sistema eléctrico cardíaco, compuesto por células especializadas y vías de conducción, regula el ritmo normal y cómo los cambios en estos componentes pueden provocar trastornos eléctricos, afectando la función cardíaca global.
🌍 Contexto y alcance
El análisis del mecanismo de arritmias se ubica en la interfaz entre la fisiología celular, la biofísica de membranas y la fisiopatología cardíaca.
Los procesos bioeléctricos implican, en primer lugar, la función de proteínas canal iónico integradas en la membrana de los cardiomiocitos y las células del sistema de conducción.
Cada latido cardíaco inicia en células especializadas dentro del órgano, requiriendo que la señal se propague ordenadamente a través de un tejido organizado.
La alteración de uno o varios componentes a escala molecular, celular o tisular puede modificar el balance eléctrico necesario para mantener el ritmo cardíaco adecuado.
Este campo abarca principalmente la fisiología del corazón y su funcionalidad eléctrica, pero también incorpora elementos de biología estructural y la comprensión de cómo las anomalías celulares pueden traducirse en manifestaciones clínicas.
🧬 Estructuras clave
-
Células del nodo sinoauricular (NSA):
- Qué son: Células especializadas capaces de despolarización espontánea.
- Dónde actúan: Región superior de la aurícula derecha, en el nodo sinoauricular.
- Qué permiten: Inician cada ciclo cardíaco generando el potencial de acción primario.
- Cómo funcionan: Poseen canales iónicos específicos (canales HCN o “funny”, Ca2+ tipo L y T, K+) que regulan fases automáticas de despolarización y repolarización, produciendo la llamada corriente marcapasos. El ciclo inicia con entrada gradual de Na+ y Ca2+ hasta alcanzar el umbral y disparar el potencial de acción, renovándose de manera rítmica.
- Qué ocurre si se altera: Disminución o aumento del automatismo puede resultar en bradicardia o taquicardia; defectos pueden favorecer focos ectópicos o ritmos anormales.
-
Fibras de Purkinje:
- Qué son: Prolongaciones celulares especializadas en la distribución rápida del impulso eléctrico en los ventrículos.
- Dónde actúan: Red terminal a lo largo de los ventrículos, parte del sistema de conducción subendocárdico.
- Qué permiten: Aseguran la sincronización en la contracción ventricular rápida y uniforme.
- Cómo funcionan: Poseen abundantes uniones gap, canales rápidos de Na+, y bajo contenido de miofibrillas, facilitando la alta velocidad de transmisión del impulso desde el nodo auriculoventricular a cada región ventricular.
- Qué ocurre si se altera: Daño o bloqueo en estas fibras puede provocar desincronización contráctil, favorecer reentrada y originar arritmias ventriculares.
-
Miocardio auricular y ventricular:
- Qué es: Tejido muscular cardíaco formado por cardiomiocitos contráctiles.
- Dónde actúa: Paredes de las aurículas y ventrículos.
- Qué permite: Responden al estímulo eléctrico generando contracción mecánica coordinada.
- Cómo funciona: Los potenciales de acción generados y propagados por vías especializadas llegan a los cardiomiocitos, despolarizando la membrana mediante entrada masiva de Na+ y Ca2+, seguidos por salida de K+ para restaurar el potencial de reposo.
- Qué ocurre si se altera: Diferencias de excitabilidad o alteraciones en la sincronización pueden causar actividad ectópica o bloqueos de conducción contribuyentes a arritmias.
-
Canales iónicos de membrana:
- Qué son: Proteínas transmembrana que controlan el movimiento selectivo de iones.
- Dónde actúan: En membranas de células del sistema de conducción y cardiomiocitos.
- Qué permiten: Regulan las fases del potencial de acción (despolarización, meseta, repolarización), orquestando la excitación y recuperación celular.
- Cómo funcionan: Apertura y cierre temporizados de canales de Na+ (inicio rápido), Ca2+ (meseta) y K+ (repolarización), adaptados a la función celular (ej: canales “funny” en NSA, canales rápidos en Purkinje).
- Qué ocurre si se altera: Mutaciones o disfunciones pueden causar despolarizaciones prematuras, prolongación del potencial, actividad desencadenada y mayor vulnerabilidad a ritmos inestables.
-
Uniones gap (conexinas o discos intercalares):
- Qué son: Complejos proteicos que forman canales directos entre citoplasmas de células adyacentes.
- Dónde actúan: Abundan entre cardiomiocitos, especialmente en vías de conducción rápida.
- Qué permiten: Facilitan el paso de iones y moléculas pequeñas, logrando una transmisión rápida y sincronizada del impulso eléctrico.
- Cómo funcionan: Cuando una célula se despolariza, la corriente iónica pasa directamente a células vecinas por las uniones gap, coordinando el frente eléctrico.
- Qué ocurre si se altera: La insuficiencia o pérdida, por fibrosis o necrosis, fragmenta el impulso y favorece circuitos de reentrada y arritmias sostenidas.
| Estructura | Función | Relevancia en arritmias |
|---|---|---|
| Nodo sinoauricular | Genera el impulso eléctrico inicial y establece el ritmo | Su disfunción facilita marcapasos ectópicos o ritmos anormales |
| Fibras de Purkinje | Distribuyen el estímulo hacia los ventrículos sincronizados | Daño impulsa desincronización y facilita reentrada |
| Canales iónicos | Definen fases del potencial de acción | Alteración provoca automatismo ectópico o actividad desencadenada |
| Uniones gap | Permiten conducción eléctrica rápida | Defecto promueve bloqueos o reentrada eléctrica |
⚙️ Funciones y procesos
La generación y propagación del impulso eléctrico en el corazón es resultado de una secuencia ordenada de fenómenos eléctricos a nivel celular.
Detallar cada fase permite entender cómo un pequeño cambio puede desencadenar arritmias.
-
Automatismo (generación espontánea del impulso):
- Qué es: Propiedad de ciertas células para despolarizarse autónomamente sin estímulo externo.
- Dónde ocurre: Predomina en el nodo sinoauricular, con menor incidencia en nodo auriculoventricular y fibras de Purkinje.
- Qué permite: Inicia cada ciclo cardíaco permitiendo un ritmo basal.
- Cómo funciona: Al finalizar la repolarización, los canales “funny” permiten un flujo lento de Na+ y Ca2+, aumentando progresivamente el potencial de membrana hasta disparar un nuevo potencial de acción.
Este automatismo es modulable por el sistema nervioso autónomo. - Alteraciones: Un aumento genera latidos prematuros; su disminución puede causar pausas o fallo en el inicio del latido.
-
Despolarización rápida:
- Qué es: Fase donde el voltaje celular aumenta bruscamente.
- Dónde ocurre: En todas las células excitables, destacando fibras rápidas ventriculares y Purkinje.
- Qué permite: Produce un frente eléctrico fuerte para propagar la activación celular.
- Cómo funciona: Apertura súbita de canales rápidos de Na+ permite entrada masiva de sodio, elevando el potencial hasta cerca de +30 mV.
- Alteraciones: Defectos en canales reducen amplitud o velocidad del impulso, favoreciendo ritmos lentos o disociados.
-
Fase de meseta y repolarización:
- Qué es: Período en que el potencial de membrana permanece estable antes de volver al reposo.
- Dónde ocurre: En cardiomiocitos ventriculares y fibras de Purkinje.
- Qué permite: Facilita el acoplamiento excitación-contracción y asegura un intervalo refractario eléctrico.
- Cómo funciona: La entrada lenta de Ca2+ por canales tipo L equilibra la salida de K+; luego predomina la salida de K+ para restaurar el potencial de reposo.
- Alteraciones: Prolongación puede propiciar actividad desencadenada o reentrada arrítmica.
-
Conducción eléctrica intercelular:
- Qué es: Transmisión del impulso entre células.
- Dónde ocurre: En todo el miocardio; facilitada por uniones gap.
- Qué permite: Sincroniza la contracción auricular y ventricular.
- Cómo funciona: Los iones que fluyen por uniones gap modifican el potencial de membrana celular vecina, propagando la señal.
- Alteraciones: Barreras anatómicas o patológicas fragmentan la conducción, generando zonas susceptibles a reentrada.
Cualquier disrupción en uno o más pasos puede desencadenar arritmias.
Por ejemplo, una repolarización incompleta permite que una célula se reactive antes de tiempo; una conducción lenta facilita circuitos de reentrada.
La integración de estas funciones desde la escala iónica hasta el tejido es la base de la homeostasis eléctrica cardíaca.
🔗 Integración funcional
El corazón requiere una integración precisa entre su arquitectura, la función de canales iónicos y la conectividad celular para mantener el equilibrio entre excitación y recuperación eléctrica.
La integridad de los canales iónicos es esencial:
- Las disfunciones en canales de potasio (K+) prolongan la repolarización, aumentando la posibilidad de posdespolarizaciones y actividad desencadenada.
- Anomalías en canales de sodio (Na+) reducen la velocidad y fuerza del frente eléctrico, favoreciendo bloqueos y ritmos ectópicos.
- Alteraciones en canales de calcio (Ca2+) afectan la duración de la meseta, alterando la contractilidad y favoreciendo arritmias dependientes de Ca2+.
La conectividad por uniones gap asegura la propagación rápida y sincronizada del impulso.
Lesiones o fibrosis pueden fragmentar la conducción, facilitando bloqueos y reentrada.
La organización espacial y los gradientes de excitabilidad dependen de la distribución regional de canales iónicos y conexiones.
Por ejemplo:
- El nodo sinoauricular tiene menor densidad de canales de sodio, pero alto contenido de canales “funny” y calcio para optimizar el automatismo.
- Las fibras de Purkinje concentran canales de sodio para una propagación eficiente del impulso.
- La heterogeneidad regional se traduce en distintos umbrales de excitabilidad y refractariedad, creando sitios vulnerables a arritmias.
Así, la arritmia resulta cuando detalles moleculares y estructurales fallan en coordinar la actividad eléctrica global, produciendo desencadenamiento, propagación o mantenimiento aberrantes del impulso cardíaco.
🔬 Métodos y evidencias
El estudio del mecanismo de arritmias utiliza métodos que descifran la dinámica eléctrica desde la escala molecular hasta la tisular:
-
Registro intracelular del potencial de acción:
Mide en células individuales las fases y amplitud del potencial de acción, permitiendo observar el efecto directo de los canales iónicos sobre la excitabilidad celular. -
Electrocardiografía (ECG):
Registra de forma no invasiva la propagación global del impulso, identificando irregularidades en automatismo, conducción o repolarización, y vinculándolas con disfunciones celulares o tisulares. -
Modelos experimentales celulares y tisulares:
Permiten manipular la función o expresión de canales y conexiones, validando su papel en la generación y propagación del impulso. -
Estudios de propagación óptica:
Visualizan frentes de activación en tejidos conjugando colorantes sensibles a voltaje, revelando bloqueos, reentradas y heterogeneidades eléctricas.
Estos métodos han establecido vínculos causales entre alteraciones moleculares o estructurales y el desarrollo de arritmias, integrando observaciones directas, patrones eléctricos y modelos explicativos.
🩺 Puente clínico
El conocimiento profundo del mecanismo de arritmias fundamenta el razonamiento clínico, permitiendo interpretar alteraciones del ritmo cardíaco observadas en la práctica.
Por ejemplo, en electrocardiogramas, una taquicardia regular puede sugerir automatismo aumentado o actividad ectópica; una arritmia irregular con ondas fragmentadas puede indicar conducción desorganizada y reentradas, producto de alteraciones en canales iónicos o conexiones celulares.
El análisis del ritmo observado tiene correspondencia directa con la función (o alteración) de los mecanismos celulares y tisulares descritos.
Así, la fisiología y fisiopatología eléctricas son la base para entender la presentación y consecuencias de trastornos del ritmo cardíaco.
💎 Perlas de alto rendimiento
- Nodo sinoauricular establece ritmo cardíaco basal: debido a su automatismo basado en canales “funny” (If) y de calcio.
- Fibras de Purkinje logran máxima velocidad: de conducción por su alta densidad de canales rápidos de sodio y abundantes uniones gap.
- Mutaciones en canales iónicos modifican fases: del potencial de acción, predisponiendo a diferentes arritmias.
- Uniones gap permiten comunicación iónica rápida: entre cardiomiocitos, facilitando la propagación sincronizada del impulso.
- Focos ectópicos suelen surgir por despolarización espontánea anómala: cuando una célula fuera del marcapasos principal desarrolla dicha actividad.
- Circuitos de reentrada aparecen con bloqueos unidireccionales: y circuitos anatómicos o funcionales que recirculan el impulso.
- Potencial de acción cardíaco tiene fases con regulación precisa: de Na+, Ca2+ y K+, clave para la función eléctrica.
- Heterogeneidad regional en excitabilidad y refractariedad: es un sustrato crucial para el inicio y mantenimiento de arritmias.
🧠 Puntos clave
- Arritmias surgen por alteraciones: en la generación o conducción del impulso eléctrico cardíaco.
- Canales iónicos controlan fases: del potencial de acción y regulan la excitación celular.
- Transmisión intercelular mediante uniones gap: es clave para la sincronía y propagación ordenada.
- Diferencias regionales en canales y estructuras: explican los sitios vulnerables a arritmias.
- Prolongación o fragmentación del potencial de acción: influye en la susceptibilidad a ritmos anormales.
- Alteraciones en cualquier componente del sistema eléctrico: del corazón pueden reflejarse en manifestaciones clínicas.
❓ Preguntas frecuentes
¿Cómo se origina normalmente el impulso eléctrico cardíaco y qué elementos lo regulan?
El impulso eléctrico cardíaco se origina en el nodo sinoauricular gracias a canales “funny” y de calcio que producen despolarización espontánea. Su actividad está regulada por el sistema nervioso autónomo y la integridad estructural del nodo.
¿Por qué los canales iónicos son tan relevantes en la generación de arritmias?
Estos canales determinan cuándo y cómo una célula cardíaca se excita o recupera. Alteraciones en su función o expresión pueden originar latidos prematuros, prolongar el potencial de acción y aumentar el riesgo de actividad desencadenada patológica.
¿Qué función cumplen las uniones gap y cómo afectan la sincronía cardíaca?
Las uniones gap forman canales que conectan el citoplasma de células adyacentes, permitiendo el paso rápido de iones y la transmisión sincronizada del impulso. Su alteración puede causar conducción lenta, bloqueos o circuitos de reentrada que producen arritmias.
¿Qué es una reentrada y cómo se establece un circuito patológico de reexcitación?
La reentrada es la recirculación del impulso eléctrico en un circuito anatómico o funcional, generando activación repetitiva anormal. Se establece cuando existe bloqueo unidireccional y retardos en conducción o recuperación que permiten la recirculación del estímulo.
¿Cómo influye la diversidad de canales iónicos y estructuras entre diferentes regiones cardíacas en la susceptibilidad a arritmias?
La variación en tipos y densidad de canales iónicos crea entornos eléctricos específicos. Por ejemplo, el nodo sinoauricular tiene más canales “funny” y menos de sodio que las fibras de Purkinje, generando diferencias en excitabilidad y refractariedad que determinan vulnerabilidad regional a arritmias.
¿De qué manera la isquemia contribuye al mecanismo de arritmias desde la perspectiva celular?
La isquemia altera el metabolismo celular y la función de canales iónicos, generando gradientes iónicos y zonas eléctricamente inestables que favorecen la actividad ectópica o la formación de circuitos de reentrada.
¿Qué técnicas experimentales permiten observar directamente la generación de una arritmia a nivel celular?
Los registros intracelulares y los estudios mediante colorantes sensibles al voltaje monitorean en tiempo real las fases del potencial de acción y la propagación del impulso, mostrando los efectos de alteraciones en canales iónicos y conexiones intercelulares.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico sobre los mecanismos de arritmias cardíacas presentado en el artículo.
Nivel 1 – Básico
¿Cuál es la función principal de las células del nodo sinoauricular (NSA)?
¿Qué permiten las uniones gap en el corazón?
¿Qué iones están implicados en la función de los canales iónicos cardíacos según el artículo?
Nivel 2 – Intermedio
Según el artículo, ¿qué relación es correcta entre las fibras de Purkinje y sus canales iónicos?
¿Cómo distingue el artículo las funciones del nodo sinoauricular (NSA) y las fibras de Purkinje en el sistema eléctrico cardíaco?
¿Cuál es la consecuencia de la alteración de las uniones gap según el artículo?
Nivel 3 – Avanzado
Si se produce una disfunción en los canales de potasio (K+) según el artículo, ¿qué alteración sería esperable en la función eléctrica cardíaca?
Según el artículo, ¿cómo puede la alteración en la fase de repolarización contribuir al desarrollo de arritmias?
En el mecanismo completo de generación y propagación del impulso, ¿qué sucede si la conducción intercelular es fragmentada por fibrosis según el artículo?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.