⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La fisiopatología insuficiencia cardiaca describe las alteraciones estructurales y funcionales del corazón que reducen su capacidad de llenado y eyección ventricular, generando baja perfusión y elevación sostenida de presiones intracardiacas. Estas disfunciones activan respuestas neurohormonales que inicialmente compensan pero agravan el daño, perpetuando un ciclo de remodelado, congestión y deterioro sistémico.
🧬 Concepto base
La insuficiencia cardiaca es un síndrome clínico por daño en tejido miocárdico y estructuras cardíacas, afectando la función contráctil y llenado ventricular. Esto disminuye el gasto cardiaco y altera la dinámica de presión que mantiene la circulación.
⚙️ Mecanismo clave
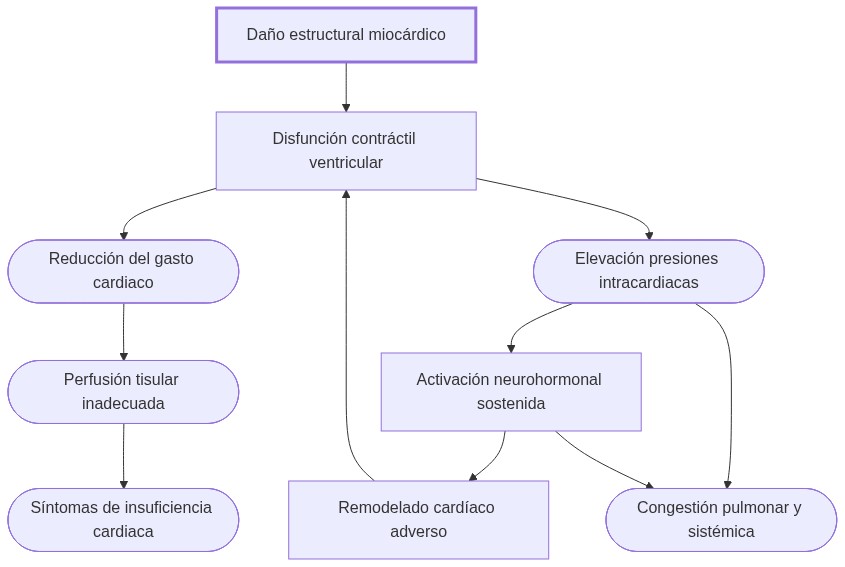
Daño estructural (isquemia, fibrosis) → disminución de la contractilidad → menor volumen sistólico y aumento de presiones intracavitarias → activación neurohormonal → retención de líquido y vasoconstricción → remodelado miocárdico progresivo y congestión vascular.
🔗 Por qué es importante
Este proceso limita la perfusión tisular y provoca congestión sistémica y pulmonar, base de los signos y síntomas característicos.
🎯 Puntos que suelen preguntarse en examen
- Definición y causas de disfunción sistólica ventricular
- Rol de la activación neurohormonal en la progresión de la insuficiencia
- Diferencia y efecto de la precarga y poscarga sobre el corazón
- Mecanismos celulares de fibrosis y remodelado cardíaco
- Relación entre gasto cardiaco y perfusión tisular
- Cambios estructurales histológicos en insuficiencia cardiaca
Palabras clave: fisiopatología insuficiencia cardiaca, miocardio, remodelado cardíaco, neurohormonal, gasto cardiaco, fibrosis, precarga, poscarga
La fisiopatología de la insuficiencia cardiaca abarca el conjunto de mecanismos estructurales y funcionales que alteran la función del corazón, originando manifestaciones sistémicas secundarias a la incapacidad del órgano para responder a las demandas metabólicas del cuerpo.
Analizar los procesos desde los cambios celulares hasta las consecuencias hemodinámicas permite profundizar en el entendimiento del síndrome y en la integración del razonamiento fisiopatológico.
🧠 Idea central
La insuficiencia cardiaca es un síndrome clínico resultado de alteraciones estructurales o funcionales del corazón que dificultan el llenado o la eyección ventricular adecuada.
Como consecuencia, se produce una disminución del gasto cardiaco y/o un aumento sostenido de las presiones intracardiacas.
Esta disfunción, de curso progresivo, representa una fase final común a diversas enfermedades cardiovasculares crónicas.
El análisis fisiopatológico descompone tres procesos interrelacionados:
- Daño estructural inicial: Afecta la arquitectura cardíaca por isquemia, hipertrofia, fibrosis o remodelado.
- Alteración funcional: Reduce la eficacia del llenado (diastólica) o expulsión (sistólica) ventricular y aumenta las presiones intracardíacas.
- Respuestas compensatorias: Activaciones neurohormonales que inicialmente sostienen la perfusión pero a largo plazo agravan la disfunción.
Comprender la insuficiencia cardiaca requiere entender cómo estos elementos generan consecuencias específicas en la circulación y órganos diana.
🌍 Contexto y alcance
La fisiopatología de la insuficiencia cardiaca se estudia principalmente a nivel del sistema cardiovascular, integrando componentes cardíacos, vasculares y neurohormonales.
Su explicación abarca desde la escala celular, con alteraciones en los cardiomiocitos, hasta el impacto global sobre la función orgánica y la circulación.
Específicamente:
- A nivel celular, se observan cambios en cardiomiocitos, metabolismo energético, canales iónicos y vías de señalización.
- A nivel tisular, hay depósitos de matriz extracelular, fibrosis y remodelado del tejido muscular cardíaco.
- A nivel de órgano, el corazón reduce su eficiencia como bomba, afectando la perfusión y dinámica hemodinámica sistémica.
- A nivel sistémico, se activan sistemas neurohormonales que modifican volumen y resistencia periférica para compensar la disfunción.
El análisis integrado de estos niveles relaciona los cambios microscópicos con manifestaciones clínicas en insuficiencia cardiaca.
🧬 Estructuras clave
La fisiopatología de la insuficiencia cardiaca involucra múltiples estructuras anatómicas, celulares y sistemas reguladores con roles específicos:
-
Miocardio:
- ¿Qué es? Células musculares cardíacas (cardiomiocitos) responsables de la contracción que genera gasto cardiaco.
- ¿Dónde actúa? Paredes ventriculares, predominando en el ventrículo izquierdo por la demanda sistémica.
- ¿Qué permite? Contracción sincrónica que genera la presión para expulsar la sangre hacia la circulación.
- ¿Qué ocurre si se altera? Isquemia, fibrosis e hipertrofia que afectan la estructura y la contractilidad, disminuyendo la eficiencia.
-
Válvulas cardiacas:
- ¿Qué es? Tejido conectivo con revestimiento endotelial que separa cavidades cardíacas.
- ¿Dónde actúa? Entre aurículas y ventrículos (mitral, tricúspide) y entre ventrículos y arterias (aórtica, pulmonar).
- ¿Qué permite? Permiten flujo unidireccional, evitando el reflujo sanguíneo.
- ¿Qué ocurre si se altera? Insuficiencia o estenosis que aumentan la carga de trabajo y la sobrecarga crónica de presión o volumen.
-
Vasos sanguíneos (arterias y venas):
- ¿Qué es? Conductos que distribuyen y retornan la sangre.
- ¿Dónde actúa? Arterias y venas sistémicas y pulmonares.
- ¿Qué permite? La resistencia y capacitancia modulan precarga (llenado ventricular) y poscarga (resistencia al vaciado).
- ¿Qué ocurre si se altera? Cambios en el tono vascular afectan la presión y favorecen congestión o hipoperfusión.
-
Sarcomero y unidad contráctil:
- ¿Qué es? Unidad funcional de contracción formada por actina, miosina y proteínas reguladoras.
- ¿Dónde actúa? Miofibrillas en cada cardiomiocito.
- ¿Qué permite? Transforma la señal eléctrica en acortamiento mecánico coordinado.
- ¿Qué ocurre si se altera? Daños en proteínas contráctiles y manejo alterado del calcio reducen la eficacia contráctil.
-
Sistema neurohormonal:
- ¿Qué es? Incluye sistema nervioso simpático, eje renina-angiotensina-aldosterona y péptidos natriuréticos.
- ¿Qué permite? Actúa en riñón, vasculatura y corazón para controlar volemia y resistencia vascular.
- ¿Qué ocurre si se altera? Vasoconstricción, retención de sodio y efectos tróficos que inicialmente compensan pero a largo plazo son dañinos.
- ¿Qué produce? Activación sostenida genera sobrecarga y remodelado adverso que progresa a insuficiencia cardiaca.
La interacción y disfunción conjunta de estas estructuras subyace a la progresión del síndrome de insuficiencia cardiaca.
⚙️ Funciones y procesos
La insuficiencia cardiaca evoluciona a través de una serie de eventos mecánicos y fisiológicos en los que respuestas adaptativas iniciales terminan siendo perjudiciales al deteriorarse la función ventricular.
Cada proceso debe analizarse según su lógica causal y estructural.
-
Disfunción miocárdica:
- Definición: Pérdida de capacidad contráctil efectiva de los cardiomiocitos.
- Localización: Principalmente ventrículo izquierdo, aunque puede afectar otras cavidades según la causa.
- Función alterada: Reducción del volumen sistólico y gasto cardiaco.
- Mecanismos: Isquemia, fibrosis y alteraciones en la excitación-contracción disminuyen fuerza sarcomérica.
- Impacto: Menor perfusión a órganos con altas demandas.
-
Alteraciones del llenado y presión intracardíaca:
- Definición: Elevación anormal y persistente de presiones ventriculares en diástole por vaciamiento insuficiente.
- Localización: Ventrículos, que acumulan volumen residual.
- Consecuencias: Mayor precarga y distensión ventricular con estrés hemodinámico y remodelado tisular.
- Pasos:
- Volumen residual tras eyección incompleta.
- Incremento de presión diastólica.
- Estrés en la pared y alteraciones en matriz extracelular.
- Resultado: Congestión retrógrada en venas pulmonares y sistémicas.
-
Alteración de poscarga y circuito vascular:
- Definición: Aumento de la resistencia al flujo que debe superar el ventrículo en sístole.
- Localización: Vasculatura arterial periférica y pulmonar.
- Implicación: Mayor demanda contráctil ventricular.
- Causas: Vasoconstricción neurohormonal (adrenalina, angiotensina II).
- Impacto: Dificultad para eyectar sangre y agravamiento de la disfunción miocárdica.
-
Activación neurohormonal (respuestas compensatorias):
- Definición: Aumento de catecolaminas, activación del sistema renina-angiotensina-aldosterona y secreción de péptidos natriuréticos.
- Áreas de acción: Corazón, vasculatura y riñones.
- Efectos inmediatos:
- Simpatía: Incremento de frecuencia y contractilidad.
- Renina-angiotensina-aldosterona: Vasoconstricción y retención de sodio y agua.
- Péptidos natriuréticos: Promueven excreción de sodio para compensar volumen.
- Repercusiones crónicas: Remodelado adverso, sobrecarga volumétrica y estrés ventricular.
-
Remodelado cardíaco:
- Definición: Cambios estructurales en tamaño, forma y composición cardíaca tras agresión crónica.
- Localización: Principalmente ventrículo izquierdo, aunque puede ser biventricular.
- Fases:
- Hipertrofia de cardiomiocitos para soportar estrés de pared.
- Dilatación ventricular con aumento del radio interno.
- Fibrosis con acúmulo de matriz extracelular que reduce distensibilidad y función.
- Impacto: Pérdida de coordinación contráctil, mayor riesgo de arritmias y avance de la insuficiencia.
-
Insuficiencia progresiva:
- Definición: Estado en que las adaptaciones compensatorias se vuelven insuficientes y dañinas.
- Manifestaciones: Pérdida de gasto cardiaco eficaz, acumulación de líquidos y bajo flujo sanguíneo.
- Signos: Congestión sistémica y pulmonar y síntomas vinculados al déficit perfusional, como disnea y fatiga.
Estos procesos son consecuencia directa de cambios estructurales, funcionales y adaptativos conectados dentro del corazón y sus sistemas reguladores.
🔗 Integración funcional
La fisiopatología de la insuficiencia cardiaca se basa en que cambios estructurales (daño e hipertrofia miocárdica) generan alteraciones funcionales que inducen respuestas compensatorias y disfuncionales en el sistema cardiovascular y neurohormonal.
-
Cadena causal:
- Disminución de contractilidad → reducción del volumen sistólico.
- Disminución del volumen sistólico → caída en el gasto cardiaco.
- Gasto cardiaco insuficiente → menor perfusión a órganos distales.
- Acúmulo de sangre ventricular → aumento de presión intracavitaria y activación de mecanismos compensatorios.
- Activación neurohormonal → retención de líquido y vasoconstricción, elevando precarga y poscarga.
- Remodelado estructural sostenido → modificación adversa de forma y función cardiaca, perpetuando disfunción.
-
Interrelación entre niveles:
- Alteraciones moleculares afectan proteínas contráctiles y canales iónicos.
- Disfunción miocítica altera mecánica ventricular global y adaptación a sobrecargas.
- Respuestas neurohormonales y estructurales integradas influyen en la progresión y severidad del síndrome.
Por ello, la insuficiencia cardiaca resulta de la suma de múltiples cambios anatómicos, hemodinámicos y adaptativos que, juntos, generan la disfunción progresiva del corazón como bomba.
🔬 Métodos y evidencias
La comprensión de la fisiopatología de la insuficiencia cardiaca se fundamenta en diversas técnicas que permiten analizar cada nivel estructural y funcional.
-
Estudios biomecánicos:
- Descripción: Evaluación de contracción y relajación en miocitos aislados o tejido cardíaco viable.
- Utilidad: Determinan acoplamiento excitación-contracción, fuerza máxima y respuesta a estrés mecánico.
-
Observaciones hemodinámicas invasivas:
- Descripción: Cateterismo cardíaco para medir presiones y flujos en cavidades cardíacas.
- Función: Correlacionan presión telediastólica, gasto cardiaco y congestión.
-
Análisis celular y molecular:
- Descripción: Biopsias y modelos experimentales para identificar cambios microscópicos.
- Hallazgos: Fibrosis, pérdida celular, remodelado sarcomérico y activación de vías de estrés y muerte celular.
-
Marcadores neurohormonales:
- Descripción: Dosificación en sangre de catecolaminas, renina, angiotensina, aldosterona y péptidos natriuréticos.
- Función: Reflejan activación compensatoria y relacionan con grado de disfunción estructural.
Estas evidencias sostienen el entendimiento de la fisiopatología desde la lesión inicial hasta los cambios funcionales sistémicos observados.
🩺 Puente clínico
El razonamiento clínico sobre la insuficiencia cardiaca interpreta signos y síntomas según los mecanismos fisiopatológicos subyacentes:
- Disminución del gasto cardiaco: Se manifiesta como bajo flujo sanguíneo tisular, fatiga y debilidad muscular, debido a la incapacidad ventricular para mantener volumen expulsado adecuado.
- Elevación de presiones intracardiacas: La congestión retrógrada hace que sangre se acumule en venas pulmonares y sistémicas, causando edema periférico y disnea, asociados al aumento de precarga y llenado ventricular insuficiente.
- Activación compensatoria: Taquicardia, hepatomegalia y retención de líquidos son efectos del sistema simpático y eje renina-angiotensina-aldosterona, que buscan mantener la perfusión pero aumentan la carga y dañan el corazón.
Interpretar cada síntoma permite conectar la disfunción miocárdica, respuesta neurohormonal y alteración hemodinámica que caracterizan la insuficiencia cardiaca.
Este enfoque facilita anticipar complicaciones basadas en la fisiología del proceso.
💎 Perlas de alto rendimiento
- Disfunción estructural o funcional: La insuficiencia cardiaca refleja disfunción estructural o funcional que limita el llenado o la eyección ventricular.
- Activación neurohormonal: La activación neurohormonal inicialmente sostiene el gasto cardiaco pero perpetúa daño estructural y fibrosis.
- Remodelado cardíaco: El remodelado cardíaco puede comprender hipertrofia y dilatación ventricular, afectando la geometría y función.
- Fibrosis y conducción eléctrica: La fibrosis altera la conducción eléctrica, favoreciendo arritmias por disincronía miocárdica.
- Disfunción excitación-contracción: La disfunción del acoplamiento excitación-contracción, principalmente por alteraciones del calcio intracelular, reduce la eficacia de cada sístole.
- Sobrecarga hemodinámica: La sobrecarga hemodinámica genera congestión venosa pulmonar o sistémica, según la cavidad afectada.
- Mecanismos múltiples: La insuficiencia cardiaca es resultado de la interacción compleja de múltiples mecanismos que comprometen la función de bomba cardíaca.
- Daño progresivo: El daño progresivo se explica por la cronificación de las respuestas compensatorias y modificaciones estructurales.
🧠 Puntos clave
- Origen y definición: La insuficiencia cardiaca surge de alteraciones en la estructura o función cardíaca que impiden el llenado o la eyección ventricular adecuados.
- Componentes del síndrome: El síndrome integra daño miocárdico, desequilibrios hemodinámicos y respuestas neurohormonales compensatorias y progresivas.
- Adaptación y disfunción: El remodelado cardíaco es una adaptación inicial que con el tiempo contribuye a la disfunción y gravedad del cuadro.
- Activación neurohormonal crónica: La activación prolongada de sistemas neurohormonales agrava la carga estructural y funcional del corazón.
- Interacción patológica: La interacción de pérdida contráctil, congestión y sobrecarga de presión define la presentación clínica y evolución.
- Cambios celulares y anatómicos: Los cambios moleculares, celulares y anatómicos convergen en deterioro progresivo de la función cardíaca efectiva.
❓ Preguntas frecuentes
¿Qué es la disfunción sistólica en insuficiencia cardiaca?
Es la incapacidad del ventrículo para generar fuerza contráctil suficiente, reduciendo el volumen expulsado y el gasto cardiaco. Se relaciona con alteraciones estructurales y del acoplamiento excitación-contracción.
¿Cómo impacta la activación neurohormonal en la progresión del daño cardíaco?
Inicialmente es compensatoria para mantener perfusión; sin embargo, su persistencia genera retención hídrica, vasoconstricción y remodelado que aumentan el estrés ventricular y aceleran la disfunción.
¿Qué explica la fibrosis miocárdica a nivel celular?
La activación de fibroblastos y acumulación excesiva de colágeno y matriz extracelular reducen la distensibilidad del miocardio y alteran la transmisión eléctrica y la capacidad contráctil.
¿Por qué el corazón se remodela y cómo puede ser perjudicial esto?
El remodelado adapta la estructura a sobrecargas de presión o volumen mediante hipertrofia o dilatación; sin embargo, aumenta el consumo energético y altera la geometría, perpetuando la disfunción.
¿Cuál es la diferencia entre precarga y poscarga y su efecto en la función cardíaca?
La precarga es el volumen ventricular de llenado antes de la contracción, y la poscarga es la resistencia que debe superar el ventrículo para expulsar sangre. El aumento sostenido de ambas carga el miocardio y empeora su función.
¿Cómo afecta la disminución del gasto cardiaco la perfusión tisular?
Reduce el suministro de oxígeno y nutrientes, causando síntomas como fatiga y disnea por déficit funcional en órganos y tejidos periféricos.
¿Qué cambios histológicos caracterizan la insuficiencia cardiaca?
Se evidencian hipertrofia de cardiomiocitos, fibrosis y pérdida celular, modificando la organización y función del tejido miocárdico.
Evaluación Interactiva Progresiva
Este cuestionario evalúa el contenido biológico relacionado con la fisiopatología de la insuficiencia cardiaca según el artículo proporcionado.
Nivel 1 – Básico
¿Qué estructura está formada por células musculares cardíacas responsables de la contracción que genera el gasto cardiaco?
¿Qué función tienen las válvulas cardiacas según el texto?
¿Cuál es la consecuencia inmediata de las alteraciones estructurales o funcionales del corazón en la insuficiencia cardiaca?
Nivel 2 – Intermedio
¿Cuál es la relación correcta entre los cambios celulares y la función miocárdica en insuficiencia cardiaca según el artículo?
Según el texto, ¿qué diferencia principal existe entre precarga y poscarga en la insuficiencia cardiaca?
¿Cuál de estas afirmaciones refleja la interacción entre activación neurohormonal y remodelado cardíaco según el texto?
Nivel 3 – Avanzado
Según la cadena causal descripta, ¿qué consecuencia sigue a la disminución del volumen sistólico ventricular en la insuficiencia cardiaca?
¿Qué secuencia describe correctamente los pasos del aumento de presión diastólica ventricular según el artículo?
¿Cuál es la consecuencia funcional crónica de la activación neurohormonal prolongada en la insuficiencia cardiaca, según el texto?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.