⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La fisiopatología isquémica cardíaca consiste en el daño celular y tisular por desequilibrio entre oferta y demanda de oxígeno en el miocardio, provocado mayormente por obstrucción aterosclerótica coronaria, que desencadena falla metabólica, alteración iónica, inflamación y necrosis.
🧬 Concepto base
Proceso biológico donde la reducción del flujo sanguíneo y oxígeno afecta las células miocárdicas, alterando su función metabólica y contráctil, generando daño estructural progresivo.
⚙️ Mecanismo clave
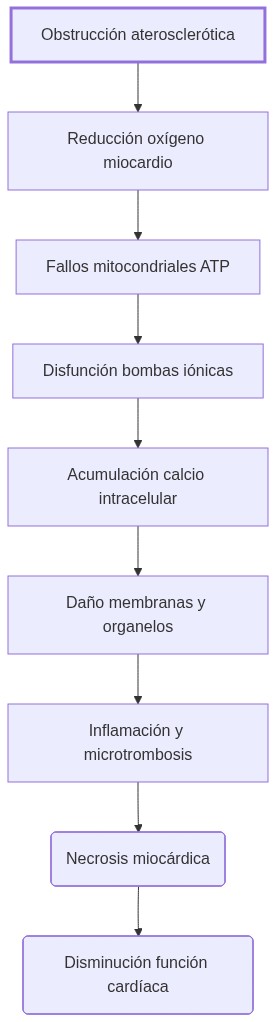
Obstrucción coronaria reduce oxígeno → disminución de ATP mitocondrial → fallo de bombas iónicas → acumulación de Ca²⁺ intracelular → activación enzimática degradativa → daño celular y necrosis.
🔗 Por qué es importante
Produce pérdida irreversible de miocitos, disminuye contractilidad cardíaca y genera inflamación y trombosis que agravan el compromiso tisular.
🎯 Puntos que suelen preguntarse en examen
- ¿Qué altera la obstrucción coronaria en la fisiopatología isquémica?
- Importancia del ATP mitocondrial en el miocardio.
- Mecanismo de falla de las bombas iónicas en isquemia.
- Rol del calcio intracelular en el daño celular.
- Razones de la vulnerabilidad de la zona subendocárdica.
- Impacto de la disfunción endotelial en la microcirculación.
Palabras clave: fisiopatología isquémica cardíaca, isquemia, miocito, mitocondria, ATP, calcio intracelular, aterosclerosis, endotelio, necrosis miocárdica
La fisiopatología isquémica cardíaca abarca los mecanismos celulares, tisulares y sistémicos inducidos por una alteración en el flujo sanguíneo coronario, que reduce la disponibilidad de oxígeno al músculo cardíaco.
Esta reducción condiciona el funcionamiento del miocardio y, cuando es severa o sostenida, genera un daño estructural y funcional progresivo.
Comprender estos procesos explica la génesis de la enfermedad cardíaca de base isquémica, una de las principales causas de morbilidad y mortalidad en el mundo.
🧠 Idea central
La fisiopatología isquémica cardíaca describe las alteraciones biológicas originadas por un desequilibrio entre la oferta y la demanda de oxígeno en el miocardio.
La causa más frecuente es la obstrucción aterosclerótica de las arterias coronarias, que limita la entrega de oxígeno al tejido cardíaco.
Cuando la oferta sanguínea no cubre las demandas metabólicas miocárdicas, se inicia una secuencia progresiva de eventos celulares que comienza con disfunción metabólica y puede culminar en muerte celular (necrosis).
La escasez de oxígeno afecta la homeostasis y función del miocardio, comprometiendo tanto su estructura como la función cardíaca global.
🌍 Contexto y alcance
La isquemia cardíaca integra eventos desde la escala molecular hasta el órgano completo.
Su origen reside en la vascularización coronaria, donde el endotelio y la luz arterial regulan la entrega de oxígeno.
La aterosclerosis provoca la formación de placas que restringen el flujo sanguíneo.
A nivel celular, la baja disponibilidad de oxígeno afecta fundamentalmente las mitocondrias de las células miocárdicas, obligando a modificar el metabolismo energético.
En el tejido cardíaco, la falta de oxigenación sostenida genera un medio ácido y vulnerable al daño, afectando preferentemente áreas más distales a la irrigación, como la zona subendocárdica.
Estas alteraciones no solo modifican al músculo cardíaco en su estructura microscópica, sino que se reflejan en la función global del corazón, pudiendo desencadenar manifestaciones clínicas.
La fisiopatología isquémica establece el nexo entre las bases moleculares y celulares y la expresión clínica de la enfermedad cardiovascular.
🧬 Estructuras clave
La isquemia cardíaca involucra múltiples estructuras especializadas que sostienen la función contráctil normal.
A continuación se describen las principales, según su contribución al daño isquémico:
| Estructura | Función principal | Rol en la isquemia |
|---|---|---|
| Células miocárdicas | Generan la contracción y mantienen la fuerza de bombeo del corazón | Sufren disfunción metabólica y estructural ante privación de oxígeno, alterando la función o provocando necrosis |
| Mitocondrias | Son la principal fuente de ATP mediante fosforilación oxidativa | Disminuyen la producción de ATP por falta de oxígeno; producen especies reactivas de oxígeno en reperfusión |
| Membranas celulares | Regulan el paso de iones y mantienen la homeostasis interna celular | Disfunción permite entrada anómala de iones (calcio, sodio), favoreciendo daño intracelular |
| Endotelio vascular coronario | Revestimiento interno de arterias coronarias; modula el flujo y el tono vascular | Se reduce su capacidad vasodilatadora, favorece inflamación y fenómenos trombóticos |
| Microcirculación coronaria | Red capilar que aporta oxígeno y nutrientes a zonas profundas del miocardio | Obstrucción o disfunción endotelial disminuye aún más la perfusión local |
A continuación, se detalla el papel específico de cada estructura:
-
Célula miocárdica:
- ¿Definición?: Miocito especializado responsable de la contracción cardíaca.
- ¿Ubicación?: Principal componente funcional de la pared miocárdica.
- ¿Función?: Coordina el latido y el bombeo sanguíneo.
- ¿Cambio en isquemia?: Déficit de oxígeno limita la contracción e induce lesión irreversible en ausencia de reparación.
-
Mitocondria:
- ¿Definición?: Orgánulo encargado de la síntesis de adenosín trifosfato (ATP).
- ¿Ubicación?: Citoplasma de miocitos.
- ¿Función?: Provee energía para la contracción y transporte iónico.
- ¿Mecanismo en isquemia?: Predomina el metabolismo anaerobio menos eficiente; la reperfusión puede generar radicales libres y estrés oxidativo.
-
Membrana plasmática:
- ¿Definición?: Límite físico de la célula con bombas y canales iónicos.
- ¿Ubicación?: Rodea cada miocito.
- ¿Función?: Mantiene segregación iónica esencial para la excitabilidad y homeostasis celular.
- ¿Cambio en isquemia?: Pérdida de función de bombas ATPasas resulta en entrada excesiva de calcio y sodio e intercambio iónico disfuncional.
-
Endotelio coronario:
- ¿Definición?: Capa interna de células endoteliales.
- ¿Ubicación?: En arterias y capilares coronarios.
- ¿Función?: Regula vasodilatación, vasoconstricción, inflamación y coagulación.
- ¿Cambio en isquemia?: Disminuye producción de vasodilatadores (óxido nítrico) y promueve fenómenos procoagulantes e inflamatorios.
-
Microcirculación:
- ¿Definición?: Red capilar que asegura la nutrición de capas subendocárdicas.
- ¿Ubicación?: Desde arterias terminales hasta vénulas del miocardio.
- ¿Función?: Distribución eficiente de oxígeno y nutrientes.
- ¿Cambio en isquemia?: La disfunción limita aún más la perfusión, incluso si se restablece el flujo arterial principal.
⚙️ Funciones y procesos
El proceso isquémico cardíaco conlleva una serie ordenada de eventos que ocurren en lugares específicos y afectan funciones celulares y tisulares:
-
Disminución del flujo sanguíneo coronario
Definición: Reducción del aporte sanguíneo a través de arterias coronarias.
Ubicación: Segmentos arteriales afectados por obstrucción.
Efecto: Menor entrega de oxígeno y nutrientes al miocardio.
Mecanismo: Placas ateroscleróticas limitan el lumen arterial. -
Privación de oxígeno (hipoxia tisular)
Definición: Falta de oxígeno disponible para la célula.
Ubicación: Miocitos en regiones irrigadas deficientemente, especialmente subendocárdicas.
Efecto: Interrupción del metabolismo oxidativo.
Mecanismo: Disminución de la presión parcial de oxígeno y gradiente para difusión. -
Alteración de la producción de ATP mitocondrial
Definición: Reducción del ATP disponible.
Ubicación: Matriz mitocondrial del miocito.
Efecto: Imposibilidad para mantener funciones energéticas como contracción y transporte iónico.
Mecanismos:- Falta de oxígeno impide fosforilación oxidativa.
- Recurrencia a glucólisis anaerobia, menos eficiente.
- Acumulación de lactato y acidificación celular.
-
Fracaso de las bombas iónicas dependientes de ATP
Definición: Disfunción de ATPasas (Na+/K+ y Ca2+).
Ubicación: Membrana plasmática y retículo sarcoplásmico.
Efecto: Alteración de gradientes iónicos y despolarización sostenida.
Mecanismos:- Sin ATP, la bomba sodio-potasio deja de funcionar.
- Se acumula calcio intracelularmente.
- Incremento citosólico de sodio y calcio; disminución de potasio.
-
Acumulación intracelular de calcio
Definición: Elevación anómala de Ca2+ en citosol.
Ubicación: Citoplasma de miocitos.
Efecto: Activación de enzymes proteolíticas y fosfolipasas.
Mecanismos:- Entrada por canales y liberación desde retículo por desregulación.
- Degradación de proteínas, lípidos y ADN por enzimas activadas.
-
Desarrollo de acidosis intracelular
Definición: Acumulación de metabolitos ácidos (ácido láctico).
Ubicación: Citosol de miocitos afectados.
Efecto: Inhibición enzimática y daño progresivo.
Mecanismos:- Glucólisis anaerobia produce lactato.
- La caída del pH inhibe enzimas y sensibiliza el daño.
-
Compromiso de integridad de membranas y organelos
Definición: Pérdida de integridad estructural.
Ubicación: Membranas celulares y orgánulos internos.
Efecto: Liberación de enzimas lisosomales que agravan el daño.
Mecanismos:- Membranas pierden selectividad iónica y estructural.
- Degradación celular por enzimas liberadas al citoplasma y espacio extracelular.
-
Inducción de inflamación y activación procoagulante locales
Definición: Respuesta a daño tisular.
Ubicación: Microambiente isquémico.
Efecto: Reclutamiento celular inflamatorio, citocinas, riesgo trombótico.
Mecanismos:- Endotelio expresa moléculas de adhesión.
- Activación de coagulación agrava obstrucción y hipoxia.
-
Progresión hacia muerte celular (necrosis)
Definición: Destrucción irreversible del miocito.
Ubicación: Zonas con isquemia prolongada.
Efecto: Pérdida contráctil y liberación celular.
Mecanismos:- Fracaso homeostático energético e iónico supera umbral de supervivencia.
- Desintegración estructural del miocito definitiva.
🔗 Integración funcional
La fisiopatología isquémica cardíaca resulta de la interacción estructural y funcional entre sus componentes.
El inicio clásico es la formación de placas ateroscleróticas en las arterias coronarias, causando estenosis que limitan el flujo sanguíneo distal.
El miocardio demanda ATP de manera constante y depende principalmente de la fosforilación oxidativa mitocondrial para su energía.
La reducción de oxígeno interrumpe rápidamente esta fuente. Al no satisfacer las demandas:
- Disminuye abruptamente la producción de ATP.
- Fallan las bombas iónicas dependientes de ATP (Na+/K+ y Ca2+ ATPasas), aumentando Na+ y Ca2+ intracelulares.
- El exceso de calcio activa enzimas degradativas de componentes celulares esenciales.
- El retículo sarcoplásmico pierde la regulación del ciclo cálcico necesario.
- La membrana celular se vuelve permeable e inestable.
De manera simultánea, la acidosis metabólica por acumulación de lactato compromete la función miocárdica.
La inflamación local promovida por células endoteliales alteradas y mediadores químicos contribuye al deterioro progresivo y necrosis en regiones afectadas.
La consecuencia final de estos procesos interrelacionados es la pérdida irreversible de células miocárdicas en zonas con isquemia sostenida, manifestándose como áreas necróticas que comprometen la función contráctil y predisponen a insuficiencia cardíaca.
🔬 Métodos y evidencias
El conocimiento de estos mecanismos se ha obtenido mediante modelos celulares y experimentales animales, que simulan obstrucciones coronarias y permiten controlar variables como flujo y oxígeno para observar efectos progresivos en miocitos.
A nivel sistémico, se analizan marcadores bioquímicos del daño celular y cambios metabólicos, incluyendo ATP, lactato y especies reactivas de oxígeno.
La medición de gradientes iónicos mediante técnicas electroquímicas confirma la pérdida de homeostasis.
El análisis histológico muestra alteraciones estructurales, como daño en membranas celulares, fragmentación nuclear y desorganización del citoesqueleto.
Las técnicas de imagen funcional (evaluación de perfusión miocárdica) correlacionan la isquemia con compromiso funcional a nivel del tejido en tiempo real.
🩺 Puente clínico
Conocer estos mecanismos proporciona un marco para entender cómo se producen las manifestaciones clínicas de la isquemia, especialmente la pérdida progresiva de miocitos viables, que reduce la contractilidad y favorece disfunción cardíaca.
El carácter irreversible de la necrosis depende de la duración e intensidad del desequilibrio oxigeno-oferta/demanda.
Además, la actividad endotelial y microvascular explican por qué algunas regiones permanecen afectadas aún después de tratar la obstrucción coronaria principal.
La activación secuencial inflamatoria y procoagulante favorece el daño progresivo y complicaciones secundarias, contribuyendo a la evolución clínica de la enfermedad isquémica.
💎 Perlas de alto rendimiento
- Reducción del flujo coronario: La reducción del flujo coronario por aterosclerosis es el evento inicial clave en la isquemia cardíaca.
- Zona subendocárdica vulnerable: La zona subendocárdica es la región miocárdica más vulnerable a la hipoperfusión.
- Dependencia del metabolismo aeróbico: El metabolismo miocárdico depende en gran medida de la fosforilación oxidativa, lo que explica la rápida afectación al disminuir el oxígeno.
- Fallo de bombas iónicas ATP-dependientes: El fallo de las bombas iónicas ATP-dependientes conduce a desequilibrios iónicos que dañan la célula.
- Acidosis intracelular por lactato: La acidosis intracelular por acumulación de lactato debilita la función contráctil y afecta enzimas esenciales.
- Daño endotelial y microtrombosis: El daño endotelial promueve microtrombosis e inflamación, agravando la isquemia local.
- Reperfusión y especies reactivas: La reperfusión rápida puede generar especies reactivas de oxígeno que contribuyen al daño tisular adicional.
- Reversibilidad precoz: Las primeras alteraciones funcionales pueden ser reversibles si se restaura la oxigenación precozmente.
🧠 Puntos clave
- Isquemia cardíaca por aterosclerosis: La isquemia cardíaca surge principalmente por aterosclerosis coronaria que limita el aporte de oxígeno.
- Fallo mitocondrial: El fallo mitocondrial en la producción de ATP compromete funciones energéticas esenciales de la célula miocárdica.
- Sobrecarga intracelular de calcio: La sobrecarga intracelular de calcio inicia la activación de enzimas que degradan la integridad celular.
- Acidosis inducida por lactato: La acidosis inducida por lactato inhibe funciones enzimáticas críticas y disminuye la contracción miocárdica.
- Disfunción endotelial y microvascular: La disfunción endotelial y microvascular agrava la obstrucción y el daño tisular local.
- Daño isquémico dependiente del tiempo: El daño isquémico depende de la duración e intensidad del desequilibrio entre la oferta y demanda de oxígeno.
❓ Preguntas frecuentes
¿Cómo se produce la reducción de la oferta de oxígeno en el corazón?
Se produce por la obstrucción del lumen arterial coronario, principalmente debido a placas ateroscleróticas que limitan el flujo sanguíneo y la presión parcial de oxígeno en el tejido.
¿Por qué el miocardio es especialmente sensible a la isquemia comparado con otros tejidos?
Porque depende casi exclusivamente del metabolismo aeróbico mitocondrial para producir ATP y su consumo energético es elevado y constante, por lo que la falta de oxígeno afecta rápidamente su función.
¿Qué efectos directos tiene la disminución de ATP en las células miocárdicas?
El descenso del ATP impide el funcionamiento de bombas iónicas, causando acumulación intracelular de calcio y sodio, pérdida de potasio y alteración de la excitabilidad y viabilidad celular.
¿Cómo contribuye la disfunción endotelial a agravar la isquemia?
Al perder su capacidad vasodilatadora y reguladora, el endotelio favorece vasoconstricción local, adhesión de células inflamatorias y formación de microtrombos, lo que limita todavía más la perfusión tisular.
¿Qué determina que una lesión isquémica evolucione de reversible a irreversible?
El tiempo y la gravedad del déficit de oxígeno: si la célula no restaura oportunamente su homeostasis energética y estructural, se instaura la necrosis y la lesión se vuelve permanente.
¿Por qué la región subendocárdica es afectada primero en la isquemia?
Porque es la más alejada de la arteria coronaria principal, tiene mayor demanda de oxígeno y menor flujo colateral, siendo por ello más vulnerable a la hipoperfusión.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico sobre la fisiopatología isquémica cardíaca presentado en el artículo.
Nivel 1 – Básico
¿Cuál es la causa más frecuente de la reducción de la oferta de oxígeno al miocardio según el artículo?
¿Dónde se ubican las mitocondrias en las células miocárdicas según el artículo?
¿Cuál es la función principal de las células miocárdicas?
Nivel 2 – Intermedio
¿Cuál es la relación correcta entre las bombas iónicas ATP-dependientes y la isquemia cardíaca?
¿Por qué la zona subendocárdica es más vulnerable a la isquemia que otras regiones del miocardio?
¿Cuál es el papel del endotelio coronario durante la isquemia según el artículo?
Nivel 3 – Avanzado
¿Qué efecto funcional tiene la acumulación acelerada de lactato en el miocito durante la isquemia?
¿Qué secuencia describe correctamente el desarrollo de daño irreversible en la isquemia cardíaca?
¿Cómo contribuye la inflamación local al deterioro tisular en la isquemia cardíaca según el texto?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.