⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La fisiopatología del asma describe la inflamación crónica de las vías aéreas causada por interacción genética y ambiental, que induce hiperreactividad bronquial, obstrucción reversible y remodelación estructural. Esta secuencia produce síntomas respiratorios variables y fluctuantes derivados de la alteración funcional y tisular bronquial.
🧬 Concepto base
El asma es un trastorno inflamatorio crónico de las vías aéreas que provoca una barrera epitelial disfuncional, producción excesiva de moco y contracción del músculo liso bronquial. Estas alteraciones estructurales y celulares generan la obstrucción del flujo aéreo y síntomas respiratorios.
⚙️ Mecanismo clave
La exposición a alérgenos en pacientes susceptibles activa linfocitos Th2, que secretan citocinas (IL-4, IL-5, IL-13) reclutando eosinófilos y mastocitos; la liberación de mediadores induce inflamación, broncoconstricción y edema, causando obstrucción variable y remodelación progresiva.
🔗 Por qué es importante
Estos procesos determinan la severidad, reversibilidad y variabilidad clínica del asma, fundamentando el diagnóstico diferencial y la interpretación funcional de la enfermedad.
🎯 Puntos que suelen preguntarse en examen
- ¿Qué células inmunitarias predominan en la inflamación asmática?
- Mecanismos que llevan a la hiperreactividad bronquial.
- Rol del epitelio respiratorio en la patogénesis del asma.
- Efectos de las citocinas Th2 sobre el tejido bronquial.
- Características principales de la remodelación de la vía aérea.
- Factores que explican la reversibilidad variable de la obstrucción.
Palabras clave: fisiopatología del asma, inflamación bronquial, linfocitos Th2, citocinas IL-4, IL-5, IL-13, hiperreactividad bronquial, remodelación de la vía aérea, obstrucción reversible
La fisiopatología del asma explora las secuencias celulares, moleculares y tisulares que subyacen al desarrollo y la perpetuación de la enfermedad.
Examina cómo la inflamación persistente, provocada por desencadenantes ambientales en individuos con predisposición genética, desencadena una hiperreactividad bronquial y una obstrucción variable de las vías aéreas, afectando directamente la función respiratoria.
Comprender estos eventos interrelacionados permite interpretar cómo surgen los síntomas típicos y la variabilidad en la presentación clínica.
🧠 Idea central
La fisiopatología del asma detalla cómo una interacción compleja entre predisposición genética y exposición ambiental conduce a la activación sostenida de mecanismos inmunológicos.
Esta activación produce inflamación de la vía aérea, hiperreactividad y episodios de obstrucción bronquial, generalmente reversibles.
Estos procesos generan síntomas respiratorios episódicos y variables debido a la alteración funcional y estructural de las vías respiratorias.
El núcleo fisiopatológico del asma es la inflamación crónica de las vías aéreas acompañada de hiperrespuesta bronquial y remodelación progresiva en algunos casos.
🌍 Contexto y alcance
El estudio moderno del asma aborda el fenómeno en varios niveles biológicos:
- Nivel molecular: Incluye señalización de citocinas, interacción de receptores inmunológicos, activación de vías intracelulares en células inflamatorias y producción de mediadores bioactivos.
- Nivel celular: Se examina la participación de linfocitos T helper tipo 2 (Th2), eosinófilos, mastocitos y células epiteliales.
- Nivel tisular: Se investigan cambios en la arquitectura bronquial, engrosamiento de la membrana basal, alteración del epitelio y proliferación de glándulas de moco.
- Nivel orgánico-sistémico: Se analiza cómo estos procesos locales afectan el funcionamiento global del sistema respiratorio y contribuyen a la presentación sintomática.
Esta perspectiva integral permite entender cómo la variabilidad en la génesis y perpetuación de la inflamación explica la heterogeneidad clínica entre quienes presentan asma.
🧬 Estructuras clave
El asma afecta principalmente las vías aéreas inferiores, cuya arquitectura determina su reacción ante estímulos externos e internos.
A continuación se detallan los principales componentes afectados:
| Estructura | Función relevante en asma | Alteración típica |
|---|---|---|
| Epitelio respiratorio | Barrera física, detección de agentes exógenos, secreción de moco y mediadores inflamatorios | Lesión, disrupción de uniones intercelulares, aumento de permeabilidad y descamación |
| Músculo liso bronquial | Regulación dinámica del diámetro de la luz bronquial por contracción y relajación | Hiperplasia e hipertrofia del músculo, aumento de sensibilidad contráctil (hiperreactividad) |
| Células inmunitarias (mastocitos, eosinófilos, linfocitos T) | Orquestación y perpetuación de la inflamación bronquial | Infiltración en la mucosa, activación sostenida, liberación de mediadores proinflamatorios |
| Glándulas y células caliciformes | Producción y secreción de moco que protege el epitelio y atrapa partículas | Hiperplasia, aumento de secreción y acumulación de moco viscoso |
| Vasos sanguíneos bronquiales | Transporte de células inflamatorias y entrega de nutrientes y señales | Dilatación, edema de la submucosa, incremento en la permeabilidad vascular |
| Tejido conectivo subepitelial | Sostén estructural de la vía aérea | Engrosamiento de la membrana basal y fibrosis subepitelial |
- Epitelio respiratorio: Capa celular que tapiza internamente los bronquios y bronquiolos, actuando como barrera ante el ambiente.
- Ubicación: Desde la tráquea hasta los bronquiolos pequeños.
- Producción: Secreta factores que modulan la inflamación y protege a los tejidos subyacentes.
- Funcionamiento: Su daño facilita la penetración de alérgenos e irritantes, activando células inmunes subyacentes.
- Músculo liso bronquial: Anillos y hebras musculares que rodean la vía aérea.
- Ubicación: Bajo la mucosa bronquial y bronquiolar.
- Función: Regula el calibre de la vía aérea mediante contracción y relajación rápidas.
- Alteración: La sensibilización inflamatoria provoca contracciones intensas ante estímulos mínimos.
- Glándulas mucosas y células caliciformes: Estructuras secretoras distribuidas en la mucosa respiratoria.
- Distribución: Dispersas en el epitelio respiratorio.
- Producción: Incrementan la secreción mucosa; en asma, existe hipersecreción patológica.
- Consecuencia: La hiperactividad obstruye la luz bronquial por aumento del volumen y viscosidad del moco.
⚙️ Funciones y procesos
La respuesta fisiopatológica del asma se compone de varios procesos principales que interactúan en secuencia y retroalimentación.
Cada mecanismo se desarrolla como respuesta a la activación inmunitaria inicial en un individuo predispuesto y tras exposición ambiental.
1. Sensibilización y activación inmunitaria inicial
- Definición: Proceso en el cual el sistema inmune reconoce un agente ambiental (alérgeno o irritante) y genera una respuesta inmunitaria.
- Localización: Mucosa de la vía aérea y ganglios linfáticos asociados.
- Resultados: Activación de linfocitos T CD4+ del subtipo Th2, que inicia y amplifica la cascada inflamatoria.
- Etapas:
- Las células presentadoras de antígeno (CPA) capturan y procesan el alérgeno.
- CPA migran a ganglios linfáticos donde presentan el antígeno a linfocitos T naïve.
- En individuos susceptibles, predominan linfocitos Th2.
- Th2 secretan citocinas (IL-4, IL-5, IL-13) que atraen y activan eosinófilos y mastocitos y favorecen la producción de IgE por linfocitos B.
2. Activación y liberación de mediadores inflamatorios
- Definición: Liberación de proteínas y moléculas bioactivas que regulan vasodilatación, contracción muscular y reclutamiento celular.
- Localización: Mucosa bronquial y espacio intersticial adyacente.
- Función: Amplifica la inflamación local y contribuye a la inflamación sistémica.
- Etapas:
- Mastocitos sensibilizados liberan histamina, leucotrienos y prostaglandinas tras reexposición al antígeno.
- Histamina y leucotrienos inducen contracción brusca del músculo liso (broncoconstricción temprana).
- IL-5 atrae y activa eosinófilos, que liberan proteínas citotóxicas perpetuando daño epitelial.
- Otros mediadores aumentan permeabilidad vascular, facilitando edema y entrada adicional de células inflamatorias.
3. Hiperreactividad bronquial
- Definición: Capacidad aumentada e inestable de las vías aéreas para contraerse excesivamente ante estímulos que no afectan a sujetos sanos.
- Localización predominante: Bronquios de pequeño y mediano calibre.
- Consecuencia: Obstrucción variable y transitoria del flujo aéreo.
- Proceso:
- Músculo liso bronquial sensibilizado responde con contracciones intensas ante irritantes menores (aire frío, ejercicio, humo).
- Esta contracción reduce reversiblemente el calibre bronquial.
- La hiperreactividad se incrementa con la persistencia de inflamación y remodelación progresiva.
4. Remodelación de la vía aérea
- Definición: Cambios crónicos estructurales en la arquitectura bronquial.
- Localización: Capas epitelial, muscular y submucosa de la vía aérea.
- Efectos: Alteraciones permanentes que reducen la reversibilidad de la obstrucción bronquial.
- Proceso:
- Daño epitelial crónico estimula proliferación de fibroblastos y depósito de matriz extracelular, engrosando la membrana basal.
- Hipertrofia e hiperplasia del músculo liso.
- Proliferación de glándulas y células caliciformes incrementando la producción de moco.
- Estos cambios disminuyen la distensibilidad y aumentan la resistencia bronquial, dificultando la reversibilidad.
5. Obstrucción episódica y reversible del flujo aéreo
- Definición: Disminución transitoria del diámetro de la vía aérea, usualmente reversible espontáneamente o tras eliminar el estímulo.
- Localización: Bronquios y bronquiolos afectados por inflamación y contracción muscular.
- Manifestación: Disminución del flujo inspiratorio y espiratorio, produciendo sibilancias, disnea y tos.
- Etapas:
- Edema submucoso, contracción muscular y moco denso se conjugan para estrechar la luz bronquial.
- La reducción luminal dificulta el paso del aire, especialmente en espiración.
- Con la resolución del estímulo inflamatorio, la obstrucción puede revertir parcial o totalmente.
🔗 Integración funcional
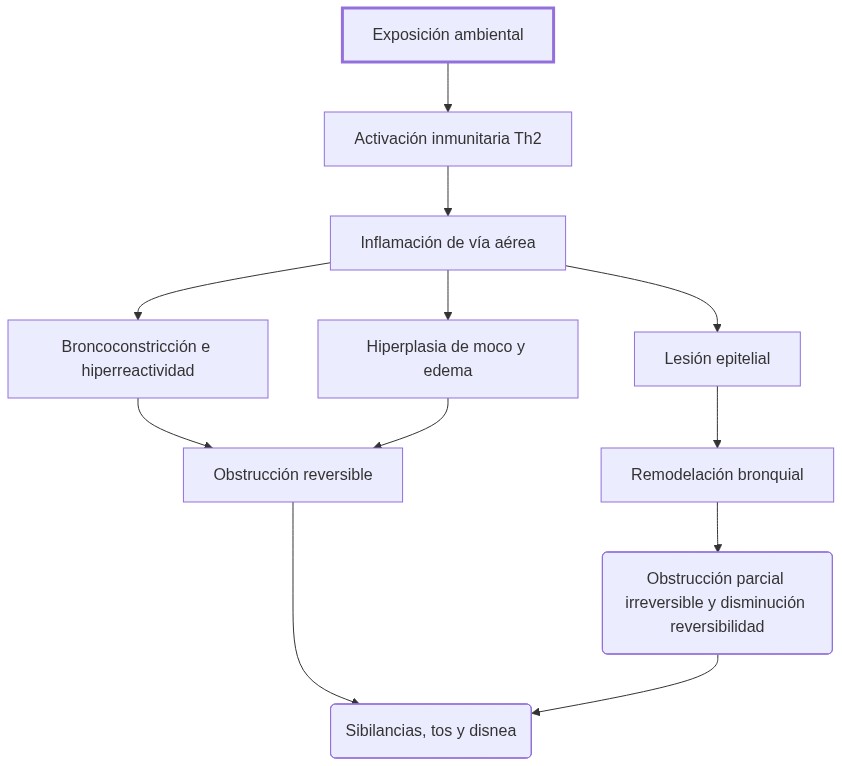
La fisiopatología del asma se organiza como una secuencia de eventos mantenidos por la interacción entre células inmunitarias, estructuras tisulares y factores ambientales.
Esta interacción determina la expresión clínica y la variabilidad en la severidad y reversibilidad.
- Un estímulo ambiental (alérgeno o irritante) provoca la sensibilización inmunitaria en el epitelio y ganglios linfáticos asociados.
- La respuesta Th2 dominante induce la liberación de citocinas proinflamatorias, promoviendo la infiltración de eosinófilos y mastocitos en la mucosa bronquial.
- Los mediadores inflamatorios actúan sobre el músculo liso bronquial, incrementando la reactividad y contribuyendo a la obstrucción reversible.
- El epitelio bronquial lesionado pierde su capacidad protectora y reguladora de inflamación, favoreciendo recurrencia de crisis.
- La inflamación persistente induce remodelación estructural, con hipertrofia muscular, fibrosis y proliferación glandular, condicionando obstrucción parcial irreversible en etapas avanzadas.
La función normal de la vía aérea depende del equilibrio entre mecanismos protectores y procesos inflamatorios alterados por predisposición genética y ambiente.
La exacerbación sintomática es la consecuencia observable de esta interacción compleja.
🔬 Métodos y evidencias
Los mecanismos fisiopatológicos del asma han sido identificados mediante diversas técnicas:
- Histología: Biopsias bronquiales muestran infiltración eosinofílica, engrosamiento de membrana basal y alteraciones epiteliales.
- Inmunohistoquímica: Permite localizar y cuantificar citocinas, receptores y células inmunitarias específicas en tejido respiratorio.
- Citometría de flujo y técnicas celulares: Perfilan linfocitos, eosinófilos y mastocitos en lavados broncoalveolares y esputo.
- Análisis bioquímicos: Miden mediadores inflamatorios (e.g., histamina, leucotrienos, interleucinas) en sangre y secreciones respiratorias.
- Pruebas funcionales respiratorias: Evalúan alteraciones y reversibilidad del flujo aéreo, correlacionando gravedad funcional con procesos inflamatorios y estructurales.
La combinación de estas metodologías relaciona hallazgos moleculares y celulares con la presentación clínica del asma, reflejando su complejidad biológica y multifactorialidad.
🩺 Puente clínico
El análisis fisiopatológico explica la génesis y variabilidad de los síntomas respiratorios en la clínica.
La inflamación crónica con hiperreactividad bronquial condiciona que, tras exposición a un desencadenante (como un alérgeno), se produzca una obstrucción reversible episódica, mediada por contracción muscular y edema.
En algunos pacientes, la remodelación progresiva vuelve la obstrucción menos reversible, explicando diferencias en la gravedad y evolución clínica del asma.
La interacción entre predisposición genética y exposición ambiental conduce a una expresión clínica variable, bajo la misma influencia desencadenante.
Esta comprensión fundamenta la heterogeneidad sintomática observada en la enfermedad.
💎 Perlas de alto rendimiento
- Predominancia de linfocitos Th2: La predominancia de linfocitos Th2 y la producción de interleucinas IL-4, IL-5 e IL-13 sustentan la respuesta inflamatoria característica del asma.
- Lesión epitelial: La lesión epitelial favorece la penetración de alérgenos y la amplificación de la respuesta inmune y la hiperreactividad bronquial.
- Obstrucción reversible: La obstrucción en el asma suele ser reversible pero puede volverse permanente por remodelación estructural.
- Hiperplasia muscular: El músculo liso bronquial presenta hiperplasia e hipertrofia, aumentando la propensión a broncoconstricciones ante estímulos menores.
- Rol de eosinófilos: Los eosinófilos liberan proteínas citotóxicas que perpetúan daño epitelial e inflamación.
- Moco hipersecreto: La hipersecreción y viscosidad del moco contribuyen a la formación de tapones luminales, agravando la obstrucción.
- Inflamación vascular: La infiltración vascular y edema submucoso intensifican la inflamación y la limitación del flujo aéreo.
- Equilibrio inmunitario: El equilibrio entre mecanismos inmunitarios, lesión epitelial y remodelación define la anatomía funcional alterada en el asma.
🧠 Puntos clave
- Inflamación crónica: El asma se caracteriza por inflamación crónica y episodios recurrentes de obstrucción reversible de las vías aéreas.
- Hiperreactividad bronquial: La hiperreactividad bronquial refleja respuesta exacerbada del músculo liso ante estímulos relativamente inocuos.
- Interacción genética-ambiental: Predisposición genética y factores ambientales interactúan para iniciar y sostener procesos inflamatorios en la vía aérea.
- Remodelación bronquial: La remodelación bronquial crónica altera la estructura, limitando la reversibilidad y modificando la expresión clínica.
- Función epitelial: El epitelio respiratorio es clave para mantener la barrera y regular la inflamación; su daño facilita la penetración de agentes nocivos.
- Variabilidad funcional: La variabilidad funcional y clínica del asma es resultado de la interacción compleja entre inflamación activa y cambios estructurales.
❓ Preguntas frecuentes
¿Cómo se inicia la respuesta inflamatoria en el asma?
Una exposición a alérgenos o irritantes en individuos susceptibles induce activación de células presentadoras de antígeno, que promueven la diferenciación de linfocitos Th2 y la liberación de citocinas, reclutando células inflamatorias en la mucosa bronquial.
¿Por qué la obstrucción bronquial es mayormente reversible en el asma?
Está mediada por contracción muscular y edema, procesos que pueden resolverse tras eliminar el estímulo y reducir la inflamación, aunque la remodelación crónica reduce esta reversibilidad.
¿Cuál es el papel del epitelio respiratorio en el asma?
Actúa como barrera inicial y sensor de agentes nocivos; su daño permite la entrada aumentada de alérgenos e irritantes, exacerbando la respuesta inmunitaria.
¿Qué es la remodelación de la vía aérea y qué la causa?
Es el conjunto de cambios estructurales que incluye fibrosis, hipertrofia muscular y proliferación glandular, originados por inflamación crónica y ciclos repetidos de daño y reparación.
¿Qué factores explican la variabilidad clínica del asma?
La interacción entre factores genéticos, tipo y cantidad de exposiciones ambientales, y grado de remodelación estructural en cada individuo determina la heterogeneidad sintomática.
¿Qué función tienen los eosinófilos en el asma?
Son células efectoras que, atraídas por citocinas como IL-5, liberan mediadores citotóxicos que dañan epitelio y perpetúan inflamación y hiperreactividad bronquial.
¿Cómo influye el moco en la fisiopatología del asma?
Su producción excesiva y alteración en la viscosidad contribuyen a formar tapones obstructivos que dificultan la depuración y agravan la obstrucción aérea.
¿Por qué la función pulmonar varía en el tiempo en asmáticos?
Porque la obstrucción es causada por procesos reversibles como broncoconstricción y edema, los síntomas y flujo aéreo pueden fluctuar de forma rápida según la exposición y resolución inflamatoria.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico sobre la fisiopatología del asma presentado en el artículo.
Nivel 1 – Básico
¿Cuál es la función principal del epitelio respiratorio en las vías aéreas según el artículo?
¿Qué caracteriza la hiperreactividad bronquial en el asma?
Según el texto, ¿qué efecto tiene la remodelación de la vía aérea en el asma?
Nivel 2 – Intermedio
¿Cuál de las siguientes relaciones estructura-función es correcta según el artículo?
¿Cómo se describe la activación inmunitaria inicial en la fisiopatología del asma?
¿Cuál es la consecuencia funcional de la lesión epitelial en el asma según el texto?
Nivel 3 – Avanzado
¿Qué secuencia correcta de pasos describe la sensibilización inmunitaria inicial en el asma?
Si la inflamación bronquial persiste, ¿qué implicaciones funcionales y estructurales se desencadenan según el artículo?
¿Cuál es la consecuencia directa de la activación y liberación de mediadores inflamatorios (histamina, leucotrienos, IL-5) en las vías aéreas?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.