⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
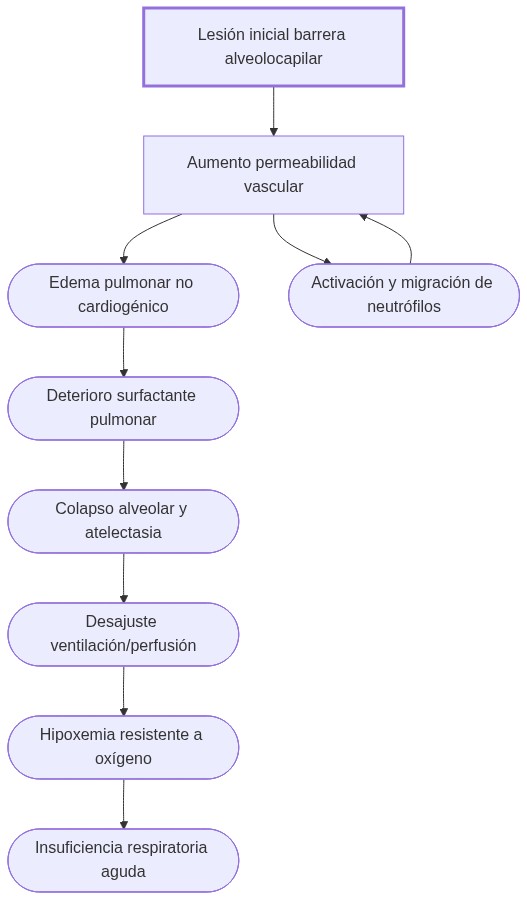
La fisiopatología del síndrome implica daño agudo a la barrera alvéolo-capilar que causa aumento de la permeabilidad vascular, edema pulmonar no cardiogénico, pérdida de surfactante y colapso alveolar, generando hipoxemia refractaria y disfunción pulmonar grave.
🧬 Concepto base
Daño tisular en parénquima pulmonar que altera la barrera alveolo-capilar y la función de neumocitos tipo I y II, comprometiendo el intercambio gaseoso y la producción de surfactante.
⚙️ Mecanismo clave
Lesión celular e inflamación aumentan la permeabilidad vascular, permiten filtración proteica al espacio alveolar, inducen edema y pérdida de surfactante, provocando atelectasia y desajuste ventilación/perfusión.
🔗 Por qué es importante
Produce insuficiencia respiratoria aguda con hipoxemia resistente, afectando la oxigenación sistémica y perpetuando daño multiorgánico.
🎯 Puntos que suelen preguntarse en examen
- ¿Qué estructura sufre daño principal en el SDRA?
- ¿Cómo afecta el edema pulmonar no cardiogénico la función respiratoria?
- ¿Cuál es el papel del surfactante y su alteración en la fisiopatología?
- ¿Por qué la hipoxemia persiste a pesar de oxígeno suplementario?
- ¿Qué células contribuyen a perpetuar la lesión mediante inflamación?
- ¿Qué hallazgos histopatológicos son característicos del síndrome?
Palabras clave: fisiopatología del síndrome, barrera alvéolo-capilar, edema pulmonar, surfactante, inflamación pulmonar, hipoxemia, neutrófilos, membranas hialinas
Comprender la fisiopatología del síndrome resulta esencial para analizar cómo los procesos biológicos normales se ven interrumpidos, repercutiendo en la función orgánica y alterando la homeostasis. En este artículo, se aborda paso a paso la fisiopatología del síndrome de distrés respiratorio agudo (SDRA), enfatizando los cambios estructurales y funcionales pulmonares que subyacen a su manifestación clínica y guiando el razonamiento sobre sus mecanismos esenciales.
🧠 Idea central
La fisiopatología del síndrome de distrés respiratorio agudo (SDRA) afecta principalmente el sistema respiratorio, con repercusiones sistémicas debidas a la alteración aguda y severa del intercambio gaseoso en los pulmones.
Esta condición es causada por daño agudo, ya sea por agentes directos (por ejemplo, neumonía, aspiración) o indirectos (sepsis, trauma), que inicia una cascada de procesos moleculares y celulares que comprometen la integridad estructural y funcional del tejido pulmonar.
El núcleo fisiopatológico radica en la disrupción de la barrera alvéolo-capilar, ocasionando un aumento de la permeabilidad vascular pulmonar.
Esto permite la entrada de proteínas plasmáticas y líquidos hacia los alvéolos, produciendo edema pulmonar no cardiogénico, que deteriora el intercambio de oxígeno y dióxido de carbono, precipitando hipoxemia e insuficiencia respiratoria aguda.
🌍 Contexto y alcance
El estudio de la fisiopatología del SDRA abarca cambios a escala celular, tisular y orgánica, situándose principalmente en el parénquima pulmonar y los compartimentos vasculares pulmonares.
A nivel celular, involucra tanto células epiteliales (neumocitos tipo I y II) como células endoteliales de los capilares pulmonares.
La alteración de estas células inicia una respuesta inflamatoria desproporcionada, mediada por la activación de leucocitos y la liberación de mediadores proinflamatorios.
Estas señales, además de reclutar más células inmunitarias, inducen daño adicional a las membranas celulares y aumentan la permeabilidad de la barrera alvéolo-capilar, profundizando la lesión.
A nivel tisular y orgánico, el SDRA se traduce en infiltración difusa del parénquima pulmonar, con formación de membranas hialinas (acúmulo de proteínas, fibrina y restos celulares) que recubren la superficie alveolar y dificultan aún más la función pulmonar.
Así, los procesos fisiopatológicos superan la escala local y condicionan la función sistémica, especialmente el transporte global de oxígeno.
🧬 Estructuras clave
La comprensión de la fisiopatología del SDRA requiere identificar las estructuras pulmonares más afectadas y su rol funcional en estado normal y alterado. La interacción entre alvéolos, capilares, células epiteliales y endoteliales determina el curso de la lesión y sus consecuencias fisiológicas.
| Estructura | Función normal | Alteración fisiopatológica |
|---|---|---|
| Barrera alvéolo-capilar | ¿Qué permite? Permite el intercambio selectivo de oxígeno y dióxido de carbono entre el aire y la sangre, preservando la impermeabilidad a proteínas plasmáticas y líquidos. | ¿Qué ocurre si se altera? Daño y aumento de la permeabilidad, generando edema pulmonar por paso de líquidos y proteínas al espacio alveolar. |
| Neumocitos tipo I | ¿Qué es? Recubren la mayor parte de la superficie alveolar y median el intercambio gaseoso eficiente. | ¿Qué produce? Destrucción o alteración que limita el área disponible para el intercambio y facilita el paso de líquidos al alvéolo. |
| Neumocitos tipo II | ¿Qué es? Secretan surfactante pulmonar, manteniendo la tensión superficial y previniendo el colapso alveolar. | ¿Qué efecto tiene la alteración? Daño o disfunción que disminuye la producción de surfactante, aumentando la atelectasia y dificultando la ventilación. |
| Células endoteliales capilares pulmonares | ¿Qué función tienen? Mantienen la integridad de la barrera vascular y regulan el tránsito de solutos y células. | ¿Qué sucede si se dañan? Daño estructural por mediadores inflamatorios que incrementan la permeabilidad y contribuyen al edema pulmonar. |
| Espacio intersticial pulmonar | ¿Qué es? Espacio entre alvéolos y capilares que regula el equilibrio de líquidos y la integridad tisular. | ¿Qué provoca la alteración? Acumulación de líquido y engrosamiento que amplifica la disfunción del intercambio gaseoso. |
| Surfactante pulmonar | ¿Qué función tiene? Reduce la tensión superficial alveolar, estabilizando los alvéolos durante la respiración. | ¿Qué efecto tiene su reducción? Reducción o inactivación que contribuye al colapso alveolar y a la disminución de la compliancia pulmonar. |
| Leucocitos polimorfonucleares (neutrófilos) | ¿Cuál es su papel? Respuesta defensiva ante daño o infección pulmonar. | ¿Cómo afectan la fisiopatología? Activación excesiva que libera enzimas y radicales libres, perpetuando el daño pulmonar y agravando la inflamación. |
⚙️ Funciones y procesos fisiopatológicos
Los mecanismos que caracterizan la fisiopatología del SDRA se desarrollan mediante una secuencia estereotipada de eventos que afectan el tejido pulmonar e involucran múltiples células e interacciones dinámicas:
-
Daño inicial a la barrera alvéolo-capilar:
- Definición: La barrera está formada por las membranas del endotelio capilar y el epitelio alveolar.
- Localización: En la microunidad funcional pulmonar, en cada alvéolo y sus capilares adyacentes.
- Función: Controla el traspaso de gases y minimiza la filtración de líquidos.
- Mecanismo: El daño causado por agentes infecciosos, tóxicos o inflamación sistémica altera la integridad, aumenta la permeabilidad y permite el paso anómalo de plasma y proteínas al espacio alveolar.
-
Aumento del edema pulmonar no cardiogénico:
- Definición: Acúmulo de líquido con alto contenido proteico dentro de los alvéolos.
- Área afectada: Espacio alveolar y el intersticio pulmonar.
- Consecuencias: Disminución del volumen alveolar funcional y deterioro del intercambio gaseoso.
- Fisiopatología: El líquido que atraviesa la barrera dañada genera edema, impidiendo la adecuada oxigenación y causando hipoxemia.
-
Deterioro del surfactante pulmonar:
- Definición: Compuesto lipoproteico producido por neumocitos tipo II, esencial para reducir la tensión superficial alveolar.
- Localización: Superficie interna de los alvéolos.
- Importancia: Mantiene los alvéolos abiertos durante la respiración, facilitando la oxigenación.
- Alteración: El daño a neumocitos tipo II y la inactivación del surfactante disminuyen su cantidad y función, favoreciendo el colapso alveolar (atelectasia) y aumentando la rigidez pulmonar.
-
Inflamación pulmonar aguda y activación leucocitaria:
- Definición: Respuesta celular exagerada frente a lesión tisular.
- Localización: Tejido pulmonar, especialmente en espacios vasculares y alveolares.
- Producción: Liberación de mediadores como citoquinas, proteasas y especies reactivas de oxígeno.
- Consecuencias: Migración e infiltración de neutrófilos que liberan sustancias tóxicas, incrementan el daño tisular, perpetúan la disfunción de la barrera y promueven la acumulación de líquido y proteínas.
-
Alteraciones en la ventilación/perfusión (V/Q):
- Definición: Desajuste entre la cantidad de aire que llega a los alvéolos y la sangre que pasa por los capilares pulmonares.
- Localización: Zonas del parénquima pulmonar afectadas por edema y colapso alveolar.
- Consecuencias: Dificultad para oxigenar la sangre, con hipoxemia persistente a pesar de oxígeno suplementario.
- Mecanismo: Alvéolos colapsados o llenos de líquido impiden el intercambio gaseoso, mientras que la sangre sigue perfundiendo esas áreas, generando cortocircuitos intrapulmonares funcionales.
-
Formación de membranas hialinas:
- Definición: Acúmulo de material proteináceo y restos celulares en la luz alveolar.
- Localización: Recubren la superficie de los alvéolos dañados.
- Consecuencia: Impide la difusión adecuada de gases y perpetúa el deterioro funcional pulmonar.
- Origen: Producto de la exudación y muerte celular, dificultando irreversiblemente el intercambio gaseoso.
🔗 Integración funcional de la fisiopatología del síndrome
El SDRA ejemplifica cómo una lesión aguda en el tejido pulmonar desencadena una cascada de alteraciones interdependientes. El proceso comienza con una injuria, ya sea directa (aspiración, neumonía) o indirecta (sepsis, traumatismo), que altera la función celular y tisular, activando una respuesta inflamatoria robusta.
Esta inflamación, mediada por la activación de neutrófilos y la liberación de mediadores, conduce a:
- Daño estructural de la barrera alvéolo-capilar
- Aumento de la permeabilidad vascular pulmonar
- Formación de edema alveolar proteico
- Alteración e inactivación del surfactante pulmonar
- Colapso alveolar y atelectasia
- Desajuste ventilación/perfusión
- Hipoxemia resistente a oxigenoterapia
Estos procesos alteran tanto la microarquitectura pulmonar como la mecánica respiratoria global, resultando en disminución de la capacidad pulmonar total y de la compliancia. Si la función respiratoria disminuye suficientemente, puede producirse insuficiencia respiratoria aguda que compromete la oxigenación tisular en todo el organismo.
Además, los fenómenos fisiopatológicos no solo afectan al pulmón, sino que mantienen un efecto en cascada, agravando la disfunción por hipoxia mantenida e inflamación sistémica, lo que puede contribuir al deterioro multiorgánico.
🔬 Métodos y evidencias para comprender la fisiopatología
El abordaje de la fisiopatología del SDRA combina técnicas que permiten observar tanto las alteraciones morfológicas como funcionales del pulmón afectado:
-
Microscopía pulmonar:
- Permite: Identificar daño celular, pérdida de la integridad de la barrera alvéolo-capilar y la presencia de membranas hialinas.
- Uso: Examen histopatológico de muestras pulmonares que evidencia edema alveolar, daño en neumocitos y engrosamiento del intersticio.
-
Análisis bioquímico de líquidos pulmonares:
- Revela: Composición proteica del edema alveolar, indicativa de un proceso no cardiogénico.
- Interpretación: Un alto contenido proteico sugiere daño a la barrera alvéolo-capilar, diferenciándolo de edemas de origen cardiaco.
-
Pruebas funcionales respiratorias:
- Demuestran: Reducción grave de la compliancia pulmonar, aumento de la derivación intrapulmonar y alteración de la relación ventilación/perfusión.
- Implicancia: El deterioro funcional se correlaciona con la severidad del daño estructural observado en los tejidos.
Estas herramientas permiten correlacionar hallazgos anatómicos con alteraciones fisiológicas, aportando evidencia sólida sobre los mecanismos que llevan a la insuficiencia respiratoria en el SDRA.
🩺 Puente clínico: conexión entre fisiopatología y manifestaciones clínicas
El conocimiento fisiopatológico facilita entender por qué el SDRA se manifiesta como insuficiencia respiratoria aguda con hipoxemia persistente y opacidades pulmonares bilaterales.
La dificultad respiratoria deriva directamente del edema alveolar causado por daño en la barrera alvéolo-capilar, la pérdida de surfactante y el colapso alveolar, así como el desajuste ventilación/perfusión.
Científicamente, la presencia de líquido proteico en los alvéolos limita el paso de oxígeno, y la hipoxemia refractaria se explica por la existencia de shunts pulmonares: áreas perfundidas pero no ventiladas. Esto explica el cuadro clínico característico del síndrome.
Por tanto, la fisiopatología actúa como una herramienta clave para interpretar adecuadamente signos, síntomas y evolución clínica, promoviendo un enfoque integrador y racional.
💎 Perlas de alto rendimiento
- Daño inicial en la barrera alvéolo-capilar: es el evento esencial que desencadena el edema pulmonar no cardiogénico en el SDRA.
- Activación y migración excesiva de neutrófilos: perpetúa la lesión pulmonar mediante liberación de mediadores tóxicos.
- Disminución o inactivación del surfactante: contribuye al colapso alveolar y a la rigidez pulmonar.
- Desequilibrio ventilación/perfusión: genera hipoxemia difícil de corregir con oxígeno suplementario.
- Membranas hialinas: representan daño tisular grave, asociado a deterioro irreversible en la difusión gaseosa.
- Progresión de la fisiopatología del SDRA: desde una fase aguda de edema hasta posibles secuelas fibróticas en etapas avanzadas.
- Diferenciación del edema pulmonar cardiogénico y no cardiogénico: requiere evaluar el mecanismo y la composición del líquido alveolar.
- Evaluación de la permeabilidad vascular pulmonar: es clave para comprender la magnitud del daño en el síndrome.
🧠 Puntos clave
- Daño agudo a la barrera alvéolo-capilar: permite el paso anómalo de líquidos y proteínas al espacio alveolar.
- Disfunción de neumocitos tipo I y II: afecta el intercambio gaseoso y la producción de surfactante pulmonar.
- Edema pulmonar no cardiogénico: reduce el volumen de aire funcional, dificultando la oxigenación.
- Activación exagerada de leucocitos: amplifica la lesión y sostiene la inflamación pulmonar.
- Desajuste ventilación/perfusión: es la causa principal de la hipoxemia persistente característica del SDRA.
- Cambios anatómicos observados en microscopía: correlacionan con las alteraciones funcionales y clínicas del síndrome.
❓ Preguntas frecuentes
¿Qué desencadena la lesión inicial en la fisiopatología del SDRA?
La lesión puede ser causada por agresores directos al pulmón, como neumonía o aspiración, o indirectos, como sepsis o trauma, que originan la ruptura de la barrera alvéolo-capilar e inician la cascada inflamatoria.
¿Por qué la presencia de edema pulmonar dificulta el intercambio de oxígeno?
El líquido con alto contenido proteico en los alvéolos genera una barrera física que limita la difusión de gases, reduciendo la eficacia del intercambio y contribuyendo a la hipoxemia.
¿Cuál es el papel del surfactante pulmonar en el SDRA?
El surfactante reduce la tensión superficial alveolar y mantiene los alvéolos abiertos; su disfunción o pérdida aumenta la tendencia al colapso alveolar y dificulta la ventilación efectiva.
¿Cómo contribuye la inflamación al daño pulmonar agudo?
La respuesta inflamatoria intensa recluta leucocitos que liberan enzimas y radicales libres, causando daño adicional a las células pulmonares y agravando la alteración de la barrera alveolo-capilar.
¿Por qué la hipoxemia en el SDRA no responde bien a la oxigenoterapia convencional?
Debido a la existencia de un desequilibrio ventilación/perfusión con alvéolos colapsados o llenos de líquido, algunas regiones del pulmón permanecen perfundidas pero no ventiladas, limitando la eficacia del oxígeno suplementario.
¿Qué hallazgos estructurales caracterizan al SDRA en el análisis histopatológico?
Se observan daño difuso de neumocitos, edema intersticial, formación de membranas hialinas y pérdida de arquitectura alveolar, reflejando la gravedad de la lesión pulmonar.
¿Cómo afecta el SDRA a la función respiratoria sistémica?
Al comprometer la oxigenación y el volumen pulmonar funcional, el SDRA reduce la oxigenación tisular general y puede inducir disfunción orgánica secundaria por hipoxia.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión de los mecanismos biológicos y fisiopatológicos del síndrome de distrés respiratorio agudo (SDRA) explicados en el artículo.
Nivel 1 – Básico
¿Cuál es la función normal de la barrera alvéolo-capilar en el pulmón?
¿Qué función tiene el surfactante pulmonar producido por neumocitos tipo II?
¿Cuál es la principal consecuencia del aumento de permeabilidad en la barrera alvéolo-capilar en SDRA?
Nivel 2 – Intermedio
Según el artículo, ¿qué relación es correcta entre el daño a neumocitos tipo II y la función pulmonar en SDRA?
¿Cuál es la función y alteración causal de las células endoteliales capilares pulmonares en SDRA?
En el contexto del SDRA, ¿qué caracteriza el desajuste ventilación/perfusión según el artículo?
Nivel 3 – Avanzado
Si la barrera alvéolo-capilar aumenta su permeabilidad en SDRA, ¿qué secuencia de eventos fisiopatológicos ocurre según el artículo?
¿Cómo contribuye la activación excesiva de neutrófilos al deterioro pulmonar en SDRA?
¿Cuál es la consecuencia sistémica del deterioro respiratorio causado por el SDRA mencionada en el texto?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.