⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
El manejo de la enfermedad crítica implica entender la desregulación aguda multisistémica que afecta órganos vitales, endotelio y sistemas inmunitarios, desencadenando fallo progresivo. La combinación de inflamación exacerbada, disfunción endotelial y estrés metabólico celular interrumpe la homeostasis y la perfusión, agravando la falla orgánica.
🧬 Concepto base
Enfermedad crítica es un estado de disfunción aguda multisistémica que altera órganos vitales, células endoteliales e inmunitarias. Su función principal abarca mantener la integridad vascular, defensa inmunológica y metabolismo celular.
⚙️ Mecanismo clave
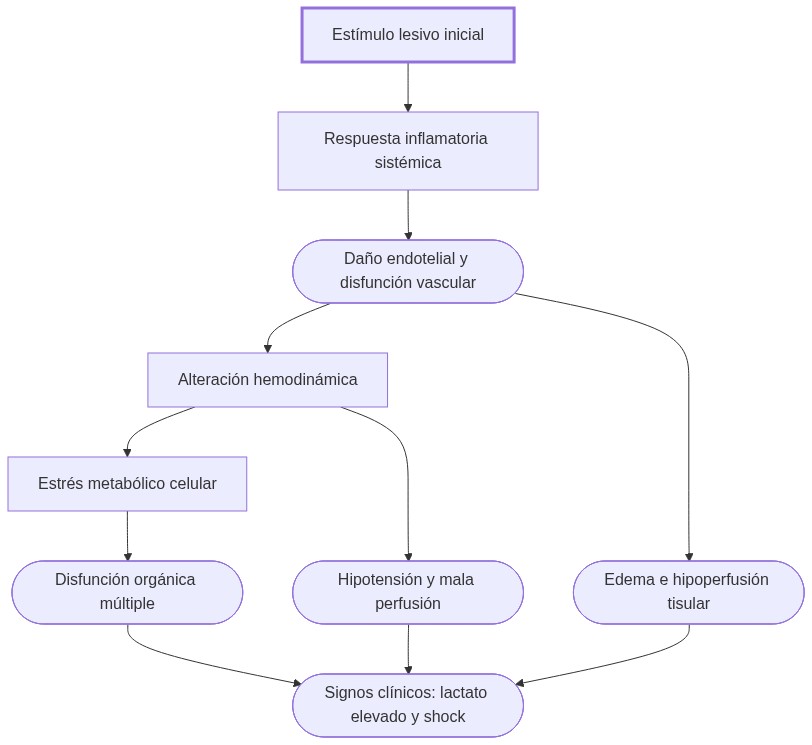
Un estímulo lesivo activa inflamación sistémica con liberación de citocinas; esto daña el endotelio, aumenta permeabilidad y forma microtrombos, generando hipoperfusión que causa estrés metabólico y falla mitocondrial, perpetuando lesión celular y disfunción orgánica múltiple.
🔗 Por qué es importante
La pérdida de integración funcional multiplica la descompensación sistémica, dificultando la recuperación y aumentando el riesgo de colapso orgánico irreversible.
🎯 Puntos que suelen preguntarse en examen
- Definición fisiológica de enfermedad crítica y su impacto multisistémico
- Rol del endotelio en la regulación vascular y consecuencias de su daño
- Procesos y fases de la respuesta inflamatoria sistémica
- Mecanismo de producción y repercusión del lactato en estrés metabólico
- Implicancia del sistema nervioso autónomo en la compensación hemodinámica
- Mecanismos biológicos que conducen a disfunción orgánica múltiple
Palabras clave: manejo de la enfermedad crítica, inflamación sistémica, disfunción endotelial, estrés metabólico celular, disfunción orgánica múltiple, perfusión tisular, sistema inmunitario innato, sistema nervioso autónomo
El manejo de la enfermedad crítica exige comprender minuciosamente los mecanismos fisiológicos y fisiopatológicos que sostienen e interrumpen la homeostasis y las funciones vitales. Este conocimiento permite analizar cómo los sistemas corporales pierden su integración y anticipar los desenlaces biológicos durante el deterioro agudo, aportando un marco funcional esencial para el razonamiento biomédico.
🧠 Idea central
La enfermedad crítica corresponde a una etapa de compromiso fisiológico extremo donde uno o más sistemas vitales experimentan desregulación aguda, amenazando la supervivencia.
Este estado se distingue por una combinación de alteraciones rápidas y profundas en la función de órganos y tejidos, habitualmente con afectación multisistémica.
El proceso inicia con un estímulo lesivo —como infección, trauma o insuficiencia orgánica— que desencadena una respuesta sistémica acelerada y, si no se revierte, provoca disfunción progresiva.
Comprender la respuesta fisiológica inicial (por ejemplo, activación neuroendocrina o inflamatoria) y su transición a mecanismos patológicos (como pérdida de la autorregulación vascular o daño endotelial) constituye la base para desentrañar las etapas en que la homeostasis se debilita.
Así, analizar la progresión de eventos celulares, tisulares y sistémicos permite anticipar las consecuencias cuando la integración funcional se pierde de forma abrupta y severa.
🌍 Contexto y alcance
El manejo biológico de la enfermedad crítica integra mecanismos desde el nivel molecular y celular hasta los sistemas orgánicos completos.
Existen tres niveles clave de estudio:
- Nivel sistémico: Evalúa la función interdependiente de órganos vitales —corazón, pulmones, riñones, hígado— y de sistemas reguladores como el nervioso autónomo e inmunitario.
- Nivel tisular y celular: Explora cómo la circulación, oxigenación y respuesta inflamatoria afectan la viabilidad y función de células especializadas (cardiomiocitos, neumocitos, células tubulares renales y hepatocitos).
- Nivel molecular: Analiza rutas bioquímicas como la producción y consumo de adenosín trifosfato (ATP), señalización intracelular de citocinas, generación de radicales libres y mecanismos de daño estructural (por ejemplo, disrupción de membranas celulares).
El campo abarca tanto fisiología normal (mantenimiento de gradientes, bombeo de iones, homeostasis ácido-base) como fisiopatología (cómo la desregulación específica precipita la disfunción aguda del órgano).
Todo razonamiento en este contexto implica integrar dónde se produce la alteración, qué estructuras o sistemas están involucrados, y cómo este fallo evoluciona en cascada hacia formas más graves de descompensación biológica.
🧬 Estructuras clave
-
Órganos vitales.
¿Qué son?: Unidades anatómicas funcionales (corazón, pulmones, riñones, hígado).
¿Dónde actúan?: Organización macroscópica del cuerpo.
¿Qué producen?: Mantienen circulación, oxigenación, filtrado y metabolismo.
¿Cómo funcionan?:- El corazón bombea sangre generando presión y flujo controlado.
- El pulmón incorpora oxígeno y elimina dióxido de carbono mediante el intercambio gaseoso alveolo-capilar.
- El riñón regula el volumen plasmático, el equilibrio iónico y ácido-base por filtración y absorción selectiva.
- El hígado detoxifica metabolitos y sintetiza proteínas esenciales.
¿Qué ocurre si se alteran?: El daño agudo compromete funciones vitales y desencadena respuestas compensatorias que, si fracasan, precipitan insuficiencia orgánica secuencial.
-
Células endoteliales.
¿Qué son?: Monocapa de células que tapizan la superficie interna de los vasos sanguíneos.
¿Dónde actúan?: Pared vascular, microcirculación.
¿Qué producen?: Controlan la permeabilidad vascular, regulan el tono y evitan la adhesión excesiva de células sanguíneas.
¿Cómo funcionan?:- Liberan óxido nítrico y otros mediadores que modulan vasodilatación y vasoconstricción.
- Forman una barrera selectiva que limita el paso de macromoléculas y células.
- Regulan la coagulación mediante proteínas de superficie y secreción de factores.
¿Qué ocurre si se alteran?: Disrupción del endotelio incrementa la permeabilidad, favorece edema y formación de microtrombos, disminuyendo la perfusión tisular.
-
Sistema inmunitario innato.
¿Qué es?: Conjunto de células (neutrófilos, macrófagos, linfocitos NK) y moléculas (complemento, citocinas) de defensa rápida.
¿Dónde actúa?: Sangre, tejidos y órganos.
¿Qué produce?: Detecta e intenta eliminar amenazas (patógenos, daño tisular).
¿Cómo funciona?:- Reconoce patrones lesivos a través de receptores de reconocimiento inespecífico.
- Activa la liberación de citocinas (por ejemplo, factor de necrosis tumoral alfa, interleucinas) que inducen inflamación local y sistémica.
- Recluta y activa células de respuesta e incrementa el flujo sanguíneo local.
¿Qué ocurre si se altera?: Una respuesta exagerada amplifica la inflamación sistémica y puede inducir daño colateral a tejidos sanos.
-
Sistema nervioso autónomo.
¿Qué es?: Red neuronal que regula funciones involuntarias (frecuencia cardíaca, presión arterial, ventilación).
¿Dónde actúa?: Órganos y vasos a través de fibras simpáticas y parasimpáticas.
¿Qué produce?: Ajustes reflejos inmediatos ante estrés fisiológico.
¿Cómo funciona?:- El sistema simpático incrementa la contractilidad y la frecuencia cardíaca, redistribuye el flujo sanguíneo y promueve la liberación de glucosa.
- El sistema parasimpático atenúa estas respuestas y promueve restauración de la calma física.
¿Qué ocurre si se altera?: Una hiperactivación o déficit autonómico desorganiza la respuesta cardiovascular y puede agravar la inestabilidad hemodinámica.
En síntesis, la alteración simultánea de estas estructuras dificulta que el organismo restablezca el equilibrio por sí mismo, ofreciendo múltiples puntos de entrada para la progresión del daño sistémico.
⚙️ Funciones y procesos
-
Respuesta inflamatoria sistémica
- ¿Qué es?: Liberación generalizada de mediadores (citocinas, quimioquinas) en respuesta a daño, infección o estrés agudo.
- ¿Dónde actúa?: Circulación y tejidos; mayor expresión en el endotelio, linfocitos y células fagocíticas.
- ¿Qué permite?: Recluta células de defensa, incrementa flujo sanguíneo local, facilita eliminación inicial del agente lesivo.
- ¿Cómo se organiza (paso a paso)?:
- Reconocimiento de patrones asociados a daño o patógenos por receptores celulares (TLR, NLR).
- Activación transcripcional de genes inflamatorios.
- Producción y liberación de citocinas sistémicas (ej., interleucina-1, TNF-α).
- Aumento de permeabilidad vascular y adhesión leucocitaria.
- Eventualmente, amplificación positiva del reclutamiento celular y producción de especies reactivas de oxígeno.
- ¿Qué ocurre si se exagera?: Surgen efectos deletéreos como daño endotelial, extravasación de líquido y desbalance entre defensa y autolesión, precipitando disfunción sistémica.
-
Disfunción endotelial
- ¿Qué es?: Pérdida selectiva o generalizada de las funciones reguladoras endoteliales.
- ¿Dónde actúa?: Lecho vascular —capilares, vénulas, arterias pequeñas y grandes.
- ¿Qué permite normalmente?: Mantener integridad de la barrera, evitar la formación excesiva de trombos y regular el tono.
- ¿Cómo ocurre el daño?:
- Las citocinas modifican la expresión de moléculas de adhesión, facilitando el anclaje de leucocitos.
- El estrés oxidativo deteriora el glicocálix endotelial, esencial para la barrera de permeabilidad.
- Se incrementa la exposición de sitios procoagulantes y disminuyen mecanismos anticoagulantes naturales.
- ¿Qué provoca si se altera?: Formación de microtrombos, extravasación de proteínas y líquidos, desencadenando edema, hipoperfusión y avance hacia insuficiencia orgánica.
-
Alteración hemodinámica
- ¿Qué es?: Inestabilidad en los parámetros circulatorios globales (presión arterial, gasto cardíaco, resistencia vascular).
- ¿Dónde actúa?: Corazón y vasos sanguíneos mayores y menores.
- ¿Qué permite normalmente?: Distribuir de manera óptima oxígeno y nutrientes según la demanda tisular.
- ¿Cómo se desencadena la alteración?:
- Pérdida de la autorregulación vascular secundaria a mediadores inflamatorios.
- Vasodilatación patológica reduce el retorno venoso y la presión arterial media.
- El gasto cardíaco puede aumentar, compensar o, si es insuficiente, descender bruscamente.
- Consecuencias: Si disminuye la perfusión tisular de manera global o regional, surge isquemia celular y desequilibrio entre oferta y demanda de oxígeno.
-
Estrés metabólico celular
- ¿Qué es?: Estado bioquímico en que la célula enfrenta déficit de oxígeno, nutrientes o altas demandas energéticas.
- ¿Dónde actúa?: Principalmente en mitocondrias de células de órganos vitales y en tejidos altamente dependientes de oxígeno.
- ¿Qué permite normalmente?: Síntesis eficiente de ATP (adenosín trifosfato) y mantenimiento de gradientes iónicos.
- ¿Cómo se desarrolla el estrés?:
- Déficit de oxígeno lleva a sustitución del metabolismo aeróbico por anaerobio, reduciendo la producción de ATP.
- Se acumula lactato como producto del metabolismo glucolítico anaerobio.
- Las mitocondrias alteradas generan especies reactivas (radicales libres), dañando membranas, proteínas y el ADN.
- Resultado: Disminución de la actividad celular, pérdida de integridad estructural y, si es persistente, muerte celular por necrosis o apoptosis.
-
Disfunción orgánica múltiple
- ¿Qué es?: Falla progresiva y simultánea de dos o más órganos principales.
- ¿Dónde ocurre?: Todo el organismo, con mayor incidencia en órganos dependientes de perfusión crítica (cerebro, corazón, riñón, pulmón, hígado).
- ¿Cómo se establece?:
- La alteración inflamatoria sistémica y la disfunción endotelial conllevan a perfusión inadecuada.
- El estrés metabólico perpetúa la desestabilización de membranas celulares.
- La falta de compensación entre sistemas lleva a la desintegración de la autorregulación fisiológica.
- ¿Qué ocurre?: La insuficiencia funcional comprometida de un órgano incrementa la vulnerabilidad de otros, generando un círculo vicioso de daño interorgánico.
En la enfermedad crítica, cada uno de estos procesos pierde secuencialmente su control, potenciando la gravedad y dificultando la recuperación sin soporte externo.
🔗 Integración funcional
La integración funcional es la capacidad de los sistemas biológicos para coordinar respuestas eficaces al estrés agudo.
Esto depende de interacciones estructuradas entre órganos, tejidos y células, reguladas dinámicamente en tiempo real.
Por ejemplo, ante un daño endotelial brusco:
- Se incrementa la permeabilidad capilar, permitiendo la extravasación de plasma y proteínas hacia el espacio intersticial.
- Esta alteración reduce el volumen circulante efectivo (“hipovolemia relativa”), lo que desciende la presión arterial.
- La caída en presión estimula el sistema nervioso simpático, que compensa elevando la frecuencia y contractilidad cardíaca.
- Aun así, si la perfusión es insuficiente, las células de órganos vitales comienzan a consumir sus reservas de ATP rápidamente.
- La disfunción mitocondrial se agrava: al agotarse el oxígeno, las mitocondrias no mantienen la fosforilación oxidativa eficiente.
- Como consecuencia, se liberan radicales libres que amplifican el daño celular y perpetúan la disfunción tisular.
Las alteraciones inflamatorias, vasculares y metabólicas no ocurren de forma aislada; se realimentan mutuamente:
- La inflamación excesiva deteriora el endotelio, facilitando la coagulación intravascular diseminada.
- La hipoperfusión genera acidosis y depleción energética, disminuyendo la capacidad de recuperación celular.
- Cuando la disfunción progresa a varios órganos, las relaciones compensatorias entre sistemas —como la redistribución circulatoria— se vuelven ineficaces o dañinas.
Este círculo vicioso biológico, donde la lesión inicial se amplifica y perpetúa por la descoordinación sistémica, es el núcleo de la fisiopatología en la enfermedad crítica.
🔬 Métodos y evidencias
El análisis fisiopatológico de la enfermedad crítica se fundamenta en la observación objetiva y el estudio experimental de variables orgánicas y moleculares.
Estos enfoques aportan evidencia sobre la severidad y el patrón de la desregulación funcional:
-
Monitorización invasiva y no invasiva:
- ¿Qué es?: Herramientas para medir parámetros hemodinámicos (presión arterial, gasto cardíaco), volúmenes y saturaciones.
- ¿Dónde se aplican?: Principalmente en cuidados críticos, enfocado en grandes vasos y control central.
- ¿Qué permite?: Detectar rápida y dinámicamente alteraciones perfusionales o de presión que acompañan el deterioro sistémico.
-
Análisis de gases arteriales y lactato:
- ¿Qué es?: Evaluación bioquímica del intercambio gaseoso y del equilibrio ácido-base.
- ¿Dónde se miden?: En sangre arterial extraída habitualmente de arterias periféricas como la radial.
- ¿Qué permiten?: Estimar eficiencia pulmonar, oxigenación tisular y grado de metabolismo anaerobio (lactato sérico).
-
Cuantificación de mediadores inflamatorios:
- ¿Qué es?: Medición de concentraciones de citocinas, proteínas inflamatorias y marcadores celulares.
- ¿Dónde se evalúan?: Suero, plasma y tejidos afectados.
- ¿Qué permite?: Correlacionar magnitud de respuesta inmunitaria con la progresión funcional del daño orgánico.
-
Estudios fisiopatológicos experimentales:
- ¿Qué son?: Modelos animales o celulares que exploran secuencias mecánicas desde el estímulo lesivo hasta la descompensación final.
- ¿Para qué sirven?: Desglosan temporal y causalmente la cascada de alteraciones y ayudan a identificar puntos de control clave.
Estos métodos aportan información esencial para diferenciar alteraciones adaptativas y disfunciones terminales, permitiendo razonamientos precisos sobre la fisiopatología involucrada.
🩺 Puente clínico
El conocimiento de mecanismos celulares, tisulares y sistémicos en la enfermedad crítica facilita interpretar manifestaciones clínicas como efectos directos de procesos biológicos alterados.
Por ejemplo:
- La presencia de edema generalizado refleja el aumento sostenido de la permeabilidad endotelial y la fuga plasmática.
- La disminución brusca de la presión arterial suele deberse a vasodilatación sistémica inducida por mediadores inflamatorios sobre la musculatura vascular.
- El aumento persistente del lactato sérico indica un desplazamiento metabólico hacia rutas anaerobias, señalando déficit de oxigenación y acidosis.
Comprender cómo cada fenómeno observable refleja una alteración en un mecanismo estructural o molecular potencia la capacidad para predecir complicaciones o anticipar la progresión del daño funcional.
Por ejemplo, la relación entre daño endotelial y signos de shock distributivo establece conexiones entre manifestaciones físicas y mecanismos fisiopatológicos subyacentes.
Esta perspectiva integra la biología y fisiología para la evaluación rigurosa del paciente crítico.
💎 Perlas de alto rendimiento
- Activación intensificada de citocinas: inicia una cascada inflamatoria clave que incluye reconocimiento, amplificación y daño endotelial.
- Endotelio vascular pierde selectividad: en inflamación sistémica, permitiendo el paso de proteínas y células hacia el intersticio.
- Formación de microtrombos: en capilares reduce la perfusión tisular y puede anticipar insuficiencia orgánica distal.
- Disfunción mitocondrial: limita la producción de ATP, forzando metabolismo anaerobio y acumulación de lactato.
- Lactato elevado: es un marcador indirecto del metabolismo anaerobio y la gravedad de la hipoperfusión.
- Autorregulación vascular puede perderse rápidamente: ante inflamación que altera el tono vasomotor y el control autonómico.
- Sobreactivación del sistema nervioso simpático: favorece vasoconstricción no selectiva y aumenta la demanda de oxígeno.
- Células endoteliales bajo estrés: expresan factores procoagulantes, desequilibrando coagulación y anticoagulación fisiológica.
🧠 Puntos clave
- Enfermedad crítica es resultado de una desregulación aguda: que afecta múltiples sistemas, causando pérdida de integridad funcional.
- Daño endotelial y respuesta inflamatoria exacerbada: son mecanismos centrales que alteran perfusión y metabolismo celular.
- Inestabilidad hemodinámica refleja incapacidad del sistema circulatorio: para compensar pérdidas sostenidas de volumen y presión.
- Integración sistémica fallida: perpetúa el daño interorgánico y dificulta la recuperación espontánea de la homeostasis.
- Evaluación funcional y bioquímica: permite identificar niveles de descompensación y orientar razonamientos fisiopatológicos.
- Manifestaciones clínicas reflejan procesos patobiológicos definidos: a nivel estructural y molecular.
❓ Preguntas frecuentes
¿Cómo se define fisiológicamente la enfermedad crítica y qué la diferencia de otros estados patológicos?
Se define por un compromiso agudo y severo de sistemas vitales, caracterizado por una respuesta adaptativa que se torna perjudicial, conduciendo a pérdida simultánea de autorregulación, perfusión y metabolismo celular.
¿Qué papel específico cumple el endotelio vascular en el fallo orgánico?
El endotelio regula la barrera sangre-tejido y mantiene la homeostasis vascular; su daño permite extravasación, favorece microtrombosis y altera la entrega de oxígeno y nutrientes, contribuyendo a la disfunción tisular.
¿Por qué la inflamación sistémica puede ser perjudicial en vez de protectora?
Porque una activación desproporcionada y sostenida lesiona tejidos sanos, induce daño endotelial y genera un ciclo auto-perpetuante de alteraciones metabólicas y funcionales.
¿Cómo contribuye el sistema nervioso autónomo a la fisiopatología de la enfermedad crítica?
Inicialmente compensa con vasoconstricción y aumento de frecuencia cardiaca, pero su sobreactivación o agotamiento impide respuestas adecuadas, empeorando la hipoperfusión y la disfunción orgánica.
¿Por qué el lactato sérico es un marcador relevante en la enfermedad crítica?
Indica que el metabolismo celular ha transicionado a vías anaerobias por déficit de oxígeno, reflejando disfunción en la entrega y utilización energética celular.
¿Cuáles son los mecanismos biológicos que explican la progresión hacia disfunción orgánica múltiple?
Incluyen inflamación sistémica, alteración endotelial, coagulación intravascular, hipoperfusión, estrés metabólico y retroalimentación negativa entre sistemas que perpetúa el deterioro global.
¿Qué tipo de información aporta la monitorización fisiológica y bioquímica en estados críticos?
Permite delimitar la etapa y gravedad de la disfunción, identificar patrones de alteración y vincular manifestaciones observables con mecanismos fisiopatológicos definidos, ajustando el análisis funcional en tiempo real.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico relacionado con la enfermedad crítica según el artículo proporcionado.
Nivel 1 – Básico
¿Qué caracteriza a la enfermedad crítica según la idea central del artículo?
¿Cuál es la función principal del endotelio vascular según el artículo?
¿Dónde ocurre principalmente el estrés metabólico celular en la enfermedad crítica?
Nivel 2 – Intermedio
Según el artículo, ¿cuál es la relación correcta entre la disfunción endotelial y la alteración hemodinámica?
¿Cuál de las siguientes estructuras y funciones está correctamente emparejada según el texto?
¿Cómo se integra funcionalmente la respuesta vascular y metabólica ante un daño endotelial brusco según el artículo?
Nivel 3 – Avanzado
Según el mecanismo paso a paso de la respuesta inflamatoria sistémica, ¿qué ocurre después de la activación transcripcional de genes inflamatorios?
Si la disfunción endotelial altera la expresión de moléculas de adhesión y el glicocálix endotelial se deteriora, ¿qué consecuencias se describen en el artículo?
¿Cómo contribuye la pérdida de integración funcional a la progresión hacia disfunción orgánica múltiple según la fisiopatología descrita?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.