⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La fisiopatología del shock implica la insuficiencia circulatoria para satisfacer la demanda celular de oxígeno, desencadenando una cascada progresiva de hipoxia, disfunción celular y fallo orgánico. La alteración en la perfusión y en la función endotelial amplifica el daño tisular y la inflamación, llevando a disfunción orgánica múltiple.
🧬 Concepto base
El shock es un estado crítico donde el sistema cardiovascular no provee oxígeno ni nutrientes suficientes a los tejidos, comprometiendo la función celular. Afecta estructuras clave como corazón, vasos sanguíneos, endotelio y células diana.
⚙️ Mecanismo clave
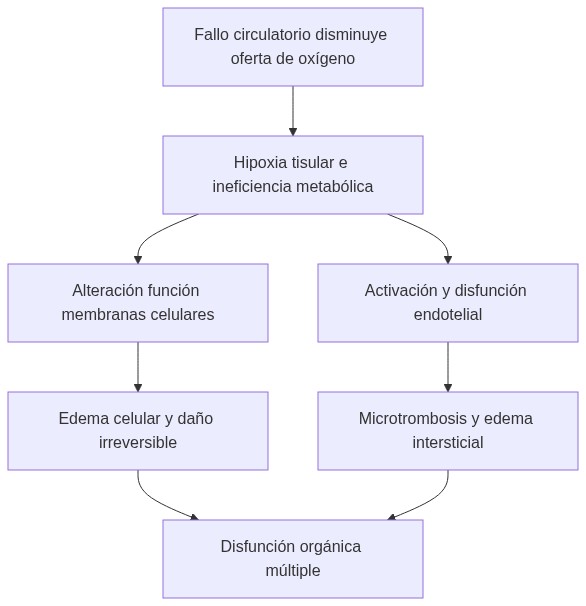
Disminución del gasto cardíaco o volumen provoca hipoperfusión → hipoxia celular → metabolismo anaeróbico → déficit de ATP → fallo de bombas iónicas → disfunción membrana y edema → activación endotelial → inflamación y microtrombosis → daño tisular progresivo y disfunción múltiple.
🔗 Por qué es importante
El shock induce un círculo vicioso de hipoperfusión y daño celular que es la base del fallo multiorgánico y la pérdida de homeostasis.
🎯 Puntos que suelen preguntarse en examen
- Definición fisiopatológica de shock y su relación con el aporte y demanda de oxígeno.
- Mecanismos celulares afectados por la hipoxia persistente en el shock.
- Rol del endotelio vascular en la progresión del shock.
- Consecuencias bioquímicas del metabolismo anaeróbico, como la acidosis láctica.
- Secuencia causal desde hipoperfusión hasta disfunción orgánica múltiple.
- Diferenciación entre estructuras involucradas: corazón, vasos, endotelio y células parenquimatosas.
Palabras clave: fisiopatología del shock, hipoxia, gasto cardíaco, endotelio vascular, metabolismo anaeróbico, acidosis láctica, disfunción celular, falla orgánica múltiple
La fisiopatología del shock describe los mecanismos por los cuales una entrega insuficiente de oxígeno y nutrientes a los tejidos, en relación con la demanda metabólica celular, genera una disfunción progresiva en células y órganos.
Este proceso sistémico y celular conduce a alteraciones clínicas significativas, resaltando la importancia de comprender el proceso desde la pérdida de la homeostasis circulatoria hasta el desarrollo potencialmente irreversible de fallo multiorgánico.
🧠 Idea central
El shock es una condición crítica caracterizada por una incapacidad del sistema circulatorio para suministrar oxígeno adecuado a los tejidos según sus necesidades celulares.
Esta insuficiencia activa mecanismos compensadores sistémicos que pueden ser efectivos temporalmente, pero que si persisten, contribuyen al daño celular y tisular progresivo.
El núcleo fisiopatológico del shock es el desequilibrio entre la oferta y la demanda de oxígeno, lo que lleva a una disfunción que progresa desde el nivel celular, pasando por el tisular, hasta afectar órganos completos.
Cuando la célula recibe menos oxígeno del requerido, se activan vías metabólicas anaeróbicas menos eficientes y potencialmente dañinas, desencadenando una cascada de alteraciones bioquímicas y estructurales.
Comprender esta sucesión explica cómo el shock puede evolucionar hacia disfunción orgánica irreversible y pérdida de la homeostasis vital si no se corrige.
🌍 Contexto y alcance
El estudio de la fisiopatología del shock abarca desde el nivel sistémico, identificando alteraciones funcionales globales del sistema cardiovascular, hasta el nivel celular, donde la insuficiencia de oxígeno provoca efectos críticos.
El shock representa la culminación de un fallo en el transporte y entrega de oxígeno, cuyas repercusiones más graves ocurren en la célula.
A nivel sistémico, el shock implica una disfunción en las estructuras encargadas del transporte de oxígeno y nutrientes —el corazón, los vasos sanguíneos y la sangre— ante una demanda celular que excede la oferta.
A nivel tisular, se produce una disminución de la presión parcial de oxígeno en la microvasculatura, alterando el gradiente para la difusión celular.
Y a nivel intracelular, la falta de oxígeno obliga a las células a depender del metabolismo anaeróbico, afectando su función, integridad y supervivencia.
🧬 Estructuras clave
-
Sistema cardiovascular:
- ¿Qué es? Conjunto integrado por corazón (bomba), vasos sanguíneos (conductos) y sangre (medio portador).
- ¿Dónde actúa? A nivel sistémico, irrigando todo el organismo.
- ¿Qué permite? Permite la entrega de oxígeno y nutrientes a tejidos y la eliminación de desechos metabólicos.
-
¿Cómo funciona?
- El corazón genera presión impulsando la sangre.
- Arterias distribuyen el flujo; arteriolas regulan resistencia periférica y perfusión local.
- Vénulas y venas permiten el retorno sanguíneo.
- La sangre transporta oxígeno unido a hemoglobina, nutrientes y productos metabólicos.
- ¿Qué ocurre si se altera? Disminución del gasto cardíaco, obstrucción vascular o insuficiencia volumétrica reducen la oferta de oxígeno, provocando hipoperfusión.
-
Endotelio vascular:
- ¿Qué es? Monocapa celular que recubre internamente los vasos sanguíneos.
- ¿Dónde actúa? En la pared de arterias, venas y especialmente capilares.
- ¿Qué permite? Mantiene la barrera vaso-sangre, regula permeabilidad y modula respuestas inflamatorias y coagulantes.
-
¿Cómo funciona?
- Controla el paso de líquidos, solutos y células mediante uniones intercelulares y secreción de factores vasoactivos.
- Secreta mediadores como óxido nítrico y prostaciclinas que regulan tono vascular y evitan agregación plaquetaria.
- Responde al daño liberando citocinas que facilitan inflamación y alteran la función barrera.
- ¿Qué ocurre si se altera? La disfunción endotelial aumenta la permeabilidad, produce edema, activa coagulación e inflamación local y sistémica.
-
Células parenquimatosas de órganos vitales:
- ¿Qué es? Células principales responsables de funciones específicas de cada órgano (miocitos cardíacos, neuronas, células tubulares renales, etc.).
- ¿Dónde actúa? En órganos esenciales como cerebro, riñón, hígado, corazón y pulmón.
- ¿Qué permite? Realización de funciones esenciales como contracción, transmisión nerviosa y filtración renal.
-
¿Cómo funciona?
- Consumen oxígeno y glucosa para generar adenosín trifosfato (ATP) mediante fosforilación oxidativa en mitocondrias.
- Mantienen gradientes iónicos, integridad membranal y funciones biosintéticas con energía derivada del metabolismo aeróbico.
- ¿Qué ocurre si se altera? La hipoxia provoca pérdida de función, fallo de bombas iónicas, edema celular y daño irreversible si la deprivación persiste.
⚙️ Funciones y procesos
El shock se inicia por la falla en la entrega adecuada de oxígeno y nutrientes, activando una secuencia fisiopatológica que afecta progresivamente células y estructuras, con consecuencias en cascada que potencian el daño inicial.
-
Fallo circulatorio y reducción del aporte de oxígeno:
- ¿Qué es? Incapacidad primaria del sistema cardiovascular para mantener gasto cardíaco, presión arterial y volumen sanguíneo adecuados.
- ¿Dónde actúa? Desde el corazón hasta la microcirculación.
- ¿Qué permite normalmente? Mantener el gradiente de presión para perfundir órganos y permitir intercambio gaseoso.
-
¿Cómo funciona?
- Alteraciones como disfunción cardíaca, hipovolemia, vasodilatación inapropiada u obstrucción vascular disminuyen la presión de perfusión.
- Esto limita el flujo sanguíneo efectivo a la microcirculación.
- Finalmente, la entrega de oxígeno al tejido es insuficiente.
- ¿Qué ocurre si se altera? El gradiente capilar-célula se reduce, limitando la entrada de oxígeno a las células.
-
Desarrollo de hipoxia tisular e ineficiencia metabólica:
- ¿Qué es? Estado de oxigenación deficiente a nivel tisular.
- ¿Dónde actúa? En células dependientes del metabolismo aeróbico, especialmente en órganos con alta demanda metabólica.
- ¿Qué permite normalmente? Producción eficiente de ATP por fosforilación oxidativa mitocondrial.
-
¿Cómo funciona?
- La reducción de oxígeno disminuye la cadena respiratoria.
- La célula aumenta glucólisis anaeróbica compensatoriamente.
- Se acumula ácido láctico, acidificando el medio celular.
- La producción de ATP se reduce abruptamente dada la baja eficiencia de la glucólisis anaeróbica.
- ¿Qué ocurre si se altera? Se afecta la síntesis proteica, transporte activo iónico y mantenimiento de gradientes osmóticos esenciales.
-
Alteración de la función de membranas celulares:
- ¿Qué es? Pérdida del control sobre el tráfico iónico y molecular a través de la membrana celular por falta de ATP.
- ¿Dónde actúa? En cada célula afectada por hipoxia y depleción energéticas.
- ¿Qué permite normalmente? Mantener gradientes de sodio, potasio y calcio mediante bombas ATP-dependientes (Na+/K+ ATPasa).
-
¿Cómo funciona?
- La disminución del ATP impide la función de bombas iónicas.
- El sodio se acumula intracelularmente, arrastrando agua y causando edema celular.
- El calcio se acumula, activando enzimas que dañan proteínas estructurales y mitocondriales.
- ¿Qué ocurre si se altera? Se pierde la integridad celular, causando hinchazón y posible lisis si la reperfusión no se restablece.
-
Activación y disfunción endotelial:
- ¿Qué es? Alteración del endotelio vascular que modifica sus funciones barriera y regulatorias.
- ¿Dónde actúa? Principalmente en la microvasculatura y capilares de órganos vitales.
- ¿Qué permite normalmente? Controlar permeabilidad, tono vascular y respuesta inflamatoria adecuada.
-
¿Cómo funciona?
- El endotelio dañado libera mediadores proinflamatorios y procoagulantes.
- Aumenta la permeabilidad, facilitando edema.
- Permite el reclutamiento leucocitario y la formación de microtrombos.
- Esto perpetúa la hipoperfusión por obstrucción microvascular y edema.
- ¿Qué ocurre si se altera? Se amplifica la lesión tisular, debilitando la barrera vascular y favoreciendo la disfunción orgánica.
-
Progresión hacia la disfunción orgánica múltiple:
- ¿Qué es? Estado avanzado tras acumulación de daño tisular por hipoxia sostenida.
- ¿Dónde actúa? Órganos con alta demanda metabólica: cerebro, corazón, riñón, hígado, pulmones.
- ¿Qué permite normalmente? Función coordinada que mantiene homeostasis; su falla conduce al colapso sistémico.
-
¿Cómo funciona?
- Daño celular prolongado genera alteraciones metabólicas e inflamatorias generalizadas.
- Los órganos fallan progresivamente, manifestando alteraciones en contractilidad, encefalopatía, insuficiencia renal y respiratoria.
- El ciclo de hipoxia, inflamación y microangiopatía perpetúa la lesión y disfunción.
- ¿Qué ocurre si se altera? La disfunción orgánica múltiple es difícilmente reversible y puede ser fatal si persiste la hipoxia.
🔗 Integración funcional
El shock implica la ruptura coordinada de múltiples mecanismos reguladores.
Las estructuras involucradas interactúan y la afectación de cualquiera repercute a nivel sistémico, desde la macro hasta la microcirculación, comprometiendo la función celular.
El daño endotelial ocasiona que un evento local se transforme en una respuesta inflamatoria y coagulopática generalizada.
Analizando la secuencia causa-efecto:
- Reducción del gasto cardíaco o volumen intravascular → menor presión de perfusión → flujo sanguíneo insuficiente hacia órganos.
- Flujo insuficiente → menor entrega de oxígeno al espacio tisular → reducción del gradiente para difusión celular.
- Hipoxia celular sostenida → metabolismo anaeróbico aumentado → disminución masiva de ATP.
- Fallo de bombas iónicas → desestabilización membranal y edema celular.
- Disfunción endotelial → inflamación y microtrombosis → agravamiento de la hipoperfusión y lesión.
Este círculo vicioso de hipoxia, acidosis, inflamación y microtrombosis perpetúa y agrava el shock.
La integración funcional radica en cómo los mecanismos celulares, vasculares y metabólicos actúan secuencialmente, amplificando el daño mientras la hipoperfusión persiste.
🔬 Métodos y evidencias
La comprensión moderna de la fisiopatología del shock proviene de múltiples herramientas experimentales y estudios clínicos sistemáticos:
-
Cuantificación bioquímica de metabolitos:
- ¿Qué es? Medición de compuestos generados o alterados en hipoxia tisular, como el ácido láctico.
- ¿Dónde actúa? Concentraciones plasmáticas y tisulares.
- ¿Qué permite? Indica intensidad del metabolismo anaeróbico y déficit de oxígeno, reflejando el estado celular.
-
Estudios hemodinámicos:
- ¿Qué es? Medición de presión arterial, presión venosa central y gasto cardíaco.
- ¿Dónde actúa? Evaluación global y regional del sistema cardiovascular.
- ¿Qué permite? Determinar grado de disfunción circulatoria y perfusión sistémica.
-
Observación histopatológica:
- ¿Qué es? Análisis microscópico de tejidos en shock.
- ¿Dónde actúa? Órganos como riñón, hígado, músculo cardíaco y cerebro.
- ¿Qué permite? Identificar daño celular, disfunción endotelial y trombosis microvascular.
-
Biomarcadores celulares de hipoxia y daño:
- ¿Qué es? Medición de enzimas y proteínas plasmáticas liberadas por células en estrés, como lactato deshidrogenasa.
- ¿Dónde actúa? En plasma durante estados hipoperfusivos.
- ¿Qué permite? Cuantificar la magnitud de daño y disfunción celular asociada a hipoxia sostenida.
Estas metodologías permiten mapear la evolución del shock, delimitando la relación entre perfusión insuficiente, metabolismo anaeróbico, acidosis, daño celular y manifestaciones clínicas.
🩺 Puente clínico
Comprender la fisiopatología del shock permite correlacionar la alteración inicial en circulación con los efectos celulares y orgánicos subsecuentes.
El desequilibrio entre aporte y demanda de oxígeno activa mecanismos compensatorios inmediatos, que si persisten, derivan en lesión celular y fallo sistémico.
Este marco analítico enfatiza el análisis de signos como caída de presión arterial, enlentecimiento del flujo capilar, aumento de ácido láctico o edema desde la perspectiva de mecanismos fisiopatológicos, más allá de lo meramente semiológico.
La integración clínica y celular facilita anticipar la progresión hacia disfunción de órganos vitales, la principal consecuencia del shock no tratado.
💎 Perlas de alto rendimiento
- Déficit en la entrega de oxígeno: El shock siempre implica déficit en la entrega de oxígeno respecto a la demanda metabólica, independientemente de su causa.
- Secuencia fisiopatológica: La secuencia fisiopatológica involucra corazón, vasos sanguíneos, endotelio y células diana en un proceso encadenado.
- Hipoperfusión e hipoxia: La hipoperfusión determina hipoxia tisular y dependencia del metabolismo anaeróbico, aumentando riesgo de daño celular.
- Ácido láctico: La acumulación de ácido láctico es un marcador directo del metabolismo anaeróbico persistente.
- Disfunción endotelial: La disfunción endotelial favorece microtrombosis y edema intersticial que exacerban la hipoperfusión.
- Círculo vicioso: El círculo vicioso de hipoxia, disfunción metabólica, inflamación y microtrombosis mantiene el daño progresivo.
- Órganos sensibles: Órganos con alta demanda de oxígeno, como cerebro, corazón y riñón, son los primeros en sufrir daño severo.
- Mecanismos comunes: Diversos tipos de shock convergen en mecanismos comunes de hipoxia celular e inflamación que explican lesiones finales similares.
🧠 Puntos clave
- Mecanismos compensadores: La insuficiente entrega de oxígeno activa mecanismos compensadores que, si se mantienen, agravan el daño celular.
- Rol del endotelio: El endotelio es un mediador central que conecta hipoperfusión, inflamación y coagulación microvascular en el shock.
- Metabolismo anaeróbico: La dependencia celular del metabolismo anaeróbico incrementa la acidosis láctica y la disfunción energética.
- Deterioro progresivo: El deterioro progresivo empieza en células y tejidos y culmina en disfunción orgánica múltiple irreversible.
- Cascada metabólica y estructural: La cascada metabólica y estructural explicada es fundamental para interpretar la evolución fisiopatológica del shock.
❓ Preguntas frecuentes
¿Por qué el shock causa daño orgánico si todas las células usan oxígeno continuamente?
Porque la reducción en el flujo sanguíneo hace que el oxígeno no llegue en cantidad suficiente para sustentar el metabolismo aeróbico, obligando a la célula al metabolismo anaeróbico poco eficiente y tóxico que conduce a fallo celular.
¿En qué órganos es más evidente la alteración fisiopatológica durante el shock?
En órganos con alta demanda metabólica, como cerebro, corazón, riñón y en menor grado hígado y pulmones, que muestran signos tempranos de disfunción por hipoxia.
¿Cómo se genera la acidosis láctica en el shock?
La hipoxia obliga a las células a convertir piruvato en lactato en la glucólisis anaeróbica, acumulándose ácido láctico y provocando acidosis metabólica.
¿Cuál es el rol del endotelio en el shock?
El endotelio actúa como sensor y modulador vascular; cuando se daña, incrementa permeabilidad, inflammation y coagulación, empeorando la microcirculación.
¿Por qué la disfunción multiorgánica es un riesgo en shock no corregido?
Porque la hipoxia prolongada daña células de órganos vitales, superando su capacidad compensatoria y provocando fallo sistémico irreversible.
¿Por qué la restauración rápida de la perfusión es importante?
Porque si la hipoxia es breve, muchas alteraciones metabólicas y estructurales pueden revertirse; sin embargo, si es prolongada, el daño puede ser irreversible.
¿Todos los tipos de shock comparten mecanismos fisiopatológicos?
Aunque difieren en su causa primaria, todos convergen en hipoperfusión, hipoxia, metabolismo anaeróbico, disfunción iónica y daño tisular, lo que explica manifestaciones semejantes en fases avanzadas.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico y conceptual sobre la fisiopatología del shock según el artículo proporcionado.
Nivel 1 – Básico
¿Qué es el shock según la idea central del artículo?
¿Cuál es el componente principal del sistema cardiovascular que genera presión para impulsar la sangre?
¿Qué producen las células cuando reciben menos oxígeno del requerido?
Nivel 2 – Intermedio
Según el artículo, ¿cómo se relaciona la disfunción endotelial con la hipoperfusión tisular en el shock?
¿Cuál es la relación correcta según el artículo entre la reducción del gasto cardíaco y la función celular?
En el contexto del shock, ¿qué función crucial tienen las bombas iónicas dependientes de ATP en las células parenquimatosas?
Nivel 3 – Avanzado
¿Cuál es la secuencia correcta de eventos en la fisiopatología del shock que conduce a edema celular, según el artículo?
Considerando la integración funcional, ¿qué efecto tiene la disfunción endotelial en el ciclo vicioso del shock?
En el estado avanzado del shock, ¿cuáles son las consecuencias metabólicas y orgánicas causadas por la hipoxia prolongada?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.