⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La fisiopatología del shock cardiogénico describe la falla aguda del ventrículo izquierdo para mantener el gasto cardíaco, provocando hipoperfusión sistémica y congestión pulmonar por sobrecarga hemodinámica. El colapso funcional se instaura por disfunción contráctil, aumento de poscarga y activación neuroendocrina exacerbando el deterioro miocárdico y metabólico.
🧬 Concepto base
El shock cardiogénico es un estado crítico donde el miocardio ventricular, principalmente izquierdo, pierde su capacidad contráctil para impulsar sangre adecuada hacia la circulación sistémica, causando insuficiencia circulatoria.
⚙️ Mecanismo clave
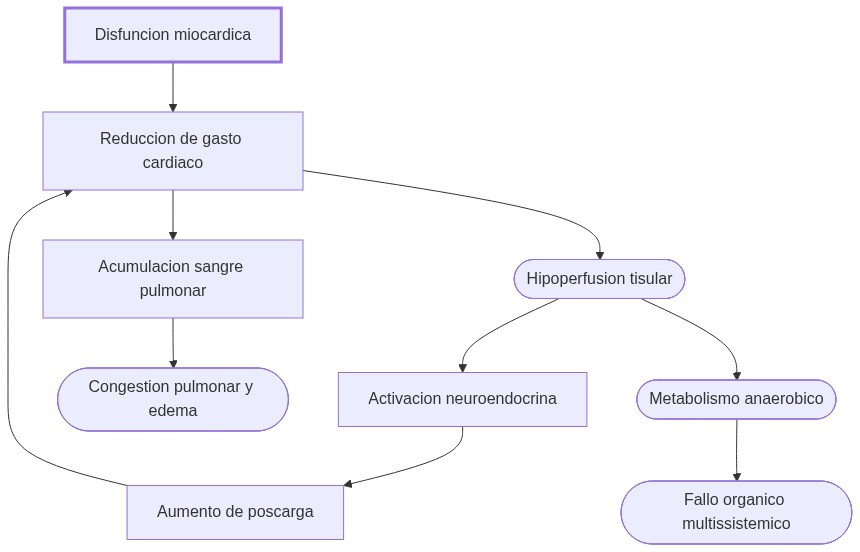
La reducción de contractilidad disminuye el volumen sistólico, activando compensaciones neuroendocrinas que elevan la poscarga y causan congestión pulmonar, lo que agrava la hipoperfusión y desplaza el metabolismo celular a la vía anaeróbica.
🔗 Por qué es importante
Esta fisiopatología explica el fallo multiorgánico por hipoxia progresiva y el círculo vicioso de sobrecarga ventricular, base para entender la descompensación clínica y signos correlacionados.
🎯 Puntos que suelen preguntarse en examen
- Definición y papel del ventrículo izquierdo en el shock cardiogénico
- Relación entre disminución del gasto cardíaco y congestión pulmonar
- Impacto de la activación neuroendocrina en la poscarga y función ventricular
- Consecuencias metabólicas del déficit de oxígeno en tejidos
- Importancia del sistema de conducción eléctrica en la sincronía contráctil
- Efectos del aumento de presiones de llenado sobre el edema pulmonar
Palabras clave: fisiopatología del shock cardiogénico, ventrículo izquierdo, gasto cardíaco, poscarga, congestión pulmonar, activación neuroendocrina, hipoperfusión, metabolismo anaeróbico
La fisiopatología del shock cardiogénico descompone los mecanismos por los cuales la alteración aguda de la función cardíaca conduce a la reducción crítica del gasto cardíaco y de la perfusión tisular.
Comprender cómo la dinámica estructural y funcional del miocardio, junto con las respuestas hemodinámicas sistémicas, colapsan bajo estas condiciones es clave para analizar tanto el compromiso cardiovascular central como las consecuencias en la oxigenación y el metabolismo de los órganos.
Esta perspectiva permite correlacionar alteraciones puntuales en la biología cardíaca con la interrupción de la homeostasis sistémica.
🧠 Idea central
El shock cardiogénico constituye una emergencia fisiopatológica causada por el fracaso agudo del corazón para mantener el flujo sanguíneo necesario que permita la oxigenación y nutrición tisular.
El sustrato principal es la incapacidad del ventrículo izquierdo de generar suficiente presión o volumen sistólico para sostener el gasto cardíaco. Como efecto inmediato, se produce hipoperfusión sistémica y acumulación de sangre en el circuito pulmonar.
Desde el punto de vista mecanicista, esta condición se origina en el desequilibrio entre la oferta de oxígeno (determinado por el flujo sanguíneo que el corazón puede aportar) y la demanda metabólica de los órganos.
La consecuencia ineludible de este desequilibrio es la disrupción de la homeostasis, con aparición de disfunción celular por déficit energético.
El estudio fisiopatológico del shock cardiogénico implica descomponer cada eslabón de la cascada: cómo la reducción inicial del gasto desencadena primero mecanismos compensatorios (por vía neuroendocrina y hemodinámica) que, lejos de corregir la falla, aumentan las resistencias y la congestión, empeorando el daño funcional y estructural.
🌍 Contexto y alcance
El análisis del shock cardiogénico se sitúa en la intersección entre la fisiología cardiovascular y la fisiopatología sistémica.
El contexto central es la pérdida repentina de la capacidad de bombeo cardíaco, evento que altera parámetros críticos como la presión arterial media, el flujo de oxígeno a los tejidos y el mantenimiento del gradiente de presiones que permite el intercambio gaseoso.
El alcance biológico abarca desde los componentes celulares del miocardio (miofilamentos, sarcolema, sistemas de señalización intracelular) y la integridad de la matriz extracelular, hasta la organización funcional de cámaras y válvulas.
Además, incorpora la interacción del corazón con circuitos extracardíacos, especialmente el lecho vascular pulmonar y sistémico. En sentido ampliado, se consideran mecanismos reguladores como la activación del sistema nervioso autónomo y la respuesta hormonal, que modulan la acción cardiovascular para intentar restaurar la perfusión.
Por último, abordar el shock cardiogénico requiere comprender cómo la descompensación primaria origina alteraciones secuenciales en la función pulmonar (por acumulación de líquido y aumento de presiones) y en el metabolismo celular, estableciendo un nexo directo entre la falla en el órgano bomba y la viabilidad de órganos periféricos.
🧬 Estructuras clave
-
Miocardio ventricular:
- ¿Qué es? Es el tejido muscular estriado especializado que forma las paredes de los ventrículos cardíacos, principalmente el izquierdo.
- ¿Dónde actúa? Conforma el grueso del ventrículo izquierdo y derecho.
- ¿Qué permite? Permite la generación de la fuerza necesaria para expulsar la sangre hacia la circulación sistémica y pulmonar mediante contracciones coordinadas.
- ¿Cómo funciona? La despolarización de la membrana sarcolémica y la liberación de calcio intracelular permiten la interacción de actina y miosina para generar contracción. La integridad celular y la energía disponible (mayormente por metabolismo aeróbico) son indispensables.
- ¿Qué ocurre si se altera? La lesión por isquemia o alteración estructural impide la contracción eficiente, reduciendo el volumen sistólico y el gasto cardíaco.
-
Válvulas cardíacas:
- ¿Qué son? Son estructuras de tejido conectivo denso recubierto por endocardio que aseguran el flujo unidireccional de sangre a través de las cámaras cardíacas.
- ¿Dónde actúan? Se encuentran en la entrada y salida de los ventrículos (mitral y tricúspide, aórtica y pulmonar).
- ¿Qué permiten? Permiten que la sangre se desplace hacia adelante evitando el reflujo o regurgitación entre cámaras.
- ¿Cómo funcionan? Se abren y cierran pasivamente según gradientes de presión generados entre cámaras durante el ciclo cardíaco.
- ¿Qué ocurre si se altera? La insuficiencia o estenosis válvular interfiere en el llenado o vaciamiento ventricular, agregando sobrecarga y agravando la hipoperfusión.
-
Sistema de conducción eléctrica cardíaca:
- ¿Qué es? Es una red de células especializadas (nódulo sinoauricular, nódulo auriculoventricular, Haz de His-Purkinje) que coordinan el desencadenamiento del potencial de acción en el miocardio.
- ¿Dónde actúa? Recorridos desde la aurícula derecha hasta los ventrículos.
- ¿Qué permite? Determina la sincronía y la frecuencia de la contracción de las fibras musculares cardíacas.
- ¿Cómo funciona? Los impulsos eléctricos viajan secuencialmente activando la despolarización y contracción ordenada del tejido muscular.
- ¿Qué ocurre si se altera? La desincronización o bloqueos pueden limitar la eficacia mecánica, reduciendo aún más el gasto cardíaco.
-
Vasos sanguíneos periféricos y pulmonares:
- ¿Qué son? Conductos vasculares formados por capas de células endoteliales, musculares lisas y tejido conectivo.
- ¿Dónde actúan? Distribuyen la sangre desde el corazón hacia los tejidos y de regreso, además de servir como reservorios de volumen.
- ¿Qué permiten? Permiten el ajuste de la resistencia vascular (poscarga), la distribución del flujo y el tiempo de retorno sanguíneo al corazón (precarga).
- ¿Cómo funcionan? Vasoconstricción o vasodilatación determinada por estímulos autonómicos, presión transmural y señales hormonales.
- ¿Qué ocurre si se altera? El aumento de resistencia (vasoconstricción) a nivel sistémico incrementa la poscarga, dificultando la eyección ventricular, y el aumento de presión en el circuito pulmonar favorece el edema alveolar.
-
Sistema neuroendocrino regulador:
- ¿Qué es? Conjunto de vías de señalización, principalmente el sistema nervioso simpático (adrenalina, noradrenalina) y el eje renina-angiotensina-aldosterona.
- ¿Dónde actúa? Sobre órganos blanco como vasos sanguíneos, riñón y miocardio.
- ¿Qué permite? Permite la respuesta adaptativa ante caídas de presión arterial y gasto cardíaco, promoviendo vasoconstricción, reabsorción de agua y sodio, e incremento de frecuencia cardíaca.
- ¿Cómo funciona? Detecta la disminución del flujo (barorreceptores) y libera catecolaminas o activa conversión de angiotensina e ingreso de aldosterona; esto modula el tono vascular y el volumen intravascular.
- ¿Qué ocurre si se activa en exceso? Respuestas exageradas favorecen el círculo vicioso de sobrecarga cardíaca, incremento de poscarga y empeoramiento de la función ventricular.
⚙️ Funciones y procesos
En el shock cardiogénico, varias funciones fisiológicas se ven alteradas a través de mecanismos estructurados en secuencia. La comprensión de cada paso permite rastrear la génesis de la hipoperfusión y sus consecuencias metabólicas.
-
Reducción aguda de la contractilidad miocárdica
- Definición: Disminución en la capacidad de las células musculares cardíacas para contraerse y ejercer fuerza.
- Ubicación: Principalmente en miofilamentos del ventrículo izquierdo.
- Mecanismo: Si el ventrículo izquierdo sufre daño por isquemia o necrosis, las células pierden su funcionalidad contráctil. Esto impide que el volumen sistólico (cantidad de sangre eyectada en cada latido) alcance los niveles mínimos para mantener la presión de perfusión.
- Consecuencia: Caída inmediata del gasto cardíaco (volumen sistólico x frecuencia cardíaca) y descenso de la presión arterial sistémica.
-
Acumulación de sangre y aumento de presiones de llenado
- Definición: Elevación progresiva de las presiones en las cámaras cardíacas y vasos aferentes.
- Ubicación: Cavidades ventriculares, aurícula izquierda y venas pulmonares.
- Mecanismo: Cuando el ventrículo izquierdo no es capaz de vaciar su contenido, el volumen residual aumenta la presión diastólica y retrasa el retorno venoso, llevando a acumulación retrógrada de sangre en el lecho pulmonar.
- Consecuencia: Desarrollo de congestión venosa pulmonar y favorecimiento del edema intersticial y alveolar. La presión elevada en los capilares pulmonares induce extravasación de plasma hacia los pulmones.
-
Activación compensatoria del sistema neuroendocrino
- Definición: Reclutamiento de mecanismos regulatorios que buscan restaurar la presión arterial y perfusión.
- Ubicación: Tronco encefálico (centros vasomotores), glándulas adrenales, eje renal.
- Mecanismo: Los barorreceptores detectan caída de presión arterial; esto activa liberación de adrenalina/noradrenalina y estimula la producción de renina. Las catecolaminas inducen vasoconstricción periférica y aumento de la frecuencia cardíaca, mientras que angiotensina II eleva la poscarga y aldosterona retiene agua y sodio.
- Consecuencia: Inicialmente intenta mantener la presión arterial y volumen intravascular, pero la sobrecarga resultante agrava la sobrecarga cardíaca y complica la función ventricular.
-
Elevación de la poscarga y sobrecarga del ventrículo
- Definición: Aumento de la resistencia contra la que el ventrículo debe eyectar sangre.
- Ubicación: Vasculatura arterial sistémica.
- Mecanismo: La activación neurohormonal induce contracción de la musculatura lisa vascular, incrementando la resistencia periférica total. Esto eleva la cantidad de presión que el ventrículo izquierdo requiere superar para mantener el flujo sanguíneo.
- Consecuencia: El ventrículo comprometido no puede responder adecuadamente, con lo que disminuye aún más el gasto cardíaco y el círculo vicioso se perpetúa.
-
Hipoperfusión tisular y disfunción orgánica
- Definición: Reducción efectiva del aporte de sangre y oxígeno a los tejidos periféricos.
- Ubicación: Todos los órganos vitales, especialmente cerebro, riñones e hígado.
- Mecanismo: El flujo insuficiente impide la adecuada llegada de oxígeno, afectando la producción de adenosín trifosfato (ATP) por la fosforilación oxidativa en mitocondrias celulares.
- Consecuencia: Emergen fallas funcionales en órganos dependientes de alta perfusión (confusión, oliguria, transaminasas elevadas, etc.), avisando la falla multisistémica.
-
Desviación metabólica al metabolismo anaeróbico
- Definición: Cambio desde la producción aeróbica de ATP hacia la glucólisis anaeróbica.
- Ubicación: Citoplasma de células privadas de oxígeno en órganos hipo-perfundidos.
- Mecanismo: La falta de oxígeno limita la entrada de piruvato en el ciclo de Krebs, forzando su conversión en lactato mediante lactato deshidrogenasa.
- Consecuencia: Acumulación de lactato, desarrollo de acidosis metabólica y generación de especies reactivas de oxígeno, agravando el deterioro celular y la disfunción orgánica.
🔗 Integración funcional
La fisiopatología del shock cardiogénico se expresa en una secuencia de causa–efecto donde el fallo cardíaco inicial genera cambios compensatorios que, paradójicamente, perpetúan y profundizan la desestabilización sistémica.
Si la contractilidad miocárdica se deprime, entonces el volumen sistólico cae y la presión arterial desciende. Ante esta situación, los barorreceptores en el arco aórtico y seno carotídeo detectan la hipoperfusión y activan el sistema nervioso simpático, que trata de restablecer la homeostasis incrementando la frecuencia cardíaca y la resistencia vascular periférica.
Sin embargo, este aumento en la poscarga representa una sobrecarga adicional para el ventrículo deficiente.
En simultáneo, la disminución del gasto cardíaco reduce la circulación renal, activando la liberación de renina y la formación de angiotensina II y aldosterona, perpetuando la vasoconstricción sistémica y promoviendo la retención de líquidos. Esta retención se traduce en un aumento del volumen intravascular, que, si el corazón carece de reserva contráctil, intensifica la presión en las cámaras cardíacas y los vasos pulmonares, promoviendo la congestión y el edema.
El resultado es un círculo vicioso: las estrategias fisiológicas destinadas a compensar la caída de la presión sistémica terminan castigando aún más el corazón disfuncional. A medida que empeora el aporte sanguíneo a los órganos vitales, las células cambian al metabolismo anaeróbico, incrementando la acidosis y el estrés oxidativo, lo que conduce al fallo multiorgánico.
De esta forma, la integración funcional en el shock cardiogénico abarca desde eventos moleculares (disminución de producción de ATP, aumento de lactato) y celulares (lesión de células miocárdicas y endoteliales) hasta la alteración del comportamiento global de órganos y sistemas bajo una perspectiva biológica y fisiológica.
🔬 Métodos y evidencias
El estudio fisiopatológico del shock cardiogénico se fundamenta en métodos que permiten cuantificar y visualizar los procesos mecánicos y bioquímicos implicados.
A nivel hemodinámico, la medición directa del gasto cardíaco, presión arterial media y presiones de llenado (mediante catéteres de flotación o técnicas no invasivas) permite delinear el grado y la ubicación de la disfunción.
Las imágenes cardíacas, como la ecocardiografía, proporcionan evidencia visual de la disminución de la fracción de eyección, alteraciones en el movimiento de las paredes y cambios morfológicos asociados a congestión o falla valvular.
El seguimiento de parámetros bioquímicos, como el lactato sanguíneo, refleja el grado del metabolismo anaeróbico activado en respuesta a la hipoperfusión.
Los modelos experimentales en animales o estudios in vitro han sido esenciales para dilucidar la respuesta del miocardio bajo condiciones de isquemia aguda, la activación de cascadas intracelulares lesivas y la relación entre sobrecarga de presión y adaptación celular.
Estos métodos han permitido extrapolar cómo el daño miocárdico agudo se traduce en disfunción de la bomba cardíaca y en la génesis del edema pulmonar por aumento de la presión intravascular.
El conocimiento resultante de estos enfoques complementarios refuerza la comprensión mecanicista de que toda disfunción cardíaca severa—no sólo estructural, sino también de regulación y señalización—puede romper la homeostasis cardiovascular y desencadenar colapso tisular.
🩺 Puente clínico
El raciocinio clínico ante el shock cardiogénico se estructura en torno a los mecanismos fisiopatológicos previamente descritos.
Los signos clínicos, como hipotensión, oliguria, alteración del estado mental y edema pulmonar, reflejan expresiones concretas de la hipoperfusión sistémica y la congestión causada por la insuficiencia contráctil ventricular y la sobrecarga de presión.
Cada uno de estos hallazgos se interpreta como el desenlace funcional de problemas biológicos subyacentes: por ejemplo, la disnea se produce tras el aumento de la presión en capilares pulmonares y el paso de líquido hacia el intersticio pulmonar.
El bajo gasto cardíaco explica la disminución de la entrega de oxígeno a tejidos de alta demanda, y la activación neuroendocrina se traduce en taquicardia compensatoria y vasoconstricción cutánea.
Así, el vínculo entre biología y clínica subraya la importancia de identificar no sólo el evento inicial (fallo miocárdico) sino también la secuencia de compensaciones y descompensaciones que producen el cuadro clínico completo.
En este contexto, cada manifestación observable puede ser trazada a un paso específico dentro de la cascada fisiopatológica del shock cardiogénico.
💎 Perlas de alto rendimiento
- Caída crítica del gasto cardíaco: refleja la reducción primaria de la contractilidad ventricular izquierda.
- Aumento de presión venosa pulmonar: proviene de la incapacidad del ventrículo izquierdo para vaciar la sangre pulmonar eficazmente.
- Insuficiencia cardíaca aguda: puede generar hipoperfusión tisular antes que la presión arterial sistólica disminuya significativamente.
- Respuestas del sistema nervioso simpático: inicialmente compensan, pero a largo plazo aumentan la poscarga y empeoran la función ventricular.
- Congestión pulmonar y edema alveolar: resultan de la presión retrógrada elevada sobre los capilares pulmonares.
- Vías neurohormonales: pueden perpetuar la retención hídrica, agravando la congestión.
- Metabolismo celular: desplaza su metabolismo hacia vías anaeróbicas ante hipoxia, acumulando lactato y favoreciendo acidosis.
- Sincronía eléctrica: el fallo en la disminuye la eficiencia contráctil, profundizando la disfunción cardiaca.
🧠 Puntos clave
- Shock cardiogénico: es causado por la incapacidad aguda del ventrículo izquierdo para mantener un gasto cardíaco suficiente.
- Reducción de la contractilidad miocárdica: se asocia con hipoperfusión y congestión pulmonar.
- Activación neuroendocrina: aumenta la poscarga, profundizando el círculo vicioso fisiopatológico.
- Metabolismo energético: cambia a anaeróbico por falta de oxígeno, con acumulación de ácido láctico.
- Alteraciones en estructuras cardíacas y vasculares: contribuyen al deterioro sistémico progresivo.
- Congestión pulmonar y disminución del flujo: a órganos vitales son manifestaciones del fracaso cardíaco central.
❓ Preguntas frecuentes
¿Cómo desencadena el fallo ventricular izquierdo el shock cardiogénico?
La incapacidad del ventrículo izquierdo para generar una contracción eficaz reduce el volumen sistólico, disminuyendo el gasto cardíaco y provocando hipoperfusión tisular.
¿Por qué la congestión pulmonar es un hallazgo central en el shock cardiogénico?
Porque el ventrículo izquierdo debilitado no vacía adecuadamente la sangre que retorna desde los pulmones, aumentando la presión venosa pulmonar y favoreciendo el edema alveolar.
¿Cómo complica la activación neuroendocrina el curso del shock cardiogénico?
Aunque busca restaurar la presión arterial mediante vasoconstricción y retención de líquidos, aumenta la poscarga ventricular, empeorando la función contráctil y perpetuando la insuficiencia.
¿Qué cambios metabólicos sufren las células en estados de hipoperfusión?
Pasan de un metabolismo aeróbico a anaeróbico, produciendo lactato, acidosis y estrés oxidativo, lo que perjudica la supervivencia celular.
¿Cuál es el rol de la poscarga en la progresión del shock cardiogénico?
La poscarga es la resistencia que enfrenta el ventrículo al expulsar sangre; su aumento incrementa la carga de trabajo y limita aún más el gasto cardíaco.
¿Por qué fallan los órganos periféricos en el shock cardiogénico?
La baja perfusión sanguínea reduce la entrega de oxígeno y nutrientes esenciales, provocando disfunción y daño irreversible en órganos sensibles como riñón y cerebro.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico relacionado con la fisiopatología del shock cardiogénico.
Nivel 1 – Básico
¿Qué tejido forma el grueso de las paredes de los ventrículos cardíacos en el shock cardiogénico?
¿Qué función principal cumplen las válvulas cardíacas según el texto?
Según la sección de funciones y procesos, ¿qué ocurre inmediatamente después de una reducción aguda de la contractilidad miocárdica?
Nivel 2 – Intermedio
¿Cuál es la relación correcta entre la activación neuroendocrina y la sobrecarga cardíaca en el shock cardiogénico?
Respecto al sistema de conducción eléctrica cardíaca, ¿qué consecuencia tiene su alteración en el contexto del shock cardiogénico?
¿Cuál es la relación correcta entre la acumulación de sangre en el circuito pulmonar y la congestión en el shock cardiogénico?
Nivel 3 – Avanzado
Si la contractilidad del ventrículo izquierdo disminuye debido a isquemia, ¿qué secuencia fisiopatológica ocurre según el artículo?
¿Cómo contribuye el aumento de la poscarga a perpetuar el círculo vicioso en el shock cardiogénico?
¿Qué cadena de eventos metabólicos ocurre en las células tisulares en respuesta a la hipoperfusión en el shock cardiogénico?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.