⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La fisiopatología del síndrome coronario describe el desequilibrio agudo entre el aporte y demanda de oxígeno en el miocardio causado por lesiones en la pared arterial coronaria que desencadenan trombosis parcial o vasoespasmo, condicionando isquemia reversible o necrosis. Este proceso involucra disfunción endotelial, ruptura o erosión de placa, activación plaquetaria y coagulación, culminando en alteraciones eléctricas y funcionales del tejido cardíaco.
🧬 Concepto base
El síndrome coronario agudo sin elevación persistente del ST (SCASEST) agrupa la isquemia miocárdica causada por trombos no oclusivos o vasoespasmo en arterias coronarias lesionadas, afectando la perfusión y función del miocardio sin elevación del segmento ST.
⚙️ Mecanismo clave
La ruptura o erosión de placas ateroscleróticas expone material trombogénico que activa plaquetas y coagulación, formando trombos parciales que reducen el flujo coronario. El resultado es isquemia miocárdica por déficit de oxígeno, que puede evolucionar a necrosis y alteraciones eléctricas si persiste.
🔗 Por qué es importante
Este proceso determina la gravedad clínica del síndrome coronario, explica la presencia o ausencia de necrosis y arritmias, y permite diferenciar variantes clínicas basadas en la extensión y reversibilidad del daño isquémico.
🎯 Puntos que suelen preguntarse en examen
- Diferencia fisiopatológica entre IAMSEST y angina inestable basada en necrosis celular.
- Mecanismo de formación y ruptura de placa aterosclerótica y su impacto en el flujo coronario.
- Rol del desequilibrio aporte-demanda de oxígeno en la génesis de la isquemia.
- Contribución de la disfunción endotelial a vasoespasmo y trombosis.
- Implicancia de las alteraciones iónicas en la generación de arritmias durante isquemia.
- Significado clínico de la elevación de troponinas en relación con la necrosis miocárdica.
Palabras clave: fisiopatología del síndrome coronario, isquemia miocárdica, placa aterosclerótica, trombosis, disfunción endotelial, necrosis miocárdica, vasoespasmo, IAMSEST
La fisiopatología del síndrome coronario abarca la secuencia de alteraciones estructurales y funcionales que privan al músculo cardíaco de oxígeno, llevando a disfunción tisular, . Analizar estos mecanismos es indispensable para comprender los fundamentos biológicos detrás de los hallazgos clínicos y los cambios electrocardiográficos en los síndromes coronarios agudos, especialmente aquellos sin elevación persistente del segmento ST.
🧠 Idea central
El síndrome coronario agudo sin elevación persistente del segmento ST (SCASEST) agrupa entidades clínicas caracterizadas por daño isquémico miocárdico sin manifestación sostenida en el electrocardiograma del clásico ascenso del segmento ST.
Incluye el infarto agudo de miocardio sin elevación del segmento ST (IAMSEST), con evidencia de necrosis celular, y la angina inestable, donde sólo ocurre isquemia reversible.
El proceso fisiopatológico subyacente consiste en un desequilibrio agudo entre el suministro y la demanda de oxígeno del miocardio. Este desequilibrio suele originarse por alteraciones en la arteria coronaria, como erosión o ruptura de la placa aterosclerótica, que desencadenan trombosis no oclusiva o vasoespasmo en una arteria patológica, comprometiendo el flujo sanguíneo sin obstrucción completa y persistente.
Comprender estos desequilibrios permite relacionar la patología coronaria, la alteración del flujo sanguíneo regional, el metabolismo energético miocárdico y la progresión desde la disfunción reversible hasta el daño celular irreversible.
🌍 Contexto y alcance
La fisiopatología del síndrome coronario se enmarca en la interacción de varias escalas biológicas, desde moléculas implicadas en señalización inflamatoria y coagulación, hasta el músculo cardíaco con su integración funcional y la dinámica anatómica de la arteria coronaria.
Los mecanismos abarcan eventos a nivel celular (como la activación plaquetaria y cambios en permeabilidad celular), alteraciones estructurales en la pared vascular, y disfunción metabólica miocárdica secundaria al déficit de oxígeno.
El análisis fisiopatológico distingue entre:
- Anomalías estructurales de la pared arterial y sus efectos sobre el flujo.
- Procesos celulares y moleculares, como activación plaquetaria, coagulación e inflamación tras daño endotelial o exposición subendotelial.
- Alteraciones metabólicas y funcionales del miocito en respuesta a la isquemia.
Un mismo mecanismo puede manifestarse como IAMSEST o angina inestable, según la severidad, duración de la isquemia y presencia o ausencia de necrosis.
🧬 Estructuras clave
La fisiopatología del síndrome coronario sin elevación persistente del ST involucra estructuras anatómicas y celulares que conectan su función con la isquemia miocárdica:
-
Arterias coronarias:
- ¿Qué es? Vasos arteriales que suministran oxígeno y nutrientes al miocardio.
- ¿Dónde actúa? Circulación epicárdica y ramas intramurales.
- ¿Qué permite? Mantienen la perfusión tisular en función de la demanda energética mediante autorregulación del calibre, que depende del tono muscular liso, función endotelial y presión.
- ¿Qué ocurre si se altera? Cambios estructurales o funcionales, como ateroesclerosis y vasoespasmo, reducen el flujo y predisponen a isquemia.
-
Placa aterosclerótica:
- ¿Qué es? Lesión focal en la íntima arterial, compuesta por lípidos, células inflamatorias, tejido fibroso y músculo liso.
- ¿Dónde actúa? Íntima de arterias coronarias.
- ¿Qué permite? Provoca estenosis asimétricas que alteran el flujo local.
- ¿Qué ocurre si se altera? Su ruptura o erosión expone lípidos y factor tisular, activando coagulación y adhesión plaquetaria, formando trombos parcialmente obstructivos.
-
Sistema de coagulación y plaquetas:
- ¿Qué es? Proteínas plasmáticas y células que limitan hemorragias y promueven trombosis.
- ¿Dónde actúa? Sobre endotelio lesionado y matriz expuesta.
- ¿Qué permite? Forman agregados plaquetarios y depósitos de fibrina para consolidar trombos.
- ¿Qué ocurre si se altera? Respuesta exagerada produce trombosis luminal, mientras la insuficiente predispone a hemorragia.
-
Miocardio:
- ¿Qué es? Tejido muscular especializado para la contracción rítmica y el bombeo sanguíneo.
- ¿Dónde actúa? Pared cardíaca, predominando en ventrículos.
- ¿Qué permite? Genera fuerza para gasto cardíaco, dependiendo de oxígeno para producir adenosín trifosfato (ATP) aerobio.
- ¿Qué ocurre si se altera? Hipoxia sostenida lleva a disfunción reversible (angina) y, si persiste, a necrosis irreversible (infarto).
-
Endotelio vascular:
- ¿Qué es? Capa unicelular que recubre el interior vascular y regula interacción sanguínea y tono vascular.
- ¿Dónde actúa? Superficie luminal de arterias coronarias.
- ¿Qué permite? Libera óxido nítrico y prostaciclina que promueven vasodilatación y previenen adhesión plaquetaria.
- ¿Qué ocurre si se altera? La disfunción endotelial facilita vasoconstricción, inflamación y trombosis.
⚙️ Funciones y procesos
La fisiopatología del síndrome coronario se compone de una serie de mecanismos que producen isquemia miocárdica. Su análisis según la secuencia causal y estructuras involucradas incluye:
-
1. Formación, evolución y ruptura de la placa aterosclerótica
- Definición: Acumulación de lípidos y células inflamatorias en la íntima arterial.
- Localización: Región subendotelial de arterias coronarias, en zonas de flujo turbulento.
- Mecanismo:
- Captación y oxidación de lipoproteínas de baja densidad (LDL).
- Activación endotelial y migración de monocitos que forman células espumosas.
- Inflamación crónica y proliferación de músculo liso.
- Adelgazamiento de la cápsula fibrosa y desestabilización, favoreciendo erosión o ruptura.
- Consecuencia: Exposición de material trombogénico e inicio de coagulación.
-
2. Activación plaquetaria y formación del trombo
- Definición: Respuesta plaquetaria ante la matriz subendotelial expuesta por ruptura o erosión.
- Localización: Sitio de lesión de la placa, sobre colágeno y factor tisular.
- Mecanismo:
- Adhesión plaquetaria mediante receptores específicos.
- Activación y secreción de mediadores (ADP, tromboxano A2) que reclutan más plaquetas.
- Agregación progresiva hasta formar un conglomerado.
- Consecuencia: Trombo parcial reduce el flujo de forma transitoria u oscilatoria, sin oclusión definitiva.
-
3. Activación de la cascada de coagulación
- Definición: Reacciones enzimáticas donde factores de coagulación activados generan fibrina.
- Localización: Sobre plaquetas y sangre en el sitio lesionado.
- Mecanismo:
- Factor tisular activa vía extrínseca.
- Protroimbina se convierte en trombina, que transforma fibrinógeno en fibrina insoluble.
- Fibrina entrecruzada estabiliza el trombo plaquetario.
- Consecuencia: Trombo parcialmente obstructivo, modulando severidad y duración de isquemia.
-
4. Isquemia miocárdica
- Definición: Cuando el aporte de oxígeno no satisface la demanda metabólica del miocardio.
- Localización: Miocitos distales a la obstrucción coronaria.
- Causas:
- Reducción luminal por trombo.
- Vasoespasmo coronario sobre placas vulnerables.
- Aumento agudo de demanda cardíaca (ejercicio, estrés, fiebre).
- Mecanismo:
- Descenso del gradiente de oxígeno arterial a tejido miocárdico.
- Alteración de fosforilación oxidativa y disminución de ATP.
- Acumulación de lactato y iones hidrógeno, reduciendo contractilidad miocárdica.
- Consecuencia: Síntomas isquémicos y disfunción ventricular, inicialmente reversible si se restaura flujo.
-
5. Necrosis miocárdica (exclusiva de IAMSEST)
- Definición: Muerte irreversible de células musculares por hipoxia prolongada.
- Localización: Zona distal a la obstrucción arterial, con extensión variable según gravedad y tiempo.
- Mecanismo:
- Pérdida de integridad membrana celular.
- Liberación de proteínas intracelulares, como troponinas, al espacio extracelular y sangre.
- Consecuencia: Daño tisular irreversible y posible compromiso permanente de función contráctil.
-
6. Inestabilidad eléctrica y arritmias
- Definición: Alteración en la conducción eléctrica por afectación de los potenciales de acción.
- Localización: Miocitos en zona isquémica y adyacentes.
- Mecanismo:
- Acidosis intracelular y desequilibrio iónico afectan canales de Na+, K+ y Ca2+.
- Propagación anómala del impulso eléctrico, facilitando focos de reentrada.
- Consecuencia: Mayor vulnerabilidad a arritmias ventriculares, con impacto en la función hemodinámica.
🔗 Integración funcional
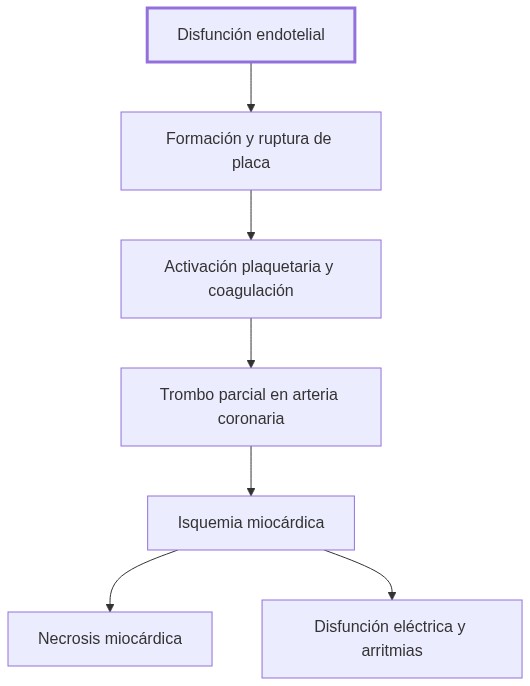
El síndrome coronario integra una cadena de eventos interdependientes, desde la disfunción endotelial hasta la lesión miocárdica y sus manifestaciones clínicas. La progresión típica es:
- Inicio: Disfunción endotelial inducida por factores de riesgo y procesos inflamatorios, que facilita la formación y desestabilización de placas ateroscleróticas.
- Desencadenamiento: Ruptura o erosión de la placa expone componentes trombogénicos, activando plaquetas y coagulación.
- Obstrucción funcional: Trombos parciales provocan episodios transitorios de isquemia, generando angina inestable.
- Desequilibrio aporte-demanda: Un balance negativo induce hipoxia, disfunción contráctil y, eventualmente, necrosis.
- Respuesta adaptativa: El metabolismo cambia de aeróbico a anaeróbico para tolerar isquemia breve; si persiste, ocurre daño celular y liberación de biomarcadores.
- Disfunción eléctrica secundaria: El entorno isquémico facilita arritmias, acrecentando la disfunción cardíaca.
Estos procesos raramente ocurren aislados. En IAMSEST, la duración y gravedad de la isquemia determinan la extensión de necrosis. En angina inestable, la isquemia suele ser breve y reversible, aunque con riesgo de progresión.
La integridad funcional cardíaca depende de la localización de la lesión arterial, la extensión del área isquémica, la capacidad vasodilatadora y la reserva metabólica miocárdica.
🔬 Métodos y evidencias
El conocimiento de la fisiopatología del síndrome coronario se basa en evidencias obtenidas mediante técnicas estructurales, celulares y funcionales:
- Histología vascular post mortem: Examina composición y estabilidad de placas, identificando rupturas, trombosis y sangrados.
- Imágenes coronarias: Angiografía, tomografía y ecografía intravascular evidencian localización y severidad de placas y trombos, correlacionando con perfusión miocárdica.
- Biomarcadores: Troponinas cardiacas indican lesión celular y necrosis, diferenciando IAMSEST de angina inestable.
- Electrofisiología: Monitoreo eléctrico del corazón muestra alteraciones del ritmo relacionadas con la gravedad y extensión de la isquemia.
🩺 Puente clínico
La fisiopatología del síndrome coronario sin elevación del ST explica manifestaciones clínicas a través del desequilibrio entre aporte y demanda de oxígeno, afectando músculo cardíaco y sistema de conducción:
- Dolor torácico: Acumulación de metabolitos isquémicos estimula terminaciones nerviosas, generando angina. Su persistencia o recurrencia indica isquemia.
- Alteraciones electrocardiográficas: Cambios como depresión transitoria del ST o inversión de onda T reflejan afectación eléctrica reversible del miocardio isquémico.
- Marcadores de necrosis: La liberación de troponinas es detectable en IAMSEST, no en angina inestable, reflejando daño irreversible únicamente en el primero.
Estos vínculos entre estructura y función sustentan el razonamiento clínico y permiten diferenciar variantes del síndrome coronario.
💎 Perlas de alto rendimiento
- El síndrome coronario sin elevación persistente del ST: incluye infarto no transmural y angina inestable, con diferente manifestación de necrosis.
- La ruptura o erosión de placas: inicia activación plaquetaria y formación de trombos frecuentemente no oclusivos.
- El desbalance entre aporte y demanda de oxígeno: es clave en la generación de isquemia y síntomas.
- La disfunción endotelial: favorece vasoespasmo y trombosis, agravando el compromiso del flujo coronario.
- El cambio metabólico del miocito hacia glucólisis anaeróbica: reduce ATP y contribuye a disfunción contráctil.
- La isquemia intermitente por obstrucción parcial: puede generar síntomas fluctuantes y daño acumulativo.
- El vasoespasmo: puede presentarse en arterias con mínimas placas, exacerbando la isquemia.
- La alteración iónica debida a metabolitos ácidos: predispone a arritmias ventriculares en zonas isquémicas.
🧠 Puntos clave
- El SCASEST se produce por isquemia: causada por trombosis no oclusiva o vasoespasmos sobre arterias coronarias lesionadas.
- La necrosis celular diferencia al IAMSEST: de la angina inestable, que no presenta daño irreversible.
- La disfunción endotelial e inestabilidad de placa: son eventos iniciales en el mecanismo del síndrome coronario.
- El desequilibrio entre la demanda y el aporte de oxígeno: es fundamental para la generación de isquemia.
- La activación plaquetaria y de la coagulación: ocurre en zonas de ruptura o erosión de la placa aterosclerótica.
- Las alteraciones en la conductancia iónica durante la isquemia: predisponen a fenómenos eléctricos anormales como las arritmias.
❓ Preguntas frecuentes
¿Cómo puede aparecer isquemia miocárdica sin obstrucción completa de la arteria coronaria?
Un trombo parcial o un vasoespasmo puede reducir suficientemente el diámetro luminal, disminuyendo el flujo sanguíneo por debajo de las necesidades del miocardio, especialmente bajo estrés o aumento de la demanda.
¿Cuál es la diferencia fisiopatológica entre IAMSEST y angina inestable?
En IAMSEST, la isquemia es prolongada y grave, causando necrosis celular detectable por troponinas; en angina inestable, la isquemia es reversible y breve, sin daño celular irreversible ni elevación de biomarcadores.
¿Por qué una misma placa aterosclerótica puede generar diferentes síndromes coronarios?
La gravedad y duración de la obstrucción que cause, el tipo y tamaño del trombo, la presencia de vasoespasmo y la actividad fibrinolítica local determinan si la isquemia es reversible o progresa a necrosis.
¿Qué papel tiene la disfunción endotelial en este proceso?
El endotelio regula el tono vascular y evita la trombosis. Su disfunción permite vasoconstricción, adhesión plaquetaria y exposición de matriz trombogénica tras la ruptura de placa.
¿Cuál es la relevancia del metabolismo anaeróbico en el daño isquémico miocárdico?
Frente a hipoxia, el miocito utiliza glucólisis anaeróbica para producir energía, proceso menos eficiente y que genera lactato, provocando acidosis y disminución de la contractilidad; prolongado, conduce a necrosis.
¿Por qué la angina inestable no eleva los marcadores de necrosis miocárdica?
Porque la isquemia es insuficiente para dañar irreversiblemente las membranas celulares, impidiendo la liberación de proteínas intracelulares al torrente sanguíneo.
¿Cómo se reflejan los cambios eléctricos en el electrocardiograma respecto a la fisiopatología?
Cambios transitorios en el segmento ST y la onda T reflejan alteraciones en los potenciales de membrana por desequilibrio iónico y daño eléctrico relacionado con la isquemia aguda.
Evaluación Interactiva Progresiva
Este cuestionario evalúa el conocimiento sobre la fisiopatología biológica del síndrome coronario sin elevación persistente del segmento ST.
Nivel 1 – Básico
¿Qué caracteriza al síndrome coronario agudo sin elevación persistente del segmento ST (SCASEST)?
¿Dónde ocurre la formación principal de la placa aterosclerótica en el síndrome coronario?
¿Cuál es la función principal del endotelio vascular en las arterias coronarias?
Nivel 2 – Intermedio
Según el artículo, ¿qué relación es correcta entre la ruptura o erosión de placas ateroscleróticas y la formación del trombo?
¿Cuál es la diferencia fisiopatológica entre IAMSEST y angina inestable según el artículo?
¿Cuál de las siguientes relaciones estructura-función es correcta en el contexto de la isquemia miocárdica?
Nivel 3 – Avanzado
¿Cuál es la secuencia correcta de eventos fisiopatológicos desde la disfunción endotelial hasta la necrosis miocárdica en el síndrome coronario sin elevación del ST?
Si la activación plaquetaria y la cascada de coagulación son exageradas, ¿qué consecuencia se espera según el artículo?
¿Cómo contribuyen los cambios iónicos y el ambiente ácido intracelular a las arritmias en la isquemia miocárdica según el texto?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.