⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
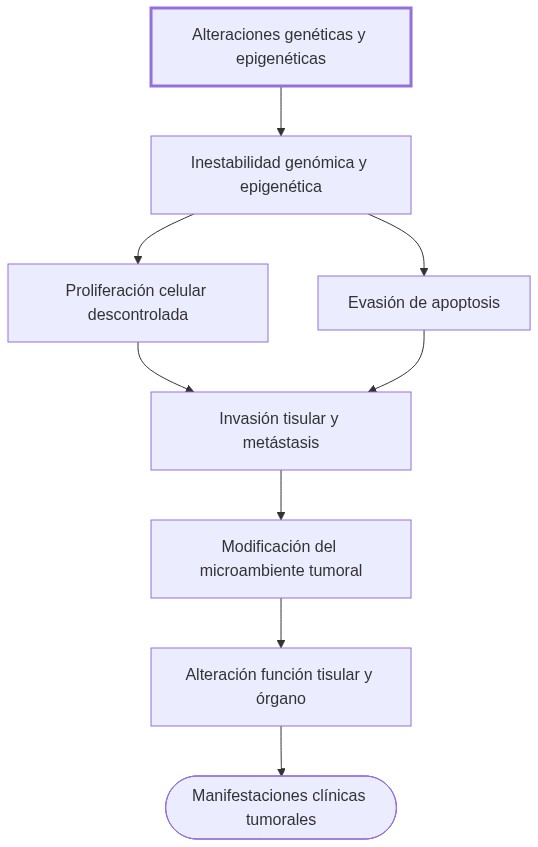
Los mecanismos celulares del cáncer implican alteraciones genéticas y epigenéticas que desregulan la proliferación, evaden la apoptosis y modifican el microambiente tumoral, originando un crecimiento maligno descontrolado y heterogéneo.
🧬 Concepto base
El cáncer es un proceso celular en el que mutaciones y cambios en la regulación génica transforman células normales en malignas, capaces de proliferar sin control y evadir la muerte programada.
⚙️ Mecanismo clave
Mutaciones en oncogenes y supresores del ciclo celular causan proliferación incontrolada, mientras que el bloqueo de rutas apoptóticas y la manipulación del microambiente promueven supervivencia y expansión tumoral.
🔗 Por qué es importante
Estos mecanismos garantizan la persistencia y agresividad del tumor, condicionando su capacidad para invadir tejidos y evitar controles inmunitarios naturales.
🎯 Puntos que suelen preguntarse en examen
- ¿Cómo afecta la mutación de oncogenes al ciclo celular?
- ¿Qué papel juegan las mitocondrias en la apoptosis cancerosa?
- ¿Por qué la inestabilidad genómica favorece la progresión tumoral?
- ¿Cómo modula el microambiente la angiogénesis tumoral?
- ¿Qué mecanismos permiten la evasión de la muerte celular programada?
- ¿Qué efecto tiene la alteración en la señalización intracelular?
Palabras clave: mecanismos celulares del cáncer, proliferación celular, apoptosis, oncogenes, microambiente tumoral, inestabilidad genómica, señalización celular, transformación maligna
Los mecanismos celulares del cáncer abarcan alteraciones genéticas y epigenéticas que desorganizan procesos celulares esenciales, como la proliferación, la muerte programada y la comunicación entre células y entorno. Estas alteraciones son responsables de transformar una célula normal en una célula maligna, capaz de crecer sin restricción, evadir sistemas de control interno, y originar un tejido tumoral.
Analizar estos mecanismos ofrece a los estudiantes de medicina una visión profunda sobre cómo los cambios microscópicos dan lugar a las características conocidas del cáncer y refuerzan el razonamiento biomédico en torno a la biología tumoral.
🧠 Idea central
El cáncer surge como resultado de anomalías acumuladas en los sistemas fisiológicos que regulan el comportamiento celular. Estas anomalías operan en el nivel molecular y afectan principalmente a la proliferación celular (capacidad de multiplicarse), la controlabilidad del ciclo celular y la muerte programada o apoptosis.
Desde el punto de vista biológico, la célula normal depende de una red de reguladores internos y señales externas para mantener el equilibrio entre división y muerte. Cuando estos mecanismos de control se alteran, las células pierden su capacidad de responder a limitaciones naturales de crecimiento, lo cual es esencial en la transformación maligna.
La progresión tumoral se acompaña de la pérdida de regulación sobre la proliferación, invasión a tejidos adyacentes, y eventualmente, diseminación a sitios distantes (metástasis).
Comprender los mecanismos celulares del cáncer proporciona una plataforma para el análisis crítico de la biología tumoral, permite identificar puntos clave en la transformación de la célula normal a la maligna y da sustento a la interpretación de fenómenos histológicos y clínicos.
🌍 Contexto y alcance
Los mecanismos celulares del cáncer deben considerarse como procesos complejos y multietapa situados en el nivel celular, pero profundamente influenciados por interacciones moleculares dentro y fuera de la célula. En el núcleo del problema se encuentran alteraciones en el ADN (a nivel genético) y en patrones de regulación de la expresión génica (a nivel epigenético).
Sin embargo, este fenómeno no es solo una cuestión de mutaciones aisladas. La biología tumoral implica:
- La acumulación de cambios: en proteínas reguladoras y sus interacciones.
- La cooperación: entre diferentes compartimentos celulares: núcleo, citoplasma, membrana y orgánulos.
- La relación dinámica: entre las células tumorales y su microambiente, formado por células no malignas, matriz extracelular, vasos sanguíneos e interacciones inmunitarias.
El enfoque del estudio integra conocimientos provenientes de biología celular, fisiología y patología para descifrar cómo estos procesos convergen y dan lugar a la formación y comportamiento heterogéneo de los tumores.
Abordar el cáncer desde esta perspectiva permite entender que el tejido tumoral es un ecosistema complejo en el que las células malignas coexisten y modifican su entorno para favorecer su propia supervivencia.
🧬 Estructuras clave
El cáncer se desarrolla a partir de alteraciones estructurales y funcionales en compartimentos definidos de la célula. Señalar cuáles son y cómo intervienen es esencial para la comprensión integral de la transformación tumoral.
-
Núcleo celular
Qué es: Orgánulo principal que contiene el ADN.
Dónde actúa: En el interior de todas las células nucleadas.
Qué permite: Almacena la información genética e incluye complejos responsables de la replicación del ADN, la transcripción de genes y la reparación de lesiones.
Cómo funciona:- La cromatina, formada por ADN y proteínas, regula el acceso a los genes.
- Las alteraciones como mutaciones o cambios epigenéticos modifican la expresión y función de genes clave.
- Si los sistemas de reparación del ADN fallan ante el daño, las mutaciones persisten y pueden activar mecanismos oncogénicos o suprimir defensas celulares.
-
Membrana plasmática
Qué es: Barrera lipídica que rodea y define el contorno celular.
Dónde actúa: En la periferia de la célula.
Qué permite: Define límites célula-entorno y alberga proteínas receptoras que detectan señales químicas externas, regulando crecimiento y supervivencia.
Cómo funciona:- Los receptores de factores de crecimiento se insertan en la membrana y, al activarse, disparan vías de señalización que pueden promover división celular.
- Alteraciones estructurales o funcionales en estos receptores perpetúan señales proliferativas aún en ausencia de estímulos normales.
-
Mitocondrias
Qué es: Orgánulos encargados de la producción de energía celular (síntesis de adenosín trifosfato, ATP).
Dónde actúan: En el citoplasma celular.
Qué permite: Orquestan el metabolismo energético y participan en la regulación de la apoptosis.
Cómo funciona:- En condiciones normales, la apoptosis requiere la liberación de factores pro-apoptóticos desde las mitocondrias.
- En células cancerosas, se alteran estos mecanismos mitocondriales y las rutas de señalización asociadas, impidiendo así la muerte celular programada.
-
Complejos proteicos de señalización
Qué son: Conjuntos de proteínas, incluidas cinasas, factores de crecimiento, factores de transcripción y moduladores citoplasmáticos.
Dónde actúan: En la membrana, citoplasma y núcleo.
Qué permiten: Transmiten señales externas al núcleo, coordinando respuestas celulares.
Cómo funcionan:- Las cascadas de fosforilación amplifican la señal inicial hacia el interior celular.
- La persistencia o hiperactivación de estas vías, por mutaciones o sobreexpresión, sostiene una proliferación incesante o evita la apoptosis.
-
Microambiente tumoral
Qué es: Entorno inmediato que rodea a las células cancerosas, compuesto por células inmunitarias, fibroblastos, vasos sanguíneos y matriz extracelular.
Dónde actúa: A nivel de tejidos tumorales.
Qué permite: Modula el crecimiento tumoral, el acceso a nutrientes y oxígeno, así como la interacción con el sistema inmunológico.
Cómo funciona:- El microambiente facilita la angiogénesis (formación de nuevos vasos sanguíneos), suministrando nutrientes que promueven el crecimiento tumoral.
- Ayuda a las células cancerosas a evadir la vigilancia inmunitaria a través de mediadores solubles y contacto celular directo.
⚙️ Funciones y procesos
Los mecanismos celulares responsables del cáncer surgen de la alteración de funciones fundamentales que regulan el comportamiento celular. A continuación se detallan los procesos clave, cada uno se desarrolla según entidades biológicas específicas y su interacción.
-
Proliferación celular descontrolada
- Qué es: Aumento constante en el número de células por división mitótica.
- Dónde actúa: En tejidos y órganos de origen tumoral.
- Qué la produce: Disminución de controles sobre el ciclo celular, hiperactividad de señales mitogénicas.
- Cómo funciona:
- La activación aberrante de receptores de crecimiento eleva continuamente las señales que favorecen la entrada y progresión por el ciclo celular.
- Eliminación de restricciones debidas a genes supresores lleva a una multiplicación sin freno.
-
Evasión de la apoptosis (muerte celular programada)
- Qué es: Incapacidad de llevar a cabo la autodestrucción ordenada ante daño genético severo.
- Dónde actúa: Dentro de células individuales afectadas por mutaciones o estrés celular.
- Qué permite: Sobrevivencia anómala de células con alteraciones que normalmente habrían sido eliminadas.
- Cómo funciona:
- La activación de vías anti-apoptóticas o inhibición de factores pro-apoptóticos bloquea la secuencia que conduce a la muerte celular.
- Las mitocondrias, esenciales en la apoptosis, dejan de liberar señales destructivas por la acción de proteínas alteradas en cáncer.
-
Alteraciones en la señalización intracelular y comunicación intercelular
- Qué es: Cambios en la transmisión de señales químicas esenciales para el destino celular.
- Dónde actúa: Receptores de membrana, citoplasma y núcleo.
- Qué produce: Desregulación de la entrada y salida del ciclo celular, evasión de señales inhibitorias y manipulación del entorno.
- Cómo funciona:
- Mutaciones en genes que codifican receptores o proteínas asociadas mantienen activadas vías de señalización (ej. MAPK, PI3K/AKT) incluso en ausencia de estímulos fisiológicos.
- Las células cancerosas liberan factores que inducen el reclutamiento de células normales para apoyar su crecimiento y evasión inmunológica.
-
Inestabilidad genómica y epigenética
- Qué es: Propensión aumentada a adquirir mutaciones y modificar la expresión génica de manera reversible.
- Dónde actúa: Núcleo (nivel ADN y cromatina).
- Qué produce: Acumulación de errores hereditarios y flexibilidad adaptativa frente a cambios del entorno tumoral.
- Cómo funciona:
- La pérdida o alteración de enzimas reparadoras del ADN aumenta la tasa de errores durante la replicación celular.
- Modificaciones en metilación del ADN y cambios en cromatinas alteran la activación o inhibición de genes, permitiendo rasgos malignos según sea necesario.
-
Invasión tisular y potencial metastásico
- Qué es: Capacidad de atravesar barreras tisulares y colonizar sitios distantes.
- Dónde actúa: Membrana basal y matriz extracelular del tejido de origen; vasos linfáticos y sanguíneos.
- Qué produce: Expansión del tumor más allá de su sitio inicial y establecimiento en nuevos órganos.
- Cómo funciona:
- Las células malignas secretan enzimas, como metaloproteinasas, que degradan matrices y permiten el paso a través de barreras extracelulares.
- Una vez en el torrente sanguíneo, se adhieren y penetran en nuevos tejidos, donde pueden proliferar si el microambiente lo permite.
-
Alteraciones metabólicas (efecto Warburg y adaptación metabólica)
- Qué es: Cambio en la forma de producir energía, favoreciendo la glucólisis aeróbica sobre la respiración mitocondrial normal.
- Dónde actúa: Citoplasma y mitocondrias.
- Qué produce: Producción rápida de ATP y generación de precursores para síntesis biomolecular, facilitando crecimiento y multiplicación acelerados.
- Cómo funciona:
- Las células cancerosas pueden convertir glucosa en lactato aun en presencia de oxígeno (efecto Warburg), permitiendo una rápida incorporación de carbono para nuevas moléculas celulares.
- La reorganización metabólica apoya la resistencia al estrés y la adaptabilidad del tejido tumoral.
-
Interacción con el microambiente tumoral
- Qué es: Relación compleja entre células tumorales y las células del entorno inmediato (inmunitarias, endoteliales, fibroblastos, matriz extracelular).
- Dónde actúa: En el tejido tumoral y su periferia.
- Qué permite: Promover angiogénesis, evasión inmunitaria y soporte estructural.
- Cómo funciona:
- Las células cancerosas secretan factores pro-angiogénicos que inducen la formación de nuevos vasos sanguíneos y proveen oxígeno y metabolitos necesarios para la expansión tumoral.
- Interactúan con células inmunitarias para inhibir su función o reclutar aquellas que facilitan la progresión del cáncer.
🔗 Integración funcional
La transformación cancerosa es la suma dinámica de múltiples mecanismos y estructuras, interconectados en una red que refuerza la supervivencia y expansión tumoral. Cada alteración impulsa a las demás, creando un círculo vicioso de disfunción progresiva.
Por ejemplo, un daño persistente en el ADN localizado en el núcleo puede derivar en la activación de oncogenes y la pérdida de función de genes supresores, lo que conduce a la proliferación incontrolada.
Paralelamente, el mal funcionamiento de la apoptosis, mediado en gran parte por las mitocondrias y sus proteínas reguladoras, permite la supervivencia de células dañadas.
Si estas células además desarrollan habilidades para manipular su entorno microambiental —por ejemplo, secretando factores que favorecen la angiogénesis o suprimen la respuesta inmunitaria— el tumor adquiere cohesión y autonomía.
Este proceso multifactorial se resume en:
- La alteración estructural: (como mutaciones en la membrana o el núcleo) habilita la comunicación aberrante con el medio.
- El microambiente tumoral: lejos de ser pasivo, es moldeado activamente por las células malignas para satisfacer sus propias necesidades metabólicas, nutritivas e inmunológicas.
- La cooperación entre vías de señalización alteradas y cambios metabólicos: refuerza la robustez del fenotipo tumoral.
Así, la biología del cáncer implica un entramado integrado donde ninguna alteración actúa de manera independiente. La suma de estos procesos determina la diversidad clínica y biológica observada en los tumores.
🔬 Métodos y evidencias
El análisis de los mecanismos celulares del cáncer se fundamenta en metodologías dirigidas a identificar alteraciones moleculares, estructurales y funcionales en células y tejidos tumorales.
-
Análisis de mutaciones y epigenética
Qué es: Detección de cambios en la secuencia de ADN y en la regulación de la expresión génica.
Métodos:- Secuenciación de ADN para identificar mutaciones específicas en oncogenes y genes supresores de tumores.
- Técnicas de inmunohistoquímica y microarrays para analizar metilaciones y modificaciones en histonas.
-
Estudios de expresión génica y proteómica
Qué es: Medición de niveles de expresión de ARN y proteínas en células normales versus cancerosas.
Métodos:- Reacciones en cadena de la polimerasa (PCR) cuantitativa para ARN mensajero.
- Electroforesis, inmunoblotting (Western blot) y espectrometría de masas para análisis de proteínas y vías alteradas.
-
Microscopía y análisis morfológico
Qué es: Visualización directa de células tumorales y su microambiente.
Métodos:- Microscopía óptica y electrónica para observar la arquitectura nuclear, cambios en la relación núcleo-citoplasma, y organización de membranas.
-
Ensayos funcionales in vitro
Qué es: Pruebas para evaluar capacidad de proliferar, resistir la apoptosis o invadir matrices en cultivo.
Métodos:- Ensayos de formación de colonias para medir crecimiento descontrolado.
- Modelos de invasión para estudiar su capacidad de atravesar barreras artificiales.
El conjunto de estos métodos ha permitido identificar que las células cancerosas presentan cambios complejos y coordinados, tanto a nivel interno como en su interacción con el entorno, facilitando así una visión más completa del proceso tumoral y sus múltiples soluciones de adaptación.
🩺 Puente clínico
La comprensión de los mecanismos celulares del cáncer ofrece al estudiante una base estructurada para interpretar los fenómenos fisiopatológicos que subyacen a la biología tumoral. No se trata solo de reconocer el crecimiento anormal en un tejido, sino de ser capaz de explicar cómo la fisiología celular altera la arquitectura y función de los órganos afectados.
Por ejemplo, la proliferación descontrolada explica el aumento de masa y la alteración de la arquitectura tisular; la evasión de la apoptosis se asocia con la presencia de células anómalas persistentes y resistentes a señales normales de muerte; la modulación del microambiente por parte de células cancerosas fundamenta la capacidad tumoral para adaptarse, crecer y superar barreras inmunológicas o físicas.
Este razonamiento permite que el médico relacione observaciones morfológicas (como la invasión tisular o la angiogénesis) y hallazgos clínicos (como la progresión local de un tumor o su capacidad de diseminarse) con mecanismos celulares específicos, mejorando así el análisis de casos y la comprensión de la evolución biológica del cáncer.
💎 Perlas de alto rendimiento
- Activación constante de oncogenes: convierte señales transitorias en comandos de proliferación persistente.
- Pérdida funcional de genes supresores: elimina puntos de control naturales del ciclo celular.
- Inestabilidad genómica: facilita la rápida adaptación de células tumorales frente a microambientes cambiantes.
- Microambiente tumoral modificado: es activamente modificado por las células malignas para favorecer la angiogénesis y suprimir respuestas inmunes.
- Evasión de la apoptosis: depende de la sobreexpresión de proteínas anti-apoptóticas y la inactivación de proteínas pro-apoptóticas mitocondriales.
- Metaloproteinasas: degradan componentes extracelulares, facilitando la invasión y remodelando el microambiente.
- Alteraciones metabólicas: incrementan la producción de precursores para biosíntesis, acelerando el crecimiento tumoral.
- Señalización desregulada en receptores de membrana: puede mantenerse activa incluso sin ligando original, por mutaciones activadoras.
🧠 Puntos clave
- Múltiples alteraciones moleculares: afectan procesos celulares fisiológicos y la interacción con el microambiente.
- Proliferación celular sin control: surge por activación de oncogenes y pérdida de mecanismos inhibitorios normales.
- Evasión de la apoptosis: permite supervivencia de células con daño crítico y contribuye al crecimiento tumoral.
- Inestabilidad genómica: favorece la diversidad celular y adaptabilidad progresiva del tumor.
- Microambiente tumoral moldeado: por las células malignas para favorecer su desarrollo y protegerse de mecanismos inmunológicos.
- Mecanismos alterados refuerzan progresión: Cada mecanismo alterado refuerza a los demás, promoviendo la progresión tumoral y su heterogeneidad funcional.
❓ Preguntas frecuentes
¿Por qué una célula cancerosa puede dividirse indefinidamente?
Porque pierde la regulación normal del ciclo celular y los mecanismos de control, como la inactivación de genes supresores, permitiendo una replicación constante y sostenida.
¿Cómo evitan las células tumorales la muerte celular programada?
Alterando las vías de señalización de la apoptosis, sobreexpresando proteínas que inhiben la muerte y bloqueando la activación mitocondrial de la apoptosis.
¿Qué papel cumple el microambiente en la biología tumoral?
Proporciona soporte estructural, nutricional y señales de protección, ayudando al tumor a adaptarse, crecer y evadir la respuesta inmunológica local.
¿Cómo contribuye la inestabilidad genómica a la progresión del cáncer?
Favorece la acumulación de mutaciones y variaciones en la expresión génica, permitiendo adaptación rápida a presiones del entorno, incluidos desafíos inmunológicos y falta de nutrientes.
¿Por qué el metabolismo de la célula cancerosa es diferente al de la célula normal?
Porque adopta rutas metabólicas menos eficientes energéticamente pero más rápidas, generando precursores moleculares vitales para su crecimiento acelerado (por ejemplo, el efecto Warburg).
¿En qué estructuras ocurren la mayoría de las alteraciones iniciales del cáncer?
Principalmente en el núcleo a nivel genético y epigenético, aunque la membrana y orgánulos como las mitocondrias participan en funciones alteradas.
¿Qué mecanismos explican la capacidad de invasión y metástasis de los tumores?
La secreción de enzimas que degradan matrices extracelulares, alteraciones en proteínas de adhesión y la interacción anómala con vasos sanguíneos y tejidos distantes.
¿Por qué es esencial analizar el cáncer como un ecosistema y no solo como células anormales?
Porque la evolución tumoral depende tanto de alteraciones internas de las células malignas como de su capacidad para modificar y manipular su entorno, logrando ventajas cooperativas que favorecen la progresión y supervivencia tumoral.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión de los mecanismos celulares y procesos biológicos involucrados en el cáncer según el artículo proporcionado.
Nivel 1 – Básico
¿Qué función principal cumple el núcleo celular en el contexto del cáncer según el artículo?
¿Cuál es una función de la membrana plasmática en las células cancerosas según el texto?
¿Qué proceso describe la “evasión de la apoptosis” en las células cancerosas?
Nivel 2 – Intermedio
Según el artículo, ¿qué relación es correcta entre el microambiente tumoral y el crecimiento celular maligno?
¿Cuál es la diferencia fundamental entre alteraciones genéticas y epigenéticas en cáncer según el artículo?
Según el texto, ¿qué papel cumplen las mitocondrias en la regulación de la apoptosis alterada en células cancerosas?
Nivel 3 – Avanzado
Si las enzimas reparadoras del ADN fallan persistentemente en una célula, según el artículo, ¿qué consecuencia funcional puede esperarse en la progresión del cáncer?
¿Cómo integran las alteraciones metabólicas y la señalización desregulada el fenotipo tumoral según el artículo?
Según el texto, ¿qué efectos tiene la interacción activa entre células malignas y su microambiente en la progresión tumoral?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.