⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
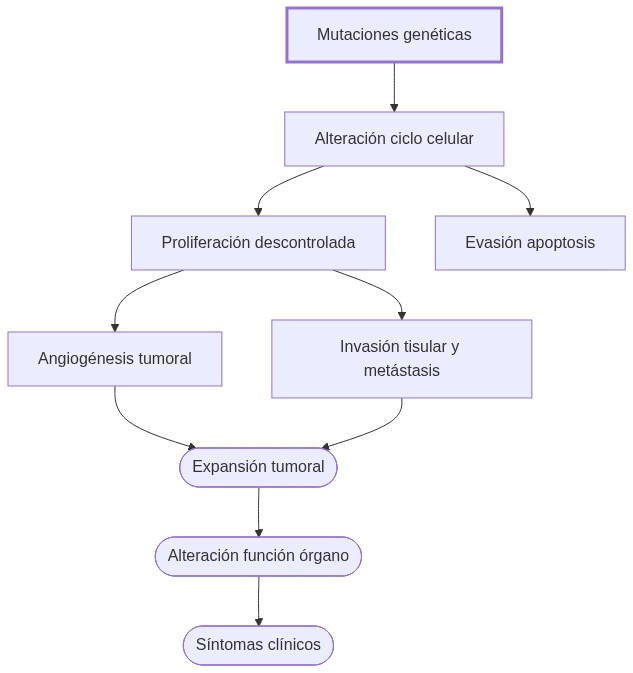
El tratamiento del cáncer se basa en controlar los mecanismos celulares y moleculares que provocan proliferación descontrolada, evasión de apoptosis y alteraciones en la señalización intracelular. Estas disrupciones permiten la expansión tumoral, angiogénesis y metástasis, comprometiendo la función tisular normal.
🧬 Concepto base
El cáncer es una entidad biológica caracterizada por crecimiento celular desregulado y capacidad invasiva, resultado de mutaciones en genes y alteración de la regulación del ciclo celular y apoptosis.
⚙️ Mecanismo clave
Mutaciones en puntos de control del ciclo celular y vías de señalización hiperactivas generan proliferación continua; la inhibición de apoptosis y cambios en el microambiente tumoral facilitan supervivencia, angiogénesis y diseminación metastásica.
🔗 Por qué es importante
Estas alteraciones causan pérdida de homeostasis tisular y permiten que el tumor progrese, afectando función orgánica y favoreciendo la invasión de tejidos y órganos distantes.
🎯 Puntos que suelen preguntarse en examen
- ¿Cómo impactan las mutaciones en puntos de control celular en la proliferación?
- Rol de la apoptosis en la prevención de acumulación celular anómala.
- Importancia del microambiente tumoral en angiogénesis e invasión.
- Mecanismos de señalización alterados que promueven supervivencia celular.
- Procesos clave que permiten la metástasis de células cancerosas.
- Relación entre mutaciones genéticas y resistencia a la muerte celular.
Palabras clave: tratamiento del cáncer, ciclo celular, apoptosis, angiogénesis, metástasis, mutaciones, microambiente tumoral, señalización intracelular
El tratamiento del cáncer se fundamenta en el conocimiento minucioso de los mecanismos celulares y moleculares que regulan el crecimiento y la diferenciación celular. Comprender cuáles son los procesos que permiten a las células cancerosas romper con la regulación normal es esencial para entender por qué los tumores surgen, invaden tejidos y afectan la función fisiológica.
La base biológica de este fenómeno facilita la interpretación de cómo iniciativas dirigidas a restablecer el control sobre esas funciones, o a eliminar células alteradas, pueden impactar el curso de la enfermedad.
🧠 Idea central
El cáncer consiste en un conjunto de alteraciones biológicas cuya consecuencia final es el crecimiento celular descontrolado y la capacidad de invadir tejidos circundantes o diseminarse a lugares distantes. Esto ocurre cuando se pierde el equilibrio normal en la regulación del ciclo celular, la diferenciación y la reparación tisular. Los mecanismos celulares involucrados incluyen cambios en los controles de ciclo, mutaciones en los genes reguladores, y modificaciones en la señalización local e intracelular.
En términos biológicos, el proceso de cáncer desafía la homeostasis fundamental que permite que las células proliferen solo cuando es necesario y en respuesta a condiciones fisiológicas. Al entender los mecanismos por los cuales las células malignas evaden estos controles, se comprende cómo pueden expandirse, invadir o diseminarse, y cómo estos mismos mecanismos constituyen blancos potenciales para controlar el crecimiento tumoral o restaurar la función normal.
Todo abordaje eficaz para el tratamiento del cáncer requiere, entonces, una visión detallada de los eventos secuenciales que ocurren desde la transformación de una célula normal en maligna hasta la alteración estructural y funcional de los tejidos afectados.
🌍 Contexto y alcance
El estudio del tratamiento del cáncer desde una perspectiva biológica abarca distintos niveles organizativos e involucra la interacción entre múltiples sistemas:
- Células individuales: En el núcleo y el citoplasma ocurren las mutaciones y desregulaciones que permiten a ciertas células abandonar los límites normales de proliferación.
- Orgánulos: Mitocondrias, retículo endoplasmático y aparato de Golgi participan en la transducción de señales y ejecución de programas de muerte o supervivencia celular.
- Microambiente tumoral: Incluye células no neoplásicas (como fibroblastos, macrófagos y células endoteliales), matriz extracelular y gradientes de oxígeno y nutrientes. Estos componentes modulan la proliferación y la respuesta inflamatoria.
- Sistemas fisiológicos: Elementos del sistema inmunitario, hormonal, nervioso y vascular condicionan tanto el crecimiento como la restricción del tumor, a través de señales locales o sistémicas.
El tratamiento del cáncer implica por tanto la comprensión de cómo las alteraciones en la comunicación entre estos componentes dan lugar a una progresión tumoral que excede los límites normales del cuerpo.
🧬 Estructuras clave
-
Núcleo celular: En el núcleo residen los cromosomas, compuestos por ADN, donde se producen mutaciones genéticas y cambios epigenéticos.
¿Qué es? Organelo delimitado por una envoltura nuclear.
¿Dónde actúa? Dentro de las células del tejido afectado.
¿Qué permite? Controla la transcripción génica y guarda la información hereditaria.
¿Cómo funciona? Almacena y expresa genes; mutaciones en oncogenes o genes supresores de tumores modifican la proliferación.
¿Qué ocurre si se altera? Si el ADN o su regulación se ven comprometidos, se favorece la transformación neoplásica. -
Ciclo celular y puntos de control: Son secuencias de fases (G1, S, G2, M) reguladas por complejos ciclinas-cinasas dependientes de ciclinas (CDK).
¿Qué es? Serie ordenada de eventos que culmina con la división celular.
¿Dónde actúa? En todas las células que pueden proliferar.
¿Qué permite? Asegura que las células se dividan solo cuando el ADN está intacto y las condiciones son favorables.
¿Cómo funciona? Mediante controles como el checkpoint G1/S (verifica daño en el ADN antes de la replicación) y G2/M (verifica integridad antes de mitosis).
¿Qué ocurre si se altera? Si los checkpoints fallan por mutaciones, la célula puede dividirse pese a errores genéticos. -
Mitocondrias: Orgánulos responsables de la respiración celular y la iniciación de la apoptosis.
¿Qué es? Organelo citoplasmático con doble membrana.
¿Dónde actúa? En el citoplasma de todas las células.
¿Qué permite? Produce energía y regula señales de muerte celular.
¿Cómo funciona? La liberación de citocromo c desde la mitocondria inicia cascadas de apoptosis.
¿Qué ocurre si se altera? Alteraciones en sus membranas pueden inhibir apoptosis, facilitando la supervivencia tumoral. -
Membrana plasmática y receptores: Incluye proteínas transportadoras, receptores de factores de crecimiento y canales iónicos.
¿Qué es? Barrera lipídica que delimita la célula.
¿Dónde actúa? En la periferia celular.
¿Qué permite? Recibe señales del entorno, coordina respuestas a estímulos.
¿Cómo funciona? Receptores como las tirosina quinasas activan vías intracelulares que controlan proliferación y supervivencia.
¿Qué ocurre si se altera? Si hay hiperactivación por mutaciones, estas vías pueden causar proliferación no regulada. -
Microambiente tumoral: Engloba células normales vecinas, matriz extracelular y vasos sanguíneos.
¿Qué es? Entorno tisular donde se asienta el tumor.
¿Dónde actúa? Rodeando y penetrando el tejido neoplásico.
¿Qué permite? Influye en el aporte nutricional, oxigenación y respuesta inmunitaria.
¿Cómo funciona? La vascularización aberrante altera gradientes de oxígeno y favorece la angiogénesis; células inmunitarias pueden facilitar o limitar el crecimiento tumoral.
¿Qué ocurre si se altera? Cambios en el microambiente pueden promover invasión o resistencia a la eliminación tumoral.
⚙️ Funciones y procesos
La transformación de una célula normal a una cancerosa no es un evento simple, sino una secuencia de alteraciones moleculares que afectan funciones esenciales. Detallamos los principales procesos involucrados:
-
Regulación del ciclo celular:
- ¿Qué es? Conjunto de mecanismos que determinan cuándo la célula entra en replicación o pausa.
- ¿Dónde actúa? Núcleo y citoplasma.
- ¿Qué permite? Evita la propagación de células con daño genético.
- ¿Cómo funciona?
- Los checkpoints de G1/S y G2/M verifican integridad del ADN y condiciones externas.
- Las CDK y ciclinas activan o silencian rutas que favorecen o detienen la mitosis.
- Si se activa una anomalía (mutación en, por ejemplo, p53), la célula puede evadir el arresto y seguir dividiéndose.
-
Apoptosis (muerte celular programada):
- ¿Qué es? Proceso ordenado por el cual una célula se autodestruye tras sufrir daño irreparable.
- ¿Dónde actúa? Mitocondria, citosol y núcleo.
- ¿Qué permite? Mantiene el equilibrio celular evitando acumulación de células anómalas.
- ¿Cómo funciona?
- Las vías intrínseca y extrínseca activan caspasas, enzimas que degradan componentes celulares.
- La liberación de citocromo c en la vía intrínseca inicia la cascada de muerte.
- ¿Qué ocurre si se altera? Si la apoptosis es bloqueada (por mutaciones en genes proapoptóticos), las células dañadas persisten y se acumulan, favoreciendo la neoplasia.
-
Señalización molecular intracelular:
- ¿Qué es? Red de vías bioquímicas que traducen estímulos externos en respuestas celulares.
- ¿Dónde actúa? Membrana, citoplasma y núcleo.
- ¿Qué permite? Coordina proliferación, diferenciación y supervivencia.
- ¿Cómo funciona?
- Receptores de membrana (como EGFR) activan cascadas como RAS/RAF/MEK/ERK o PI3K/AKT/mTOR.
- Estas rutas regulan la expresión génica relacionada con el crecimiento y la resistencia a la muerte celular.
- ¿Qué ocurre si se altera? Hiperactivación de estas rutas amplifica señales de proliferación y supervivencia, perpetuando la expansión tumoral.
-
Angiogénesis:
- ¿Qué es? Formación de nuevos vasos sanguíneos a partir de vasos preexistentes.
- ¿Dónde actúa? Tejido tumoral circundante.
- ¿Qué permite? Asegura suministro de oxígeno y nutrientes a células que crecen de forma anormal.
- ¿Cómo funciona?
- Células tumorales secretan factores estimulantes de vasos como VEGF.
- Endotelio vascular responde promoviendo proliferación y migración células endoteliales.
- ¿Qué ocurre si se altera? Un aporte elevado de sangre favorece la expansión y potencia la posibilidad de metástasis a través del torrente sanguíneo.
-
Metástasis:
- ¿Qué es? Capacidad de las células cancerosas para abandonar el sitio original y colonizar tejidos distantes.
- ¿Dónde actúa? Desde el tumor primario hacia vasos linfáticos, sanguíneos y tejidos secundarios.
- ¿Qué permite? Permite que el cáncer comprometa órganos alejados.
- ¿Cómo funciona?
- Las células modifican moléculas de adhesión (como integrinas y cadherinas) para desprenderse del tumor primario.
- Secretan enzimas (por ejemplo, metaloproteinasas) que degradan la matriz extracelular.
- Acceden a vasos, sobreviven en el torrente, se extravasan y crean nuevas colonias en tejidos distantes.
- ¿Qué ocurre si se altera? La desregulación de pasos secuenciales permite la propagación del cáncer a sitios que afectan funciones vitales.
🔗 Integración funcional
El desarrollo del cáncer deriva de la interacción entre mutaciones genéticas, errores en el ciclo celular, evasión de la apoptosis y modificaciones en la comunicación célula-microambiente. El resultado es una ruptura profunda de la coordinación entre estructura y función tisular.
Si una mutación afecta un gen supresor de tumores (como sucede en el núcleo celular), el punto de control celular correspondiente puede volverse ineficaz. Esto, a su vez, facilita que más células proliferen con daño acumulado.
La resistencia a la apoptosis, mediada por proteínas que estabilizan la membrana mitocondrial o suprimen señales proapoptóticas, previene la eliminación de células mutadas, perpetuando la expansión tumoral.
A medida que la masa tumoral crece, se incrementa la demanda de oxígeno y nutrientes, lo que desencadena la angiogénesis. La organización anómala de los nuevos vasos produce áreas de hipoxia y heterogeneidad, condicionando tanto la biología tumoral como la respuesta tisular.
Las interacciones con el microambiente tumoral determinan si las células logran movilidad, discreción inmunológica o capacidad invasiva. Por ejemplo, si la matriz extracelular es degradada, se facilita el paso de células al torrente sanguíneo y la colonización de órganos distantes.
Todo este sistema integrado explica cómo la alteración de un componente (por ejemplo, la función de un receptor de superficie o un factor de transcripción nuclear) repercute en cascada sobre procesos de proliferación, muerte o diseminación, afectando la arquitectura y la función global del tejido involucrado.
🔬 Métodos y evidencias
Los conocimientos acerca de la biología del cáncer se han construido a través de una variedad de aproximaciones experimentales y observacionales, cada una dirigida a un nivel diferente de organización:
-
Estudios moleculares de mutaciones y expresión génica:
¿Qué permiten? Identifican alteraciones en secuencias de ADN o patrones de expresión que pueden actuar como eventos iniciadores del cáncer.
¿Cómo funciona? Se utilizan técnicas como PCR, secuenciación y microarreglos para mapear mutaciones en oncogenes y genes supresores de tumores. -
Análisis de señalización celular:
¿Qué permiten? Revelan alteraciones funcionales en vías bioquímicas responsables del crecimiento y supervivencia.
¿Cómo funciona? Técnicas como Western blot, inmunofluorescencia y ensayos enzimáticos identifican cambios en la activación de proteínas clave. -
Modelos celulares y animales:
¿Qué permiten? Permiten observar la dinámica de proliferación, invasión y respuesta a estímulos.
¿Cómo funciona? El cultivo de células y la inducción de tumores en animales permiten manipular variables y analizar consecuencias sobre el crecimiento y la biología tumoral. -
Evaluación histológica y del microambiente tumoral:
¿Qué permite? Analizar la arquitectura de los tejidos y la composición celular, incluyendo la respuesta inmune.
¿Cómo funciona? Técnicas de tinción, microscopía y marcadores inmunohistoquímicos identifican patrones de infiltrado celular, angiogénesis y remodelado de la matriz.
Todo avance en la comprensión de los mecanismos celulares y moleculares del cáncer se fundamenta en la integración crítica de datos experimentales a estos niveles. Ello permite desentrañar cómo las alteraciones iniciales pueden escalar para provocar la desorganización global del tejido y la pérdida de control fisiológico.
🩺 Puente clínico
El entendimiento de los procesos celulares y moleculares que subyacen al cáncer es esencial para interpretar por qué los tumores no solo proliferan, sino también cómo interactúan con el organismo completo. Estas alteraciones biológicas guían el razonamiento fisiopatológico y explican los hallazgos clínicos más frecuentes.
Por ejemplo, la pérdida de control en el ciclo celular y la evasión de señales proapoptóticas explican la persistencia y el crecimiento progresivo de la masa tumoral. A medida que el tumor expande su necesidad metabólica y vascular, surgen alteraciones en el entorno local (como hipoxia o inflamación crónica). Estas condiciones pueden manifestarse como masas palpables, cambios en la función de un órgano o fenómenos sistémicos derivados de la invasión tumoral.
Comprender el impacto de la angiogénesis aberrante y la metástasis proporciona la base biológica para la interpretación de síntomas relacionados con la diseminación, como obstrucciones, derrames o compromiso multiorgánico. Así, el razonamiento causal que interesa al estudiante de medicina se fundamenta en cómo las mutaciones, la desregulación de vías y los cambios tisulares se traducen fisiológicamente en signos, síntomas y alteraciones funcionales detectables.
💎 Perlas de alto rendimiento
- Alteración en puntos de control: La alteración en los puntos de control del ciclo celular permite que células con daño genético progresen hacia la división.
- Mutaciones en genes supresores: Mutaciones en genes supresores de tumores son determinantes para la pérdida de la regulación proliferativa.
- Evasión de la apoptosis: La evasión de la apoptosis favorece la supervivencia y acumulación de células neoplásicas.
- Señalizaciones intracelulares hiperactivas: Señalizaciones intracelulares hiperactivas pueden desencadenar proliferación continua e independencia de estímulos externos.
- Microambiente tumoral: El microambiente tumoral modula la angiogénesis y la respuesta inmune local, influyendo en la progresión tumoral.
- Angiogénesis tumoral: La angiogénesis tumoral es fundamental para el crecimiento más allá de ciertos límites tisulares.
- Metástasis y barreras biológicas: Para metastatizar, las células deben superar múltiples barreras biológicas mediante cambios en adhesión y migración.
- Mutaciones y resistencia: Las mutaciones en rutas de reparación del ADN condicionan sensibilidad o resistencia a tratamientos dirigidos.
🧠 Puntos clave
- Ciclo celular y puntos de control: El ciclo celular y sus puntos de control son blancos primarios en la transformación neoplásica.
- Mutaciones en genes reguladores: Mutaciones en genes reguladores del crecimiento alteran la homeostasis tisular.
- Interacciones con microambiente: El microambiente tumoral interactúa con células malignas determinando progresión y agresividad.
- Rol de la angiogénesis: La angiogénesis permite que tumores crezcan más allá de límites fisiológicos normales.
- Proceso de metástasis: La metástasis implica un proceso secuencial de escape, invasión y colonización guiado por alteraciones estructurales y funcionales.
- Evasión de apoptosis: La evasión de apoptosis contribuye a la permanencia y expansión de clones celulares aberrantes.
❓ Preguntas frecuentes
¿Cómo se controla normalmente el ciclo celular en las células sanas?
El ciclo celular está regulado por puntos de control (checkpoints) en fases clave. Proteínas como p53 y las ciclinas-cinasas dependientes de ciclinas detectan daño en el ADN o condiciones inadecuadas y detienen el ciclo hasta que se resuelve el problema, previniendo la división anómala.
¿Qué mecanismos favorecen la evasión de la apoptosis en el cáncer?
Mutaciones en genes que regulan la vía apoptótica (como Bcl-2, una proteína antiapoptótica mitocondrial) permiten a la célula evitar programas de muerte incluso ante daño, perpetuando su supervivencia y expansión tisular.
¿Por qué es importante el microambiente tumoral para la progresión del cáncer?
El microambiente provee factores de crecimiento, soporte estructural y modula la respuesta inmunitaria. Las células neoplásicas pueden modificar este entorno para favorecer angiogénesis, invasión y evadir mecanismos defensivos locales.
¿Qué vías de señalización intracelular están comúnmente alteradas en las células cancerosas?
Rutas como PI3K/AKT/mTOR y RAS/RAF/MEK/ERK suelen activarse de forma constitutiva por mutaciones en receptores o proteínas quinasas, promoviendo proliferación y evitando señales de arresto o apoptosis.
¿Cómo influye la angiogénesis en el crecimiento tumoral?
La angiogénesis provee oxígeno y nutrientes para sostener el crecimiento celular anómalo. Sin nuevos vasos sanguíneos, los tumores no pueden superar cierto tamaño y sobreviven regiones hipóxicas que estimulan respuestas adaptativas.
¿Qué papel tienen las mutaciones en la resistencia a tratamientos contra el cáncer?
Las mutaciones pueden producir proteínas alteradas que modifican la respuesta de las células neoplásicas a señales que normalmente inducirían apoptosis o detención, generando resistencia a tratamientos dirigidos.
¿Por qué el estudio del metabolismo celular es relevante en la biología del cáncer?
Las células tumorales reprograman su metabolismo para favorecer la síntesis de macromoléculas y sobrevivir en ambientes pobres en oxígeno, conocido como efecto Warburg, condicionando crecimiento y resistencia al estrés.
¿Cómo contribuyen los modelos experimentales al entendimiento de la biología del cáncer?
Modelos celulares y animales permiten reproducir etapas de la progresión tumoral bajo condiciones controladas, validando hipótesis sobre el rol de genes, vías de señalización y cambios estructurales en la evolución del cáncer.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico y conceptual presentado sobre la biología del cáncer.
Nivel 1 – Básico
¿Qué permite controlar el núcleo celular en las células afectadas por cáncer?
¿Dónde actúan principalmente los puntos de control del ciclo celular, según el texto?
¿Cuál es el papel fundamental de la apoptosis en el contexto del cáncer?
Nivel 2 – Intermedio
¿Cuál de las siguientes relaciones estructura-función es correcta según el artículo?
Según el artículo, ¿qué diferencia principal existe entre la función del punto de control G1/S y G2/M en el ciclo celular?
¿Cuál es un efecto del microambiente tumoral según el artículo?
Nivel 3 – Avanzado
Si hay una mutación que inactiva un gen supresor de tumores en el núcleo, ¿qué consecuencia directa describe el artículo?
¿Cómo afecta la alteración en la membrana mitocondrial según el artículo a la progresión tumoral?
Según el artículo, ¿cuál es la secuencia correcta de eventos en la metástasis en células cancerosas?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.