⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La biopatología neurológica estudia mecanismos celulares, moleculares e inmunitarios que alteran y dañan el sistema nervioso central. Involucra neurodegeneración, inflamación glial, disfunción sináptica y ruptura de barreras que conducen a pérdida estructural y funcional.
🧬 Concepto base
La biopatología neurológica analiza el daño y la disfunción en neuronas, células gliales y barreras tisulares del SNC. Examina cómo estos elementos interactúan con el sistema inmunológico y factores externos para afectar la salud neural.
⚙️ Mecanismo clave
El acúmulo proteico anómalo y la activación persistente de la microglía generan inflamación crónica. Esto causa daño estructural, pérdida sináptica y desmielinización, que culminan en neurodegeneración y déficit funcional irreversible.
🔗 Por qué es importante
Comprender estos mecanismos permite interpretar la progresión y severidad de enfermedades neurológicas desde una base biológica integral y causal.
🎯 Enfoque de examen
- Relación entre acumulación proteica y disfunción neuronal
- Rol de la microglía en inflamación y daño neural
- Importancia de la barrera hematoencefálica en protección y patología
- Mecanismos de desmielinización y pérdida sináptica como precursores del déficit clínico
Palabras clave: biopatología neurológica, neurodegeneración, inflamación glial, microglía, barrera hematoencefálica, proteínas anómalas, desmielinización, sinapsis
La biopatología neurológica examina cómo procesos celulares, moleculares e inmunológicos desencadenan y perpetúan alteraciones en el sistema nervioso central (SNC).
Este estudio integra la comprensión de fenómenos clave como la neurodegeneración, la disfunción inmunitaria y la influencia de factores externos sobre la función neural, estableciendo así las bases para interpretar las enfermedades neurológicas desde una perspectiva biológica integradora.
🧠 Idea central
La biopatología neurológica se fundamenta en el análisis de los mecanismos subyacentes que llevan a la alteración y daño del tejido nervioso.
Incluye el estudio integral de procesos celulares y moleculares que afectan a las neuronas, células gliales y barreras tisulares, así como la interacción con el sistema inmunológico y factores ambientales que impactan el SNC.
La finalidad es esclarecer de qué manera la disfunción de estos mecanismos, como la activación inmune inapropiada o la acumulación de proteínas anómalas, da lugar a inflamación, daño estructural y pérdida funcional en el tejido nervioso.
Esto permite construir una lógica causal en la que cada alteración contribuye a la evolución de patologías neurológicas complejas.
🌍 Contexto y alcance
La biopatología neurológica abarca el estudio sistemático del tejido cerebral y medular, prestando especial atención a las interacciones entre neuronas, células gliales (como astrocitos, oligodendrocitos y microglía) y a los elementos de soporte (vasculatura, barrera hematoencefálica).
Va más allá del análisis de células aisladas, integrando la influencia del sistema inmunológico (neuroinmunología), la dinámica de proteínas patológicas en procesos neurodegenerativos y la contribución de factores externos como el microbioma.
Se busca comprender cómo la suma de factores internos y externos moldea la respuesta del SNC, facilitando el desarrollo, progresión y eventual irreversibilidad de la enfermedad neurológica.
🧬 Estructuras clave
Las principales estructuras implicadas en la biopatología neurológica son:
- Neuronas: Células especializadas para señalización eléctrica y química, susceptibles a daño por acumulación de proteínas anómalas, procesos inflamatorios e hipoxia.
- Células gliales:
- Astrocitos: Regulan el microambiente extracelular y dan soporte metabólico.
- Oligodendrocitos: Forman mielina que aísla los axones y permite transmisión rápida.
- Microglía: Células inmunocompetentes del SNC, esenciales en vigilancia y respuesta inflamatoria.
- Sinapsis: Sitios de comunicación química y eléctrica intercelular, cuyo deterioro afecta la transmisión y plasticidad neural.
- Barrera hematoencefálica (BHE): Estructura que regula el paso de sustancias entre sangre y cerebro, crucial para proteger el tejido neural.
| Estructura | Función principal | Implicancia patológica |
|---|---|---|
| Neurona | Transmisión de impulsos eléctricos y procesamiento de información | Dañada por acúmulo proteico, inflamación y disfunción sináptica |
| Astrocito | Soporte metabólico, regulación iónica y mantenimiento de la BHE | Participa en respuestas reactivas e inflamación; alteraciones afectan la homeostasis |
| Oligodendrocito | Formación y mantenimiento de la mielina axonal | Degeneración da lugar a desmielinización y fallos en la conducción |
| Microglía | Vigilancia inmunitaria y eliminación de residuos celulares | Activación prolongada genera inflamación tisular y neurodegeneración |
| Barrera hematoencefálica | Control del paso molecular sangre–SNC | Disrupción facilita entrada de células inmunes y proteínas nocivas |
| Sinapsis | Transmisión química/electrofisiológica intercelular | Desequilibrio favorece fallo en circuitos, alterando función cognitiva y motora |
⚙️ Funciones y procesos
En la biopatología neurológica, los procesos centrales implican cascadas que vinculan daño inicial, respuesta celular e integración tisular, con evolución temporal y espacial dentro del SNC. Estos mecanismos incluyen:
- Neurodegeneración:
- Definición: Proceso progresivo de disfunción y muerte neuronal.
- Dónde ocurre: Principalmente en neuronas de áreas críticas del cerebro y médula.
- Causa–mecanismo: Acumulación de proteínas anormales (por ejemplo, cuerpos proteicos extracelulares o intraneuronales), generación de radicales libres y activación de vías de muerte celular como apoptosis.
- Consecuencia: Pérdida de neuronas → alteración de circuitos → deterioro funcional persistente.
- Neuroinmunología (respuesta inmunitaria en el SNC):
- Definición: Procesos por los que células gliales, sobre todo microglía, detectan, procesan y responden a señales de daño o invasores externos.
- Dónde: Microambiente cerebral y medular.
- Causa–mecanismo: Cuando detectan señales de peligro, la microglía se activa y libera citocinas proinflamatorias. Si esta respuesta se prolonga, se genera inflamación crónica que contribuye al daño neuronal.
- Consecuencia: Inflamación persistente que amplifica la lesión y favorece la progresión de neurodegeneración.
- Alteración de proteínas y homeostasis:
- Definición: Desbalance en la síntesis, plegamiento y degradación de proteínas neuronales.
- Mecanismo: Formación de agregados proteicos que interfieren con funciones celulares y desencadenan mecanismos citotóxicos.
- Consecuencia: Disfunción sináptica, afectación del transporte axonal y activación de la respuesta inmune local.
- Influencia del microbioma:
- Definición: Impacto de los microorganismos intestinales sobre el SNC.
- Cómo actúa: Modula procesos inmunitarios y metabólicos que pueden favorecer o limitar la neuroinflamación y la vulnerabilidad a daño estructural.
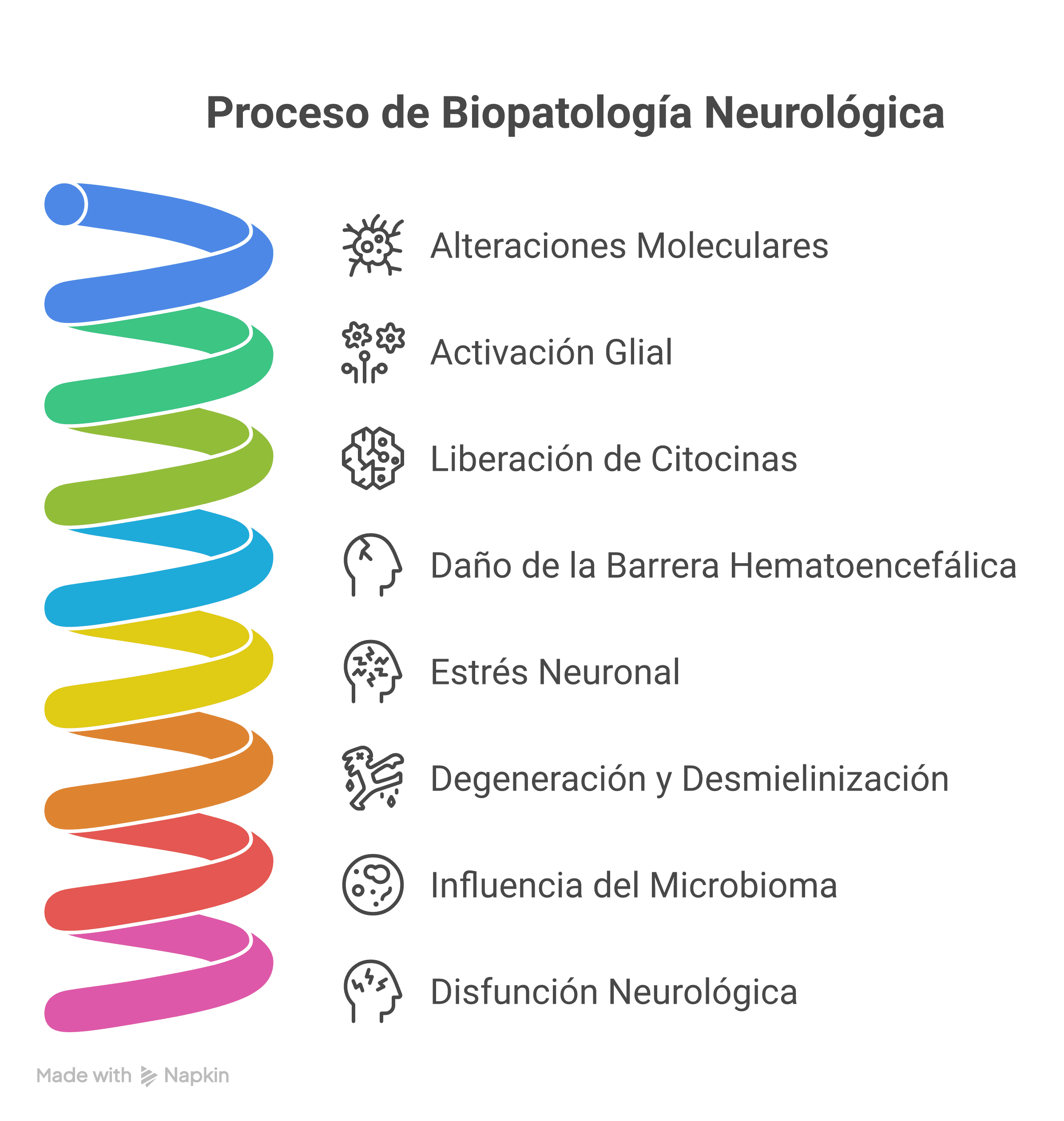
El daño en cualquiera de estos procesos suele seguir una progresión: insulto inicial (por proteínas anómalas, activación inmune o factores externos) → activación glial y mecanismos de defensa → inflamación sostenida → degeneración neuronal y remodelación tisular irreversible.
🔗 Integración funcional
La biopatología neurológica ilustra cómo la interacción entre células y moléculas en el SNC orquesta tanto la resistencia como la vulnerabilidad frente a la enfermedad.
Un ejemplo está en la respuesta inicial de las células gliales al daño: microglía y astrocitos detectan señales de lesión, respondiendo con secreción de mediadores que, en fase aguda, buscan reparar y aislar el daño.
Si los estímulos persisten, se inicia una cascada de inflamación mantenida, donde la microglía cambia su perfil funcional, liberando radicales libres y citocinas tóxicas.
La acumulación de proteínas patológicas y la disfunción de la barrera hematoencefálica amplifican la respuesta lesiva, permitiendo la entrada de factores inmunitarios periféricos y exacerbando la pérdida neuronal.
Finalmente, la alteración sostenida de la comunicación sináptica y del metabolismo neuronal consolida la disfunción clínica, con pérdida de plasticidad, alteración funcional generalizada y déficit irreversible en las áreas cerebrales afectadas.
🔬 Métodos y evidencias
El conocimiento de la biopatología neurológica proviene del uso complementario de técnicas como:
- Estudios histológicos post mortem: Permiten observar patrones de neurodegeneración, acúmulo proteico y cambios en la arquitectura celular.
- Técnicas de imagen: Revelan alteraciones estructurales en áreas neurales, especialmente mediante resonancia magnética y tomografía.
- Análisis bioquímico: Identifican marcadores de inflamación, estrés oxidativo y desregulación proteica en muestras de tejido o líquidos biológicos.
- Modelos celulares y animales: Permiten reproducir y estudiar de manera controlada mecanismos patológicos concretos y su secuencia temporal.
Estos enfoques han sido claves para correlacionar hallazgos moleculares y celulares con estadios de la enfermedad y manifestaciones funcionales, permitiendo afinar la interpretación causal en la biopatología neurológica.
🩺 Puente clínico
Comprender a fondo los mecanismos fundamentales de la biopatología neurológica proporciona bases sólidas para vincular la disfunción clínica con procesos celulares subyacentes concretos.
Por ejemplo, la identificación de inflamación neuroinmune persistente o de acumulación de proteínas aberrantes explica la aparición progresiva de déficits neurológicos, desde cambios en la cognición hasta deterioro motor.
Así, el razonamiento médico se enriquece al reconocer que muchos cuadros neurológicos reflejan la convergencia de vías patológicas como neurodegeneración, inflamación crónica o colapso de la homeostasis, en vez de lesiones aisladas, facilitando una interpretación integral del paciente neurológico.
💎 Perlas de alto rendimiento
- Microglía: es la principal célula inmunitaria residente del SNC y dirige la respuesta inflamatoria ante daño o invasores.
- Neurodegeneración: implica la muerte progresiva de neuronas mediada por acúmulo proteico y estrés oxidativo.
- Barrera hematoencefálica: regula el entorno cerebral; su alteración facilita entrada de células y moléculas proinflamatorias.
- Acúmulo anómalo de proteínas: desencadena cascadas tóxicas que afectan sinapsis y transporte axonal.
- Inflamación crónica sostenida: causada por activación glial amplifica la lesión y acelera la pérdida funcional.
- Oligodendrocitos: mantienen la mielina; su daño conduce a desmielinización y alteración conductiva axonal.
- Microbioma: influye en la susceptibilidad a enfermedades neurológicas a través de la modulación inmunitaria y metabólica.
- Plasticidad neuronal: puede limitar temporalmente el daño clínico, pero se pierde con la progresión patológica.
🧠 Puntos clave
- Mecanismos celulares: La biopatología neurológica integra mecanismos celulares, moleculares e inmunitarios implicados en las enfermedades del SNC.
- Neurodegeneración e inflamación: La neurodegeneración y la inflamación glial sostenida constituyen la base de daños estructurales y funcionales cerebrales.
- Acúmulo proteico: El acúmulo aberrante de proteínas origina toxicidad y degeneración neuronal progresiva.
- Disfunción de barrera: La disfunción de la barrera hematoencefálica amplifica procesos de daño y facilita neuroinflamación mantenida.
- Microbioma: El microbioma influye indirectamente en la salud cerebral mediante la modulación de la respuesta inmune.
- Pérdida sináptica: La pérdida de sinapsis y mielina precede la muerte neuronal irreversible y al déficit funcional.
- Interpretación integral: Comprender estos mecanismos permite una interpretación integral y causal de los trastornos neurológicos.
❓ Preguntas frecuentes
¿Cuál es el papel de la microglía en la patología neurológica?
La microglía detecta señales de daño y desencadena la respuesta inmunitaria local; su activación prolongada puede inducir inflamación crónica y favorecer la neurodegeneración.
¿Cómo afectan las proteínas anómalas a las neuronas?
Las proteínas mal plegadas o mal degradadas se acumulan en las neuronas, interfiriendo con la función sináptica y el transporte axonal, lo que puede activar vías de muerte celular.
¿Por qué es relevante la barrera hematoencefálica en la biopatología neurológica?
La barrera hematoencefálica limita el paso de sustancias dañinas al SNC; su alteración permite la entrada de células inmunitarias y proteínas que potencian la inflamación y el daño neuronal.
¿Qué contribución tiene el microbioma en la patología del sistema nervioso?
El microbioma intestinal modula el sistema inmune y puede influir en la susceptibilidad y la respuesta inflamatoria local cerebral mediante diversos mecanismos.
¿Cómo se relaciona la inflamación persistente con la neurodegeneración?
La inflamación prolongada mantiene activadas a las células gliales, que liberan mediadores lesivos para el tejido nervioso y promueven la progresión de la pérdida neuronal.
¿En qué consiste la progresión típica del daño en el SNC?
Comienza con un insulto inicial, sigue la activación glial y la respuesta inflamatoria, que si se perpetúan, culminan en degeneración neuronal y reorganización tisular irreversible.
¿Cuál es la diferencia entre daño sináptico y muerte neuronal?
El daño sináptico afecta la comunicación intercelular e inicia la disfunción neural; la muerte neuronal es el resultado final de procesos patológicos avanzados y conlleva pérdida funcional permanente.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión biológica de los conceptos centrales del artículo sobre biopatología neurológica.
Nivel 1 – Básico
¿Cuál es la función principal de los oligodendrocitos según el artículo?
¿Qué proceso se define como la muerte progresiva y disfunción de neuronas en el sistema nervioso central?
¿Cuál es el papel de la barrera hematoencefálica en el sistema nervioso central?
Nivel 2 – Intermedio
¿Cuál de las siguientes relaciones es correcta según la tabla sobre estructuras clave y sus implicancias patológicas?
Según el texto, ¿qué diferencia principal existe entre el daño sináptico y la muerte neuronal?
¿Cómo se relacionan la activación prolongada de microglía y la inflamación crónica en la biopatología neurológica?
Nivel 3 – Avanzado
¿Cuál es la secuencia típica del daño en el SNC según la progresión descrita en el artículo?
Si se altera la barrera hematoencefálica, ¿qué efecto tiene esta disfunción en la patología neurológica?
¿Cómo influye el microbioma intestinal en la vulnerabilidad a daño estructural en el SNC?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.