⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La hemorragia intracerebral es la salida súbita de sangre hacia el parénquima cerebral que genera compresión tisular, aumento de la presión intracraneal y daño estructural y funcional neuronal, alterando la homeostasis y conduciendo a daño neuronal progresivo.
🧬 Concepto base
La hemorragia intracerebral involucra el sangrado dentro del tejido cerebral por ruptura vascular, afectando directamente neuronas, glía y vasos. Este sangrado produce daño por compresión y alteración de la microcirculación cerebral.
⚙️ Mecanismo clave
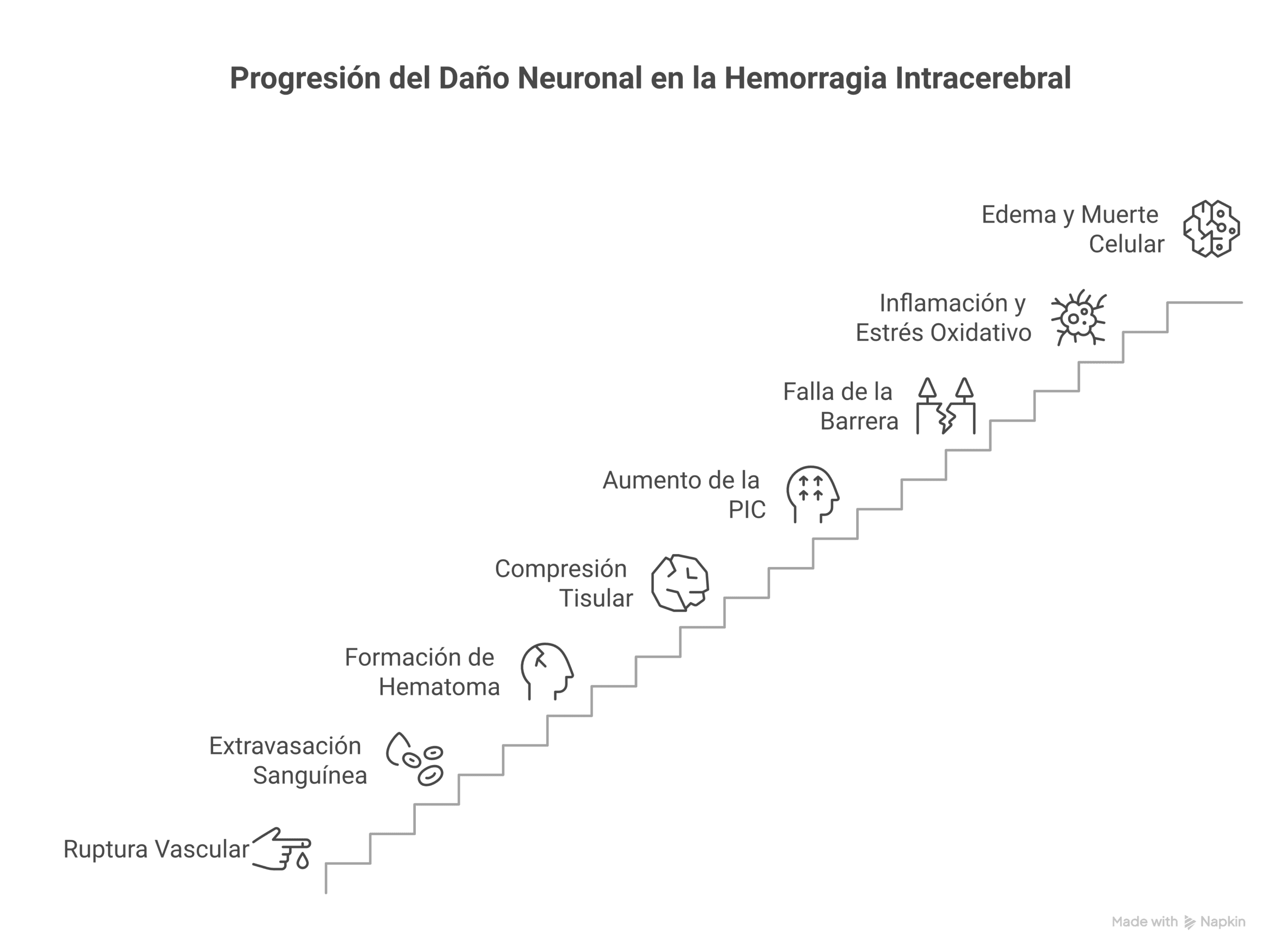
Ruptura de vasos pequeños → extravasación sanguínea → formación de hematoma → compresión y desplazamiento de tejido → aumento presión intracraneal → falla barrera hematoencefálica → inflamación y estrés oxidativo → edema y muerte celular.
🔗 Por qué es importante
Genera disfunción cerebral local y sistémica que explica la pérdida funcional y daños neuronales duraderos tras la lesión vascular.
🎯 Enfoque de examen
- Mecanismo de formación y efecto del hematoma en el parénquima cerebral
- Efectos del aumento de presión intracraneal sobre la perfusión y función neuronal
- Importancia de la ruptura y compromiso de la barrera hematoencefálica
- Rol de la activación glial e inflamación en la propagación del daño
Palabras clave: hemorragia intracerebral, hematoma, presión intracraneal, barrera hematoencefálica, inflamación glial, edema cerebral, estrés oxidativo, necrosis neuronal
La hemorragia intracerebral es un tipo de accidente cerebrovascular que implica el sangrado espontáneo directamente en el tejido cerebral. Esta lesión desencadena una cadena de efectos fisiopatológicos en el sistema nervioso central, dado que el acúmulo de sangre origina compresión cerebral, aumento de la presión intracraneal y alteraciones en la función neurológica.
Comprender estos procesos ayuda a interpretar los mecanismos estructurales y funcionales asociados al daño cerebral tras una hemorragia.
🧠 Idea central
La hemorragia intracerebral (HIC) consiste en la salida repentina de sangre hacia el interior del parénquima cerebral, resultado de la ruptura de vasos sanguíneos cerebrales pequeños o de malformaciones vasculares.
Este fenómeno interrumpe la arquitectura y dinámica normales del tejido cerebral mediante:
- Compresión física: la sangre acumulada en el espacio cerebral ejerce presión directa sobre las neuronas y la glía.
- Aumento de la presión intracraneal: la presencia de sangre eleva la presión dentro del cráneo, afectando la perfusión y la homeostasis cerebral.
- Daño funcional y estructural: la integridad neural se deteriora tanto a nivel local, por el sangrado, como en el funcionamiento de las redes neuronales.
El análisis de estos mecanismos es esencial para conectar la lesión aguda con las alteraciones funcionales persistentes que se observan tras una hemorragia intracerebral.
🌍 Contexto y alcance
La hemorragia intracerebral ocurre dentro del sistema nervioso central y afecta directamente al tejido nervioso especializado (parénquima cerebral). Este evento no solo produce una lesión localizada, sino que impacta la función cerebral global, ya que las regiones afectadas participan en circuitos complejos y en el mantenimiento de funciones superiores, motoras y sensoriales.
A nivel sistémico, la ruptura vascular altera la estabilidad de la presión intracraneal y perturba la microcirculación cerebral. Estos cambios iniciales desencadenan respuestas secundarias en el tejido cerebral y en el ambiente extracelular, amplificando el daño a través de una secuencia interrelacionada de mecanismos fisiopatológicos.
🧬 Estructuras clave
La hemorragia intracerebral compromete varios compartimientos y elementos estructurales del cerebro. Los componentes anatómicos y celulares más relevantes son:
- Parénquima cerebral: conjunto de neuronas, axones, dendritas y células gliales responsable de las funciones integradas del cerebro. Aquí se produce la acumulación de sangre y el daño primario.
- Vasos sanguíneos intracerebrales: arterias pequeñas y capilares que, al romperse debido a factores como debilidad de la pared vascular o malformaciones, inician el proceso hemorrágico.
- Espacio perivascular: zona donde suele acumularse sangre recién extravasada, alterando el intercambio normal entre sangre y tejido.
- Barrera hematoencefálica: sistema que regula el paso de moléculas entre la sangre y el cerebro; su ruptura facilita la entrada de sustancias nocivas.
- Glía (astrocitos y microglía): células que detectan la presencia de sangre y participan en la reacción inflamatoria y la reparación tisular.
La magnitud del sangrado y la localización cerebral determinan el tipo y gravedad de la disfunción observada.
⚙️ Funciones y procesos
El proceso fisiopatológico de la hemorragia intracerebral implica una serie de pasos secuenciales en los que cada mecanismo contribuye a la alteración de la homeostasis cerebral:
-
Ruptura vascular y extravasación sanguínea:
- La falla en la integridad de un vaso intracerebral, típicamente arterias perforantes o capilares, permite la salida súbita de sangre hacia el tejido cerebral.
- Esta sangre ocupa espacios intracerebrales que normalmente carecen de elementos sanguíneos.
-
Generación de masa y compresión tisular:
- La sangre coleccionada forma un hematoma que desplaza y comprime neuronas, fibras mielínicas y estructuras de soporte.
- Esto limita la conducción de señales eléctricas y puede aislar regiones cerebrales.
-
Aumento de la presión intracraneal (PIC):
- El volumen extra producido por el hematoma eleva la PIC, dado que el cráneo es rígido y no expansible.
- Cuando la PIC supera ciertos límites, se reduce la perfusión cerebral, favoreciendo isquemia secundaria.
-
Compromiso de la barrera hematoencefálica:
- El daño vascular y la presión mecánica alteran la selectividad de la barrera, permitiendo el paso de proteínas plasmáticas, iones y células inmunitarias.
- Esto incrementa el riesgo de edema y exposición a mediadores tóxicos.
-
Activación glial e inflamación secundaria:
- Astrocitos y microglía reconocen productos sanguíneos como extraños, activando cascadas inflamatorias que incluyen liberación de citocinas y reclutamiento inmunitario.
- La inflamación puede ampliar el daño al tejido periférico al hematoma.
-
Efecto tóxico de la sangre y productos de degradación:
- Elementos como la hemoglobina y el hierro liberado promueven estrés oxidativo en neuronas y glía.
- Esto desestabiliza membranas celulares y altera funciones mitocondriales y enzimáticas.
-
Edema cerebral:
- La fuga de plasma y proteínas desde vasos dañados produce edema vasogénico alrededor del hematoma.
- El edema aumenta la PIC y dificulta la oxigenación celular.
-
Alteración metabólica y muerte celular:
- Neurons privadas de oxígeno o expuestas a toxinas pierden la capacidad de mantener gradientes iónicos y producir adenosín trifosfato (ATP).
- Esto conduce a necrosis o apoptosis según severidad y tiempo de la lesión.
Estos procesos interactúan y progresan, incrementando la gravedad y extensión del daño cerebral.
🔗 Integración funcional
La ruptura vascular inicial desencadena una serie de eventos interdependientes.
De inmediato, la sangre extravasada desplaza el tejido cerebral, comprometiendo la función local por la compresión.
El rápido aumento de la presión intracraneal deteriora la perfusión y limita la llegada de oxígeno y nutrientes a zonas cercanas, generando un ambiente favorable para lesiones secundarias.
La falla de la barrera hematoencefálica expone a las neuronas a macromoléculas y células inmunitarias, intensificando el daño inicial.
Paralelamente, la activación glial genera inflamación y altera el microambiente neural. Estos procesos desencadenan fases progresivas que incluyen:
- Necrosis focal: destrucción localizada donde la presión y toxicidad son mayores.
- Desbalance iónico y edema: consecuencia de la alteración mantenida de barreras y transporte celular.
- Fase de resolución y reorganización estructural: la glía limpia detritos celulares y produce tejido cicatricial (gliosis).
Esta cadena explica cómo una lesión vascular puntual provoca pérdida funcional duradera y reorganización cerebral.
🔬 Métodos y evidencias
El estudio de la hemorragia intracerebral requiere técnicas que permitan identificar origen y extensión.
Dos herramientas neurobiológicas clave son:
-
Neuroimagen estructural:
- Tomografía computarizada (TC): detecta sangre aguda, localización y tamaño del hematoma.
- Resonancia magnética (RM): analiza efectos secundarios como edema cerebral y destrucción tisular progresiva.
-
Análisis histopatológico:
- Permite observar la respuesta celular a la presencia de sangre, incluyendo inflamación, lesión de barrera hematoencefálica y muerte neuronal.
Estas pruebas aportan evidencia directa de las alteraciones estructurales y fisiopatológicas tras la hemorragia intracerebral.
🩺 Puente clínico
Comprender los mecanismos de la hemorragia intracerebral facilita explicar los hallazgos neurológicos tras el sangrado.
La compresión del parénquima y el aumento de la presión intracraneal provocan disfunción en circuitos neuronales, generando déficits según el área afectada.
Adicionalmente, la inflamación y la respuesta secundaria amplifican la alteración funcional, puesto que el tejido circundante al hematoma puede sufrir daño incluso sin exposición directa al sangrado.
Así, el vínculo entre fisiopatología y clínica reside en cómo la alteración estructural y la respuesta tisular emergente se reflejan en síntomas y signos neurológicos.
💎 Perlas de alto rendimiento
- Ruptura de vasos sanguíneos pequeños: es el evento inicial en la hemorragia intracerebral.
- Acumulación súbita de sangre: genera un aumento rápido de la presión intracraneal que afecta la perfusión cerebral.
- Hematoma: desplaza y comprime el tejido cerebral, alterando funciones locales e integradas.
- Disrupción de la barrera hematoencefálica: permite el tránsito de sustancias y células que agravan el daño.
- Activación glial: produce inflamación, que puede extender la lesión al tejido adyacente.
- Productos de degradación sanguínea: inducen estrés oxidativo, contribuyendo a la muerte celular neuronal y glial.
- Edema cerebral vasogénico: aumenta la presión intracraneal y perjudica la función celular.
- Interacción de mecanismos: se potencian, exacerbando el compromiso neurológico.
🧠 Puntos clave
- Hemorragia intracerebral: surge por sangrado espontáneo en el parénquima debido a ruptura vascular.
- Hematoma: genera compresión tisular y eleva la presión intracraneal, comprometiendo la función neuronal.
- Ruptura de la barrera hematoencefálica: facilita la entrada de agentes injuriosos y células inflamatorias.
- Inflamación secundaria y estrés oxidativo: amplían el daño más allá del foco hemorrágico.
- Edema cerebral: agrava la disfunción y expone más tejido a isquemia y lesión.
- Fisiopatología: explica la evolución del daño funcional y estructural tras el sangrado.
❓ Preguntas frecuentes
¿Qué ocurre fisiológicamente tras una hemorragia intracerebral?
La sangre se extravasa hacia el tejido cerebral, formando un hematoma que comprime células nerviosas y altera la función local.
¿Por qué aumenta la presión intracraneal tras una hemorragia cerebral?
El cráneo rígido limita la expansión; el volumen sanguíneo adicional eleva la presión, reduciendo el flujo sanguíneo cerebral.
¿Cómo afecta la ruptura de la barrera hematoencefálica al cerebro?
Su disrupción permite el paso de proteínas y células inmunes, induciendo inflamación y amplificando el daño neuronal.
¿Qué función tiene la glía durante la hemorragia intracerebral?
Astrocitos y microglía detectan el daño, coordinan la respuesta inflamatoria y ayudan a limpiar detritos, aunque también pueden aumentar el daño secundario.
¿Por qué la localización del sangrado es importante en sus consecuencias?
Cada región cerebral cumple funciones específicas; su afectación determina la naturaleza y gravedad de los déficits neurológicos.
¿Qué relación tiene el hematoma con el edema cerebral?
El hematoma altera la permeabilidad vascular, promoviendo la extravasación de líquidos y proteínas que generan edema.
¿Qué mecanismos conducen a la muerte neuronal en la hemorragia intracerebral?
La compresión mecánica, isquemia por reducción del flujo y sustancias tóxicas provocan desequilibrio iónico, falla energética y muerte celular.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico de la hemorragia intracerebral basado en el artículo proporcionado.
Nivel 1 – Básico
¿Qué es la hemorragia intracerebral según el artículo?
¿Cuál es una consecuencia inmediata de la acumulación de sangre en el tejido cerebral?
¿Qué estructuras conforman el parénquima cerebral afectado en la hemorragia intracerebral?
Nivel 2 – Intermedio
¿Cuál es la relación correcta entre el aumento de la presión intracraneal (PIC) y la perfusión cerebral tras una hemorragia?
¿Cuál de estas estructuras participa activamente en la inflamación secundaria tras el sangrado cerebral?
¿Cuál es el vínculo correcto entre el hematoma y el edema cerebral en la hemorragia intracerebral?
Nivel 3 – Avanzado
¿Qué secuencia mecanística ocurre tras la ruptura vascular en la hemorragia intracerebral, según el artículo?
Si el daño compromete la barrera hematoencefálica, ¿qué efecto fisiopatológico sucede en el entorno cerebral?
Según la integración funcional, ¿cómo contribuye la activación glial a la evolución del daño tras una hemorragia intracerebral?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.