⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
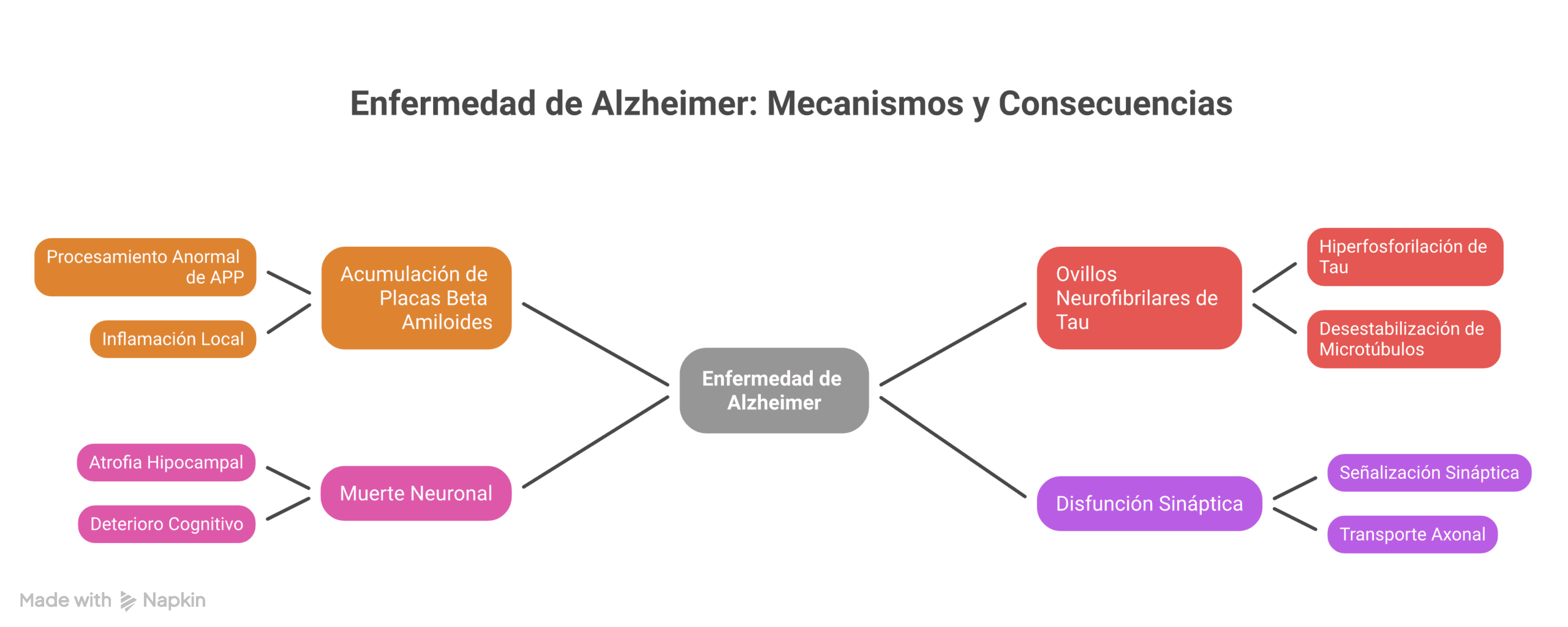
La enfermedad de Alzheimer es un trastorno neurodegenerativo caracterizado por acumulación de placas beta amiloides y ovillos neurofibrilares de tau, que alteran la arquitectura neuronal y causan pérdida progresiva de memoria y funciones cognitivas.
🧬 Concepto base
Es una enfermedad que provoca muerte neuronal y desorganización cerebral mediante placas extracelulares y ovillos intracelulares, afectando estructuras como el hipocampo y la corteza cerebral.
⚙️ Mecanismo clave
El procesamiento anormal de APP genera beta amiloide que forma placas; la hiperfosforilación de tau causa ovillos neurofibrilares intracelulares, lo que interrumpe la función sináptica y provoca muerte celular progresiva.
🔗 Por qué es importante
La acumulación de lesiones estructurales y la disfunción sináptica afectan la memoria y otras funciones cognitivas, reflejando degeneración cerebral acumulativa y deterioro funcional.
🎯 Enfoque de examen
- Placas beta amiloides interfieren la señalización sináptica y generan inflamación local.
- Ovillos tau hiperfosforilados desestabilizan microtúbulos y alteran transporte axonal.
- Atrofia hipocampal correlaciona con deterioro temprano de la memoria.
- Disfunción sináptica precede a la muerte neuronal y determina déficit cognitivo.
Palabras clave: enfermedad de Alzheimer, beta amiloide, tau, hipocampo, placas amiloides, ovillos neurofibrilares, atrofia cerebral, disfunción sináptica
La enfermedad de Alzheimer es un proceso neurodegenerativo progresivo y la causa más frecuente de demencia a nivel mundial. Su desarrollo implica cambios biológicos que afectan selectivamente las funciones cognitivas, en especial la memoria, debido a la acumulación de estructuras anormales en el tejido cerebral y pérdida neuronal.
🧠 Idea central
La enfermedad de Alzheimer es un trastorno neurológico progresivo que lleva a la disfunción y muerte de neuronas en el cerebro.
Este proceso obedece a mecanismos moleculares y celulares característicos que, al afectar la arquitectura y conectividad cerebral, ocasionan pérdida gradual de la memoria y demás capacidades cognitivas fundamentales.
La base del Alzheimer reside en dos lesiones neuropatológicas principales: las placas extracelulares de beta amiloide y los ovillos neurofibrilares intracelulares formados por proteína tau hiperfosforilada.
Estos elementos resultan de alteraciones en el procesamiento de proteínas dentro de grupos neuronales críticos para la memoria y el pensamiento.
🌍 Contexto y alcance
Comprender la enfermedad de Alzheimer implica analizarla desde varias dimensiones que abarcan diferentes niveles de organización biológica:
- Nivel molecular: alteraciones en el metabolismo de la proteína precursora amiloide (APP) y de la proteína tau, involucradas en los cambios bioquímicos que inician la patología.
- Nivel celular: acumulación de proteínas anómalas en el compartimento extracelular (placas amiloides) e intracelular (ovillos neurofibrilares), deteriorando la función y viabilidad de las neuronas.
- Nivel tisular: pérdida progresiva de neuronas, desorganización de circuitos neuronales y atrofia cerebral localizada principalmente en regiones implicadas en la memoria y el pensamiento abstracto.
- Nivel funcional: disminución gradual de capacidades cognitivas, que abarca desde fallos iniciales en la memoria reciente hasta la pérdida integral de habilidades intelectuales y funcionales.
El abordaje sistémico reconoce la interacción de factores genéticos, moleculares y ambientales que desencadenan y perpetúan los procesos degenerativos, reflejados en la evolución clínica y neuropatológica.
🧬 Estructuras clave
La enfermedad se caracteriza por daños estructurales específicos en el cerebro, identificables tanto a nivel macroscópico como microscópico:
- ¿Qué es? Corteza cerebral: áreas asociativas (frontal, temporal y parietal) implicadas en funciones complejas como la memoria, el juicio y el lenguaje. La progresiva atrofia cortical se debe a la muerte selectiva de neuronas.
- ¿Qué es? Hipocampo: estructura en el lóbulo temporal medial esencial para la formación y consolidación de la memoria declarativa, siendo la primera región en mostrar pérdida neuronal y reducción volumétrica.
- ¿Qué es? Neurona: célula nerviosa cuya función y estructura se alteran por la acumulación patológica de proteínas y pérdida de conexiones sinápticas.
- ¿Qué es? Placas amiloides: depósitos extracelulares compuestos por péptido beta amiloide, que interfieren con la señalización sináptica y fomentan procesos inflamatorios locales.
- ¿Qué es? Ovillos neurofibrilares: agregados intracelulares formados por filamentos de proteína tau hiperfosforilada, que comprometen la estabilidad del citoesqueleto y el transporte intracelular neuronal.
El daño progresivo en estas estructuras conduce a alteraciones desde la comunicación neuronal hasta la destrucción irreversible del tejido nervioso.
⚙️ Funciones y procesos
Los mecanismos patológicos que subyacen a la enfermedad de Alzheimer siguen un patrón secuencial y afectan múltiples niveles:
-
Formación y acumulación de beta amiloide:
- La proteína precursora amiloide (APP) es una proteína transmembrana presente en la mayoría de las neuronas.
- En condiciones patológicas, la APP es procesada por enzimas que generan segmentos de beta amiloide insolubles y capaces de agregarse.
- El péptido beta amiloide se acumula en el espacio extracelular formando placas neuríticas.
- Estas placas bloquean la comunicación sináptica normal y activan una respuesta inflamatoria local, dañando el tejido neuronal.
-
Alteraciones de la proteína tau y formación de ovillos:
- La proteína tau estabiliza microtúbulos en las neuronas, esenciales para el transporte interno axonal.
- En el Alzheimer, la tau se hiperfosforila, perdiendo su función y agregándose en filamentos helicoidales.
- Los ovillos neurofibrilares se forman dentro de las neuronas, afectando la arquitectura interna y viabilidad celular.
-
Deterioro neuronal y atrofia cerebral:
- La toxicidad del beta amiloide y la tau modificada desencadena la muerte celular por mecanismos como apoptosis.
- La pérdida neuronal comienza en el hipocampo y la corteza entorrinal y se extiende progresivamente a otras áreas corticales.
- Esto resulta en una reducción visible del volumen cerebral (atrofia) y dilatación ventricular.
-
Disfunción sináptica:
- Antes de la muerte masiva neuronal, se produce la disrupción de las conexiones sinápticas, limitando la transferencia de información.
- La plasticidad sináptica necesaria para el aprendizaje y la memoria se reduce, generando el deterioro cognitivo progresivo clínico.
Este proceso es acumulativo y lento, dando lugar a síntomas neurológicos que se intensifican conforme avanzan los cambios estructurales y moleculares.
🔗 Integración funcional
Las lesiones en estructuras clave generan una cascada de disfunciones interrelacionadas:
- Las placas amiloides promueven microambientes tóxicos e inflamatorios que alteran la homeostasis neuronal.
- Los ovillos neurofibrilares bloquean el transporte intracelular, acelerando la degeneración neuronal.
- El daño sináptico limita la codificación y recuperación de información, especialmente la memoria reciente y el aprendizaje.
- La atrofia cortical y del hipocampo determina la gravedad funcional y amplía el espectro sintomático a medida que progresa.
La acumulación secuencial de lesiones moleculares se refleja en la disfunción global del sistema nervioso y la manifestación progresiva de los síntomas neurocognitivos característicos del Alzheimer.
🔬 Métodos y evidencias
El estudio del Alzheimer se apoya en técnicas morfológicas y de imagen para identificar y cuantificar las lesiones principales:
- El análisis histopatológico post mortem confirma placas amiloides y ovillos neurofibrilares mediante tinciones específicas.
- La resonancia magnética (RM) volumétrica visualiza la atrofia cerebral, fundamentalmente en hipocampo y corteza temporal medial, correlacionada con el deterioro clínico.
- La tomografía por emisión de positrones (PET) con radiotrazadores selectivos identifica in vivo regiones con acumulación anómala de beta amiloide, apoyando el diagnóstico biológico.
Estas metodologías permiten medir cambios estructurales y moleculares y estudiar la progresión de la enfermedad en base a evidencias biológicas.
🩺 Puente clínico
El entendimiento de los mecanismos patológicos del Alzheimer relaciona las lesiones cerebrales con las alteraciones cognitivas en los pacientes.
La pérdida inicial de la memoria se vincula con daño en el hipocampo, mientras que el deterioro progresivo de funciones como el lenguaje, la orientación y el juicio refleja la extensión de la atrofia y la disrupción sináptica a regiones corticales adicionales.
💎 Perlas de alto rendimiento
- Beta amiloide origen: El beta amiloide se origina por la escisión aberrante de la proteína precursora amiloide (APP), depositándose extracelularmente.
- Función tau: La proteína tau estabiliza microtúbulos; su hiperfosforilación conduce a insolubilidad y agregación intracelular.
- Ovillos tau efecto: Los ovillos tau desestructuran el citoesqueleto neuronal desde el interior de la célula.
- Ambiente neurotóxico: Placas amiloides y ovillos tau crean un ambiente neurotóxico que induce muerte neuronal.
- Hipocampo vulnerabilidad: El hipocampo es la región más tempranamente afectada en la pérdida neuronal asociada al Alzheimer.
- Disfunción sináptica importancia: La disfunción sináptica antecede y determina el deterioro cognitivo más que la muerte neuronal aislada.
- Progresión atrofia: La atrofia cerebral progresa desde áreas temporales mediales hacia regiones asociativas corticales superiores.
- Deterioro funcional gradual: El deterioro funcional es gradual, acumulativo y correlaciona con la progresión de lesiones estructurales y moleculares.
🧠 Puntos clave
- Característica patológica: La enfermedad de Alzheimer se caracteriza por placas beta amiloides extracelulares y ovillos neurofibrilares de tau hiperfosforilada.
- Mecanismos moleculares: El procesamiento anómalo de proteínas neuronales desencadena cascadas de toxicidad y muerte celular.
- Déficits cognitivos: La destrucción de sinapsis y la pérdida neuronal se relacionan con déficits cognitivos topográficamente específicos.
- Atrofia hippocampal: La atrofia inicial del hipocampo fundamenta la pérdida precoz de memoria.
- Áreas corticales afectadas: El proceso patológico afecta preferentemente áreas corticales superiores conforme avanza la enfermedad.
- Diagnóstico biológico: La integración de técnicas neuropatológicas y de imagen sustenta la comprensión biológica del deterioro cognitivo.
❓ Preguntas frecuentes
¿Qué desencadena la acumulación de beta amiloide en el Alzheimer?
La acumulación de beta amiloide se debe a un procesamiento alterado de la proteína precursora amiloide (APP) en las neuronas, que genera un péptido insoluble depositado extracelularmente como placas amiloides.
¿Cómo afecta la formación de ovillos neurofibrilares a la función neuronal?
Los ovillos neurofibrilares, compuestos por tau hiperfosforilada, desestabilizan los microtúbulos del citoesqueleto intracelular, interrumpiendo el transporte interno y contribuyendo a la disfunción y muerte neuronal.
¿Qué regiones cerebrales son más vulnerables y por qué?
El hipocampo y la corteza temporal medial son especialmente vulnerables debido a su rol central en la formación de memoria y su susceptibilidad a la acumulación temprana de proteínas patológicas.
¿Por qué disminuye la comunicación sináptica antes de la muerte neuronal?
Porque las acumulaciones de beta amiloide y tau alteran la estructura y función de las sinapsis, reduciendo la plasticidad y la conectividad neuronal antes de que ocurra la muerte celular.
¿Cómo se detectan las lesiones de Alzheimer en neuropatología e imágenes?
Las placas amiloides y ovillos neurofibrilares se identifican con tinciones específicas en tejido post mortem, mientras que técnicas de resonancia magnética y PET permiten visualizar atrofia cerebral y depósitos proteicos en pacientes vivos.
¿Hay un solo mecanismo responsable del Alzheimer?
No, la enfermedad resulta de la interacción compleja entre factores genéticos, moleculares y ambientales que promueven la formación de placas, ovillos, disfunción sináptica y muerte neuronal progresiva.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico sobre la enfermedad de Alzheimer presentado en el artículo.
Nivel 1 – Básico
¿Cuál es la característica patológica principal de la enfermedad de Alzheimer según el artículo?
¿Qué estructura cerebral es la primera en mostrar pérdida neuronal en Alzheimer?
¿Cuál es la función esencial normal de la proteína tau en las neuronas?
Nivel 2 – Intermedio
¿Cuál es la relación correcta entre las placas amiloides y la disfunción neuronal en Alzheimer?
¿Cómo se distingue la implicación de ovillos neurofibrilares respecto a la proteína tau?
Según el artículo, ¿qué relación es correcta entre niveles molecular, celular y tisular en Alzheimer?
Nivel 3 – Avanzado
¿Cuál es la secuencia correcta de eventos patológicos que llevan a la atrofia cerebral en Alzheimer según el texto?
Si se inhibiera la hiperfosforilación de tau, ¿qué efecto esperado tendría sobre el transporte intracelular neuronal de acuerdo al artículo?
¿Qué consecuencia funcional deriva directamente de la disrupción sináptica previa a la muerte neuronal en Alzheimer?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.