⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
El accidente cerebrovascular isquémico es una interrupción súbita del flujo sanguíneo cerebral causada por oclusión arterial que priva a las neuronas de oxígeno y glucosa, desencadenando falta de ATP, alteración iónica, glutamato excesivo y muerte celular. Este daño evoluciona desde un núcleo infartado irreversible hacia una penumbra isquémica potencialmente recuperable si se restaura la perfusión rápidamente.
🧬 Concepto base
El accidente cerebrovascular isquémico es una lesión cerebral causada por bloqueo arterial que impide el suministro sanguíneo. Esto impide que las neuronas mantengan su función y viabilidad, provocando daño neurológico según la región afectada.
⚙️ Mecanismo clave
La oclusión arterial reduce abruptamente oxígeno y glucosa, disminuyendo ATP en neuronas. Esto desactiva la bomba Na⁺/K⁺, altera el potencial de membrana, causa edema citotóxico y libera glutamato que induce excitotoxicidad y muerte neuronal por necrosis y apoptosis.
🔗 Por qué es importante
La conectividad vascular y neuronal condiciona el daño y la recuperación. La extensión del infarto y la penumbra determinan déficits neurológicos y la posibilidad de preservar función si se restaura el flujo.
🎯 Enfoque de examen
- Causa → efecto: oclusión arterial → isquemia → falla metabólica neuronal
- Rol de la bomba Na⁺/K⁺ y homeostasis iónica en edema y disfunción celular
- Excitotoxicidad por glutamato: mecanismo molecular de daño neuronal
- Diferencia entre núcleo infartado y penumbra isquémica
Palabras clave: accidente cerebrovascular isquémico, oclusión arterial, neurona cortical, bomba Na⁺/K⁺ ATPasa, glutamato, penumbra isquémica, edema citotóxico, barrera hematoencefálica
El accidente cerebrovascular isquémico es consecuencia de la obstrucción súbita de una arteria cerebral, lo que corta el suministro de sangre y oxígeno a parte del tejido encefálico. Dicha privación desencadena daño y muerte neuronal, produciendo déficits neurológicos de acuerdo con la localización afectada. Analizar estos mecanismos permite entender la relación entre vasos cerebrales, tejido nervioso y las bases biológicas del daño funcional.
🧠 Idea central
El accidente cerebrovascular isquémico tiene como base la interrupción brusca del flujo sanguíneo a una región cerebral, habitualmente por la oclusión de una arteria. Esta obstrucción impide la llegada de oxígeno y nutrientes indispensables, como la glucosa, al tejido nervioso. Al verse privadas de estos elementos, las neuronas no pueden mantener su función y viabilidad, generando daños que se traducen en pérdida de capacidades neurológicas controladas por la zona afectada.
Es fundamental comprender que el daño no es homogéneo. Existe un área central donde la lesión neuronal es inmediata e irreversible, y una zona periférica llamada penumbra isquémica, que si bien está en riesgo, puede recuperarse si se restablece el flujo sanguíneo de forma rápida. El mecanismo subyacente refleja la relación directa entre el suministro vascular y la supervivencia neuronal.
🌍 Contexto y alcance
El análisis del accidente cerebrovascular isquémico se realiza primordialmente a nivel de órganos y sistemas, integrando conceptos de neurología y fisiología vascular cerebral. El enfoque se centra en cómo el sistema arterial cerebral abastece al parénquima encefálico y las consecuencias de la suspensión abrupta de este aporte.
Se consideran tanto los componentes anatómicos —vasos sanguíneos y tejido nervioso— como las consecuencias funcionales a nivel celular. Tras la oclusión, evolucionan eventos que afectan la homeostasis de las neuronas y células del sistema nervioso central. La atención se dirige a la secuencia de cambios bioquímicos y estructurales que conectan la lesión vascular inicial con el daño neurobiológico evidente.
🧬 Estructuras clave
El accidente cerebrovascular isquémico involucra:
- Arterias cerebrales principales: Destaca la arteria cerebral media, el vaso bloqueado con mayor frecuencia, seguida por las arterias cerebral anterior y posterior. La arteria carótida interna y las arterias vertebrales son rutas esenciales de aporte a diversos territorios encefálicos.
- Tejido cerebral: Incluye neuronas, especialmente corticales, y células gliales, que constituyen el parénquima cerebral vulnerable al daño isquémico.
- Barrera hematoencefálica: Estructura que regula el paso de sustancias entre sangre y cerebro; su alteración es crucial en la evolución del daño y en la formación de edema.
- Microvasculatura cerebral: Red capilar que asegura una perfusión fina y el intercambio metabólico. Su integridad es clave para mantener un ambiente homeostático neuronal.
| Estructura | Función principal | Implicación en el accidente isquémico |
|---|---|---|
| Arteria cerebral media | Distribuye sangre (oxígeno y glucosa) a corteza frontal, parietal y subcorteza relacionadas con funciones motoras y sensoriales | Oclusión afecta el territorio más amplio, asociado a déficits neurológicos focales importantes |
| Neurona cortical | Procesa, transmite y recibe señales eléctricas; responsable de integración sensorial y motora | La falta de oxígeno induce disfunción metabólica y muerte celular por mecanismos energéticos y tóxicos |
| Barrera hematoencefálica | Filtra y protege el microambiente cerebral, regula el ingreso de moléculas y células | Se ve afectada en la isquemia, promoviendo edema y entrada de mediadores inflamatorios que agravan el daño |
| Astrocitos (células gliales) | Proveen soporte nutritivo, regulan neurotransmisores y modulan el ambiente extracelular | Su función se altera en la isquemia y pueden contribuir a la respuesta inflamatoria local |
La interacción anatómica y funcional de estas estructuras determina la susceptibilidad y evolución del daño ante la falta de perfusión.
⚙️ Funciones y procesos
El evento inicial es la oclusión arterial súbita, que provoca una caída instantánea en el suministro de oxígeno (O2) y glucosa al tejido cerebral irrigado por la arteria afectada. Este déficit causa hipoxia y la incapacidad para generar adenosín trifosfato (ATP), el principal portador de energía celular, en las mitocondrias neuronales.
- Reducción de ATP: Sin ATP, fallan los mecanismos activos, especialmente la bomba sodio-potasio (Na+/K+ ATPasa), que mantiene los gradientes iónicos esenciales para la actividad eléctrica neuronal.
- Pérdida de homeostasis iónica: El cese de la bomba Na+/K+ causa pérdida del potencial de membrana y una entrada excesiva de sodio y agua, originando edema citotóxico (hinchazón celular).
- Despolarización e hiperexcitabilidad: La despolarización masiva induce la liberación descontrolada de glutamato en el espacio extracelular.
- Excitotoxicidad: El exceso de glutamato hiperactiva receptores glutamatérgicos NMDA y AMPA en neuronas vecinas, aumentando la entrada de calcio intracelular.
- Daño celular final: La acumulación de calcio activa enzimas destructivas (proteasas, lipasas, endonucleasas) y genera especies reactivas de oxígeno, conduciendo a muerte celular irreversible: necrosis en el núcleo infartado y apoptosis en la penumbra.
Además, la interrupción del flujo sanguíneo desencadena procesos adicionales en la microvasculatura y la barrera hematoencefálica, facilitando la migración de células inmunes y la liberación de mediadores inflamatorios que contribuyen al daño.
Este proceso conduce a una zonificación del área lesionada: un núcleo central con daño irreversible y una penumbra isquémica potencialmente recuperable si la perfusión se restablece a tiempo.
🔗 Integración funcional
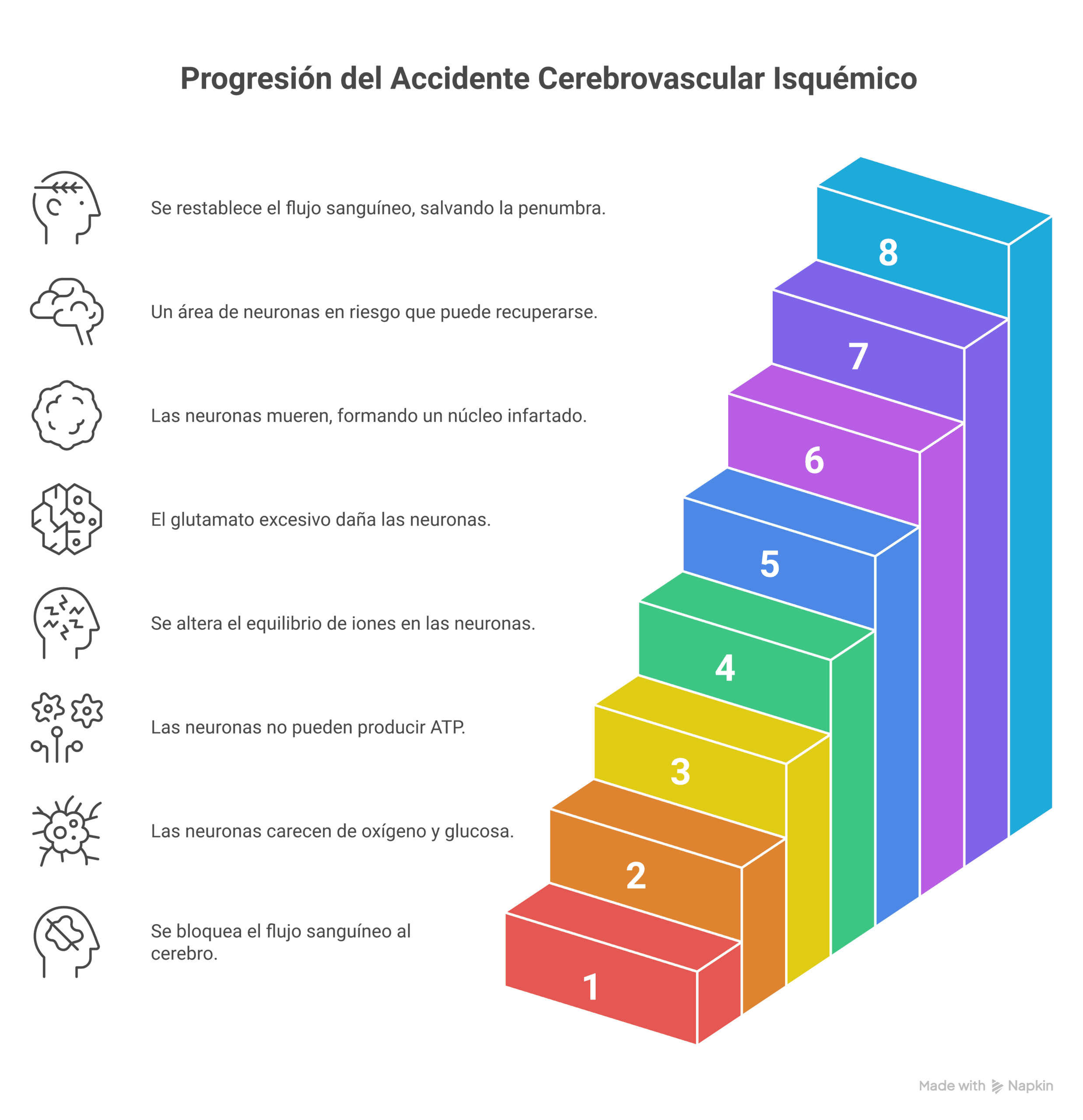
La relación entre obstrucción vascular, desequilibrio metabólico y daño neuronal progresa en fases:
- Oclusión arterial: Impide el transporte de oxígeno y glucosa, provocando pérdida inmediata de producción de ATP y función neuronal.
- fracaso energético: Detención de sistemas de transporte y acumulación iónica intracelular resultan en hinchazón, despolarización y liberación masiva de glutamato.
- Formación de núcleo infartado y penumbra: En el centro, la muerte celular es rápida y permanente, mientras que en la penumbra la lesión es reversible si se restituye el flujo sanguíneo.
- Circulo de daño progresivo: Persistencia de la oclusión perpetúa excitotoxicidad, inflamación y edema vascular, expandiendo el daño y transformando la penumbra en tejido infartado.
En síntesis, toda alteración abrupta del flujo cerebral activa cascadas bioquímicas y celulares que determinan la magnitud del daño y la posibilidad de recuperación según el tiempo hasta restaurar la perfusión.
🔬 Métodos y evidencias
El conocimiento sobre el accidente cerebrovascular isquémico proviene de la observación metódica del tejido cerebral lesionado mediante técnicas avanzadas.
- Resonancia magnética: Visualiza la topografía de la isquemia y permite diferenciar entre el núcleo infartado y la penumbra.
- Evaluación funcional: Pruebas electrofisiológicas reflejan el deterioro de la transmisión neuronal en áreas específicas afectadas.
- Modelos experimentales: La reproducibilidad de la oclusión arterial en animales ha permitido describir fases tempranas y tardías del daño y la progresión fisiopatológica.
Estas herramientas evidencian cómo una interrupción inicial del flujo vascular desencadena mecanismos neuronales y celulares que llevan a pérdida progresiva de función y alteración estructural cerebral.
🩺 Puente clínico
La fisiopatología del accidente cerebrovascular isquémico explica la secuencia de signos neurológicos observados tras la lesión. El área cerebral irrigada por la arteria obstruida determina los déficits funcionales presentes. Por ejemplo, la oclusión de la arteria cerebral media produce alteraciones motoras y sensoriales contralaterales acordes al territorio afectado.
La coexistencia de zonas de muerte neuronal permanente y penumbra recuperable justifica la urgencia en el diagnóstico temprano y la distribución del déficit según el territorio vascular lesionado.
💎 Perlas de alto rendimiento
- Oclusión arterial súbita: es el desencadenante esencial del accidente cerebrovascular isquémico.
- Falta de oxígeno y glucosa: bloquea la generación de ATP necesaria para la función neuronal.
- Fallo de la bomba Na+/K+: conduce a edema citotóxico por entrada excesiva de sodio y agua.
- Despolarización generalizada: induce liberación excesiva de glutamato y excitotoxicidad neuronal.
- Aumento intracelular de calcio: activa rutas destructivas culminando en muerte celular irreversible.
- Daño organizado: en un núcleo infartado irreversible y una penumbra potencialmente recuperable si se restablece la perfusión.
- Permeabilidad alterada de la barrera hematoencefálica: favorece edema y proceso inflamatorio que agravan el daño.
- Duración de la isquemia: determina la extensión y gravedad de la lesión cerebral.
🧠 Puntos clave
- Accidente cerebrovascular isquémico: es causado por la interrupción del flujo arterial que afecta la oxigenación y metabolismo neuronal.
- Rápida caída de ATP: desencadena alteraciones iónicas y bioquímicas perjudiciales para la viabilidad celular.
- Muerte neuronal: ocurre por excitotoxicidad mediada por glutamato y daño oxidativo.
- Vínculo entre irrigación sanguínea y función neurobiológica: es fundamental para entender la lesión isquémica.
- Penumbra isquémica: representa tejido con potencial de recuperación ante restablecimiento oportuno del flujo.
- Extensión y irreversibilidad del daño: aumentan con la prolongación del tiempo isquémico.
❓ Preguntas frecuentes
¿Cuál es el suceso inicial en el accidente cerebrovascular isquémico?
La oclusión súbita de una arteria cerebral que impide el suministro de sangre, oxígeno y glucosa al tejido irrigado.
¿Qué sucede en la neurona ante la falta repentina de oxígeno?
La neurona deja de producir ATP, pierde la capacidad de mantener su gradiente iónico y entra en daño funcional irreversible.
¿Por qué es importante la penumbra isquémica?
Es una región adyacente al núcleo infartado donde el tejido aún puede recuperarse si la perfusión se restablece rápidamente.
¿En qué consiste la excitotoxicidad en la isquemia cerebral?
Es el daño provocado por el exceso de glutamato que provoca sobrecarga de calcio en las neuronas, activando mecanismos destructivos y muerte celular.
¿Cómo influye la barrera hematoencefálica en el proceso isquémico?
Su alteración favorece la formación de edema y permite el ingreso de células y mediadores inflamatorios que amplifican el daño cerebral.
¿Qué relación existe entre el vaso sanguíneo obstruido y el déficit neurológico?
Cada arteria irriga determinadas áreas cerebrales; la oclusión afecta las funciones controladas por la zona vascular comprometida.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión de los contenidos biológicos relacionados con el accidente cerebrovascular isquémico presentados en el artículo.
Nivel 1 – Básico
¿Cuál es el suceso inicial que provoca un accidente cerebrovascular isquémico?
¿Qué función tiene la arteria cerebral media según el texto?
¿Qué es la penumbra isquémica en el contexto del accidente cerebrovascular?
Nivel 2 – Intermedio
¿Cuál es la relación correcta entre la falta de ATP y el edema citotóxico en la isquemia cerebral?
¿Qué función desempeñan los astrocitos en condiciones fisiológicas y cómo se alteran en la isquemia?
¿Cuál es la correcta correspondencia entre la estructura cerebral y su implicación en el accidente isquémico?
Nivel 3 – Avanzado
¿Qué consecuencias genera el aumento intracelular de calcio en las neuronas durante la isquemia?
¿Cómo progresa la zona de penumbra isquémica ante persistencia de la oclusión arterial?
¿Cuál es el papel de la barrera hematoencefálica en la evolución del daño isquémico?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.