⏱ Lectura rápida: 3 minutos
📌 Resumen rápido
La fisiopatología de lesión renal implica mecanismos celulares y tisulares que afectan la filtración glomerular y la reabsorción tubular, ocasionando deterioro rápido de la función renal y alteraciones sistémicas en fluidos, electrolitos y ácido-base.
🧬 Concepto base
La lesión renal aguda es un síndrome caracterizado por descenso rápido en la función filtrante renal. Involucra daño celular en glomérulos, túbulos y vasculatura que interrumpe la eliminación de residuos y la homeostasis corporal.
⚙️ Mecanismo clave
El daño isquémico o tóxico provoca disfunción tubular por pérdida de gradientes iónicos y daño estructural, reduciendo la tasa de filtración glomerular y provocando inflamación, estrés oxidativo y fibrosis progresiva.
🔗 Por qué es importante
La lesión renal genera acumulación de productos nitrogenados y alteraciones hidroelectrolíticas que afectan múltiples sistemas, condicionando la función orgánica y marcando la severidad del daño.
🎯 Puntos que suelen preguntarse en examen
- ¿Qué estructuras renales son más vulnerables al daño isquémico?
- ¿Cómo afecta la pérdida de integridad tubular a la reabsorción de solutos?
- ¿Qué rol tiene la respuesta inflamatoria en la progresión del daño renal?
- ¿Por qué disminuye la filtración glomerular en lesión renal aguda?
- ¿Cómo contribuye el estrés oxidativo a la muerte celular tubular?
- ¿Qué indica la presencia de proteinuria en el contexto de lesión renal?
Palabras clave: fisiopatología de lesión renal, lesión renal aguda, filtración glomerular, túbulo proximal, inflamación renal, estrés oxidativo, fibrosis renal, proteinuria
La fisiopatología de la lesión renal aborda los mecanismos celulares, tisulares y sistémicos que interrumpen la capacidad del riñón para filtrar la sangre y eliminar productos de desecho, además de mantener el equilibrio hidroelectrolítico y ácido-base.
Comprender estos procesos es fundamental para clarificar cómo el daño renal puede provocar una rápida alteración funcional y estructural que afecta a todo el organismo.
🧠 Idea central
La lesión renal aguda se define como un síndrome caracterizado por la disminución rápida y significativa de la capacidad renal de filtrado y excreción que se desarrolla en días o semanas.
Este proceso conlleva a la retención de productos nitrogenados, como urea y creatinina, en el plasma, así como a desequilibrios en líquidos, electrolitos y ácido-base.
La lesión puede variar desde alteraciones funcionales reversibles, con mecanismos adaptativos sin daño tisular permanente, hasta lesiones estructurales con daño celular agudo.
La naturaleza y localización de la lesión determinan la gravedad y las manifestaciones sistémicas, reflejando mecanismos fisiopatológicos convergentes que afectan la función renal global.
🌍 Contexto y alcance
El estudio fisiopatológico de la lesión renal abarca múltiples niveles biológicos, desde el molecular hasta el sistémico:
- Nivel molecular: Alteraciones en transportadores de membrana, proteínas estructurales, señales inflamatorias y moléculas reguladoras del funcionamiento celular renal.
- Nivel celular: Daño a células epiteliales renales del glomérulo y túbulo, y a células endoteliales vasculares que comprometen la función local.
- Nivel tisular: Cambios en la arquitectura histológica renal, incluyendo engrosamiento de membranas basales, apoptosis, necrosis y remodelado de la matriz extracelular.
- Nivel sistémico: Alteraciones en la homeostasis general, con retención de productos nitrogenados, desequilibrio hidroelectrolítico y acidósis que afectan al organismo.
La integración de estos niveles permite comprender cómo una lesión puntual en la microestructura renal se traduce en una disfunción global de la función renal.
🧬 Estructuras clave
Las diferentes estructuras renales intervienen en la fisiopatología de la lesión renal aguda, y cada una presenta características específicas que determinan su vulnerabilidad y tipo de lesión:
-
Glomérulo:
- ¿Qué es? Complejo formado por capilares fenestrados, podocitos y membrana basal que inicia la filtración plasmática.
- ¿Dónde actúa? Corteza renal.
- ¿Qué permite? Formación del ultrafiltrado primario libre de proteínas.
- ¿Qué ocurre si se altera? Daño a células endoteliales, podocitos o membrana basal reduce la permeabilidad selectiva, disminuye la tasa de filtración glomerular y favorece la proteinuria.
-
Túbulo renal (principalmente túbulo proximal):
- ¿Qué es? Segmento tubular con células epiteliales especializadas en reabsorber agua, sodio y solutos esenciales.
- ¿Dónde actúa? Desde la corteza hacia la médula renal en la nefrona.
- ¿Qué permite? Regula la composición final de la orina y recupera sustancias vitales.
- ¿Qué ocurre si se altera? Daño isquémico o tóxico destruye microvellosidades y compromete uniones intercelulares, causando pérdida de reabsorción y formación de cilindros en el lumen tubular.
-
Vasos sanguíneos renales (arteriolas aferente y eferente, vasa recta, capilares peritubulares):
- ¿Qué es? Red microvascular que irriga la nefrona y regula la presión de filtración glomerular.
- ¿Dónde actúa? Corteza hasta la médula renal.
- ¿Qué permite? Suministro de oxígeno, nutrientes y eliminación de desechos metabólicos.
- ¿Qué ocurre si se altera? Vasoconstricción prolongada o disfunción endotelial que reducen el flujo sanguíneo, favoreciendo hipoxia e isquemia.
-
Matriz extracelular y espacio intersticial:
- ¿Qué es? Red de colágeno, glicoproteínas y células intersticiales que brinda soporte estructural.
- ¿Dónde actúa? Entre túbulos y vasos del riñón.
- ¿Qué permite? Mantiene la arquitectura interna y propaga señales de reparación o inflamación.
- ¿Qué ocurre si se altera? Acumulación de matriz que induce fibrosis y reduce la capacidad de intercambio, favoreciendo daño crónico.
⚙️ Funciones y procesos
La lesión renal aguda afecta funciones fisiológicas y mecanismos celulares esenciales para la homeostasis sistémica; entre los procesos afectados destacan:
-
Filtración glomerular:
- Definición: Paso de agua y solutos pequeños desde la sangre hacia el espacio de Bowman, impulsado por diferencias de presión.
- Mecanismo fisiológico:
- Presión hidrostática capilar favorece el ultrafiltrado a través de la membrana basal glomerular.
- Podocitos y uniones de hendidura regulan la selectividad, evitando la pérdida de proteínas plasmáticas.
- Alteraciones:
- Daño endotelial, podocitos o aumento de presión intraglomerular reduce la tasa de filtración y favorece acumulación de productos nitrogenados y proteinuria.
-
Reabsorción tubular:
- Definición: Proceso activo y pasivo mediante el cual las células tubulares recuperan agua y solutos útiles del ultrafiltrado.
- Mecanismo fisiológico:
- Transportadores membranales y canales iónicos regulan el paso selectivo hacia el intersticio.
- La bomba Na+/K+-ATPasa mantiene gradientes para la reabsorción.
- Alteraciones:
- Daño tubular interfiere con los gradientes iónicos, causando pérdidas urinarias de solutos y agua, y alteraciones en el equilibrio corporal.
-
Regulación hemodinámica intrarrenal:
- Definición: Modulación continua de la resistencia arteriolar renal para preservar perfusión y presión glomerular ante cambios sistémicos.
- Mecanismo fisiológico:
- Retroalimentación túbulo-glomerular por mácula densa ajusta la resistencia arteriolar según sodio y flujo.
- Autacoides locales (prostaglandinas, óxido nítrico) modulan vasoconstricción y vasodilatación renal.
- Alteraciones:
- Disregulación or vasoconstricción persistente producen hipoperfusión e isquemia, afectando células tubulares.
-
Respuesta inflamatoria:
- Definición: Activación y reclutamiento de células inmunitarias locales que liberan citoquinas tras daño celular.
- Mecanismo fisiológico:
- DAMPs liberados por células dañadas atraen leucocitos y activan inflamación.
- Citoquinas aumentan permeabilidad vascular y estimulan fibrosis mediante células mesangiales y miofibroblastos.
- Alteraciones:
- Inflamación persistente promueve daño tisular, cicatrización desorganizada y pérdida funcional crónica.
-
Estrés oxidativo:
- Definición: Acumulación excesiva de especies reactivas de oxígeno (ROS) que superan la capacidad antioxidante celular.
- Mecanismo fisiológico:
- Hipoxia y daño mitocondrial aumentan producción de ROS que oxidan lípidos, proteínas y ácidos nucleicos.
- Alteraciones:
- Daño oxidativo incrementa necrosis y apoptosis, reduciendo la viabilidad celular y perpetuando el daño renal.
-
Alteración en concentración urinaria y equilibrio ácido-base:
- Definición: Capacidad del túbulo distal y colector para concentrar o diluir la orina y mantener la homeostasis ácido-base.
- Mecanismo fisiológico:
- Gradientes medulares y transportadores específicos permiten esta función.
- Intercambio H+/K+ en células intercaladas regula el equilibrio ácido-base.
- Alteraciones:
- Daño tubular impide la concentración urinaria y excreción adecuada de protones, favoreciendo acidosis metabólica y poliuria.
🔗 Integración funcional
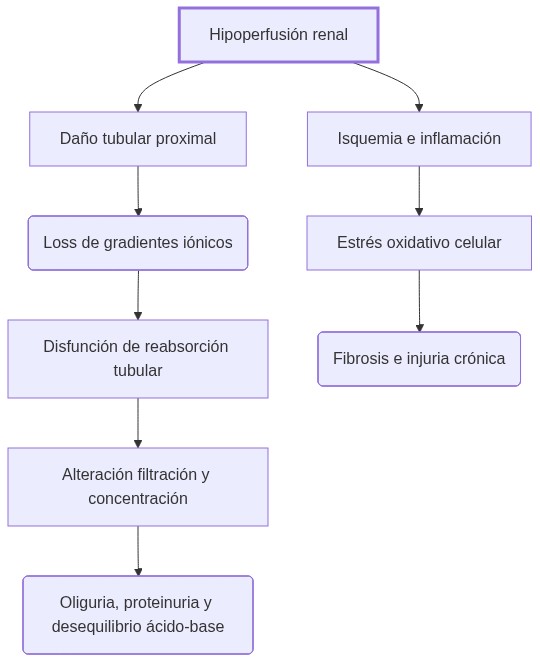
La fisiopatología de la lesión renal implica la interacción de múltiples mecanismos que perpetúan el daño y dificultan la recuperación. Por ejemplo, en isquemia tubular proximal:
- Se reduce el suministro de oxígeno por disminución del flujo sanguíneo.
- Las células epiteliales pierden ATP, esencial para mantener gradientes iónicos.
- Se altera el transporte activo provocando hinchazón celular y desorganización de uniones intercelulares.
- La membrana basal se ve comprometida, facilitando desprendimiento celular y formación de cilindros obstructivos.
- La obstrucción y flujo retrógrado elevan la presión intracapsular, reduciendo la filtración glomerular.
- La hipoxia activa la inflamación local con citoquinas y radicales libres.
- La inflamación y estrés oxidativo inducen fibrosis por proliferación de miofibroblastos, reemplazando tejido funcional.
Estos procesos se potencian mutuamente, creando un ciclo de daño estructural y disfunción funcional. El grado de reversibilidad depende de la extensión del daño y la capacidad de reparación.
🔬 Métodos y evidencias
La comprensión de la fisiopatología de la lesión renal aguda se basa en diferentes tipos de evidencia:
- Biopsias renales: Permiten analizar la arquitectura renal, detectando necrosis tubular, pérdida epitelial e infiltrado inflamatorio.
-
Análisis de biomarcadores:
- Moléculas en sangre y orina que reflejan daño celular, como creatinina, urea y proteínas de bajo peso molecular.
- Se utilizan para inferir grado y localización funcional de la lesión.
-
Modelos experimentales in vitro:
- Cultivo de células renales expuestas a estímulos isquémicos o tóxicos para estudiar mecanismos moleculares de daño y reparación.
-
Modelos animales in vivo:
- Organismos sometidos a lesiones controladas para evaluar la interacción de compartimentos renales y el impacto sistémico.
El estudio combinado de estos métodos permite analizar la dinámica de la lesión renal en distintos niveles biológicos.
🩺 Puente clínico
La fisiopatología de la lesión renal explica manifestaciones clínicas importantes como:
- Incremento de productos nitrogenados (urea, creatinina): Reflejan disminución del filtrado glomerular por daño funcional o estructural.
- Proteinuria: Indica alteración de la barrera de filtración glomerular con pérdida anormal de proteínas.
- Oliguria o poliuria: Modificaciones en la producción urinaria relacionadas con disfunción tubular o alteración en concentración urinaria.
Estos hallazgos permiten relacionar síntomas sistémicos, como edema e hiperkalemia, con mecanismos moleculares y celulares de la lesión renal.
Además, es relevante entender las fases de lesión reversible e irreversible para la evolución funcional.
💎 Perlas de alto rendimiento
- Filtración glomerular depende de la integridad estructural endotelial: y del gradiente de presión dentro del glomérulo.
- Túbulo proximal es la zona renal más susceptible a la isquemia: debido a su alta demanda metabólica y baja reserva de oxígeno.
- Destrucción de microvellosidades tubulares compromete la reabsorción: de solutos y agua, afectando la concentración urinaria.
- Citoquinas liberadas tras la lesión amplifican la inflamación: y promueven la fibrosis renal.
- Estrés oxidativo incrementa la muerte celular: y perpetúa el daño tisular renal.
- Retroalimentación túbulo-glomerular es clave para mantener la perfusión: y evitar daño tubular persistente.
- Equilibrio entre muerte celular y reparación determina la recuperación: de la función renal.
- Fibrosis convierte tejido funcional en matriz inerte: favoreciendo la cronicidad de la insuficiencia renal.
🧠 Puntos clave
- Lesión renal aguda representa una pérdida súbita de la función renal: de filtración y excreción renal como resultado de mecanismos celulares y tisulares.
- Daño funcional inicial puede ser reversible: mientras que la lesión estructural prolongada conduce a remodelado fibrótico irreversible.
- Fisiopatología integra alteraciones en la microcirculación: transporte tubular y respuesta inflamatoria renal.
- Pequeñas variaciones en la perfusión renal desencadenan cambios funcionales: significativos.
- Equilibrio entre agresión y reparación celular determina evolución: de la lesión renal.
- Alteración conjunta de estructuras y procesos fisiológicos explica cambios: en biomarcadores clínicos.
❓ Preguntas frecuentes
¿Por qué el túbulo proximal es particularmente vulnerable al daño hipóxico?
Porque requiere gran cantidad de oxígeno para la reabsorción activa y sus reservas energéticas son limitadas, por lo que la disminución del flujo sanguíneo afecta rápidamente su función.
¿Cómo se relacionan inflamación y fibrosis en la lesión renal aguda?
La inflamación activa células inmunitarias y citoquinas que estimulan la proliferación de miofibroblastos y producción excesiva de matriz extracelular, favoreciendo fibrosis.
¿Qué causa el aumento plasmático de creatinina y urea en la lesión renal?
La disminución de la tasa de filtración glomerular reduce la eliminación de estos productos, provocando su acumulación en plasma.
¿La lesión renal aguda siempre implica daño estructural irreversible?
No, en ocasiones el daño es funcional y reversible si se resuelve el insulto precozmente; la lesión prolongada puede causar daño irreparable.
¿Cómo distingue el riñón entre daño reversible e irreversible?
El daño reversible conserva la arquitectura celular y permite reparación, mientras que la muerte celular masiva y fibrosis intersticial indican daño irreversible.
¿Por qué se afecta la capacidad de concentración urinaria en la lesión renal?
Porque el daño tubular y la alteración del gradiente osmótico medular impiden que el riñón concentre o diluya adecuadamente la orina según la necesidad.
¿Qué indica la presencia de proteinuria en lesión renal aguda?
Daño significativo en la barrera glomerular permite el paso y pérdida anormal de proteínas plasmáticas hacia la orina.
¿Por qué es esencial la regulación hemodinámica intrarrenal en la lesión renal?
Porque regula el flujo sanguíneo y presión glomerular necesarios para preservar la función renal frente a cambios hemodinámicos y daño.
Evaluación Interactiva Progresiva
Este cuestionario evalúa la comprensión del contenido biológico sobre la fisiopatología de la lesión renal aguda presentado en el artículo.
Nivel 1 – Básico
¿Qué define a la lesión renal aguda según el artículo?
¿Dónde se localiza principalmente el glomérulo dentro del riñón?
¿Cuál es una función principal del túbulo proximal según el artículo?
Nivel 2 – Intermedio
Según el texto, ¿qué relación es correcta entre el daño en podocitos y la función glomerular?
¿Cuál de las siguientes alteraciones ocurre debido al daño isquémico en el túbulo proximal?
¿Cómo se relaciona la vasoconstricción prolongada en vasos sanguíneos renales con la fisiopatología descrita?
Nivel 3 – Avanzado
En el contexto de isquemia tubular proximal, ¿qué secuencia correcta explica el ciclo de daño y disfunción descrito?
¿Cuál es la consecuencia funcional de la inflamación persistente y el estrés oxidativo en la lesión renal aguda?
Si hay daño tubular que afecta la concentración urinaria, ¿qué alteraciones sistémicas pueden ocurrir según el artículo?
📚 Estudia más sobre el tema
- 🔎 Artículos científicos revisados en PubMed
- 🩻 Información de salud global en Organización Mundial de la Salud (WHO)
- 🦠 Datos clínicos y epidemiológicos en Centers for Disease Control and Prevention (CDC)
Contenido educativo. No sustituye la enseñanza formal ni el juicio clínico.